RMITの科学者たちは、危険なスーパーバグによる耐性を回避するために、迅速に遺伝子組み換えができる新しいタイプの抗生物質を開発しました。 RMIT scientists have created a new type of antibiotic that can be rapidly re-engineered to avoid resistance by dangerous superbugs.
2023-02-07 ロイヤルメルボルン工科大学(RMIT)
◆「プリシリシジン」と名付けられたこの抗生物質は、アミノ酸の構成要素が小さいため、さまざまな種類の抗菌剤耐性に対応するよう調整することが可能です。
◆プリシリシジンは、抗菌ペプチドの一種である。このペプチドは、細菌やウイルスに対する最初の防御として、すべての生物によって産生される。
◆抗菌ペプチド分子工学に関する文献を調査し、20種類の短いペプチドを設計・試験した結果、Priscilicidinが最有力候補に選ばれたのです。プリシリシジンは、牛の免疫系に含まれる天然の抗生物質であるインドリシジンから派生したものである。2023年1月にFrontiers in ChemistryのWomen in Nanoscience 2022特集号で発表された研究チームの研究によると、プリシリシジンは、ゴールデンスタフ、大腸菌、カンジダ真菌などの耐性微生物株に対して高い活性を示すことがわかった。プリシリシジンは、微生物の膜を乱すことで作用し、最終的に細胞を死滅させる。
◆研究チームの研究によると、プリシリシジンの分子は自然にハイドロゲル状に自己集合するので、抗生物質のゲルやクリームを作るのに理想的だという。
◆ Frontiers in Chemistry (DOI: 10.3389/fchem.2022.1009468) で公開されました。
<関連情報>
- https://www.rmit.edu.au/news/all-news/2023/feb/priscilicidin
- https://www.frontiersin.org/articles/10.3389/fchem.2022.1009468/full
ナノ構造ハイドロゲルへの組込みが可能な強力な超短期抗菌ペプチドの合理的デザイン Rational design of potent ultrashort antimicrobial peptides with programmable assembly into nanostructured hydrogels
Priscila Cardoso, Samuel Appiah Danso, Andrew Hung, Chaitali Dekiwadia, Nimish Pradhan, Jamie Strachan, Brody McDonald, Kate Firipis, Jacinta F. White, Arturo Aburto-Medina, Charlotte E. Conn and Céline Valéry
Frontiers in Chemistry Published: 13 January 2023
DOI:https://doi.org/10.3389/fchem.2022.1009468
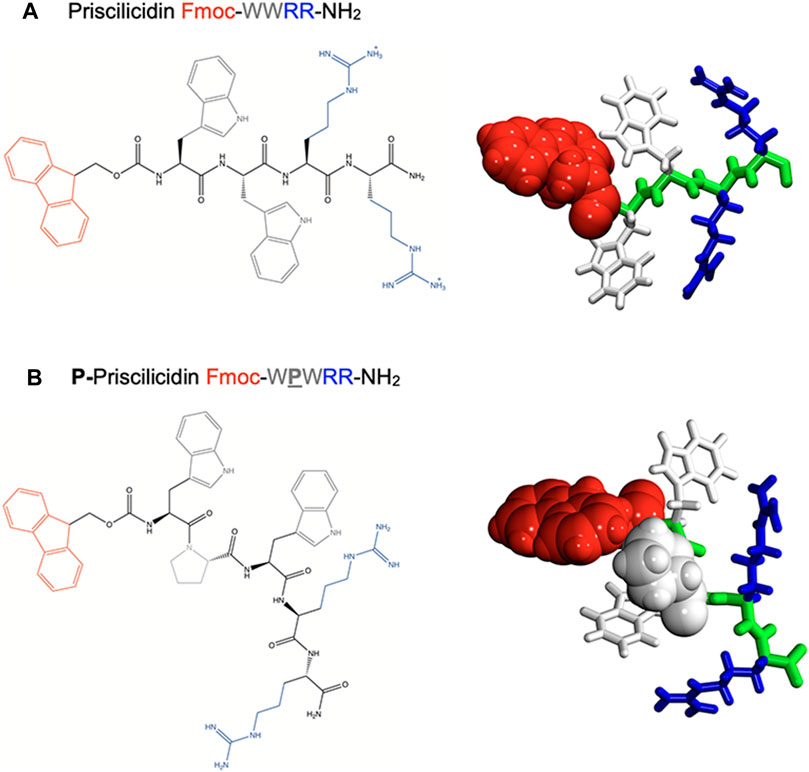
Microbial resistance to common antibiotics is threatening to cause the next pandemic crisis. In this context, antimicrobial peptides (AMPs) are receiving increased attention as an alternative approach to the traditional small molecule antibiotics. Here, we report the bi-functional rational design of Fmoc-peptides as both antimicrobial and hydrogelator substances. The tetrapeptide Fmoc-WWRR-NH2—termed Priscilicidin—was rationally designed for antimicrobial activity and molecular self-assembly into nanostructured hydrogels. Molecular dynamics simulations predicted Priscilicidin to assemble in water into small oligomers and nanofibrils, through a balance of aromatic stacking, amphiphilicity and electrostatic repulsion. Antimicrobial activity prediction databases supported a strong antimicrobial motif via sequence analogy. Experimentally, this ultrashort sequence showed a remarkable hydrogel forming capacity, combined to a potent antibacterial and antifungal activity, including against multidrug resistant strains. Using a set of biophysical and microbiology techniques, the peptide was shown to self-assemble into viscoelastic hydrogels, as a result of assembly into nanostructured hexagonal mesophases. To further test the molecular design approach, the Priscilicidin sequence was modified to include a proline turn—Fmoc-WPWRR-NH2, termed P-Priscilicidin–expected to disrupt the supramolecular assembly into nanofibrils, while predicted to retain antimicrobial activity. Experiments showed P-Priscilicidin self-assembly to be effectively hindered by the presence of a proline turn, resulting in liquid samples of low viscosity. However, assembly into small oligomers and nanofibril precursors were evidenced. Our results augur well for fast, adaptable, and cost-efficient antimicrobial peptide design with programmable physicochemical properties.