2018/10/23 国立医薬品食品衛生研究所,日本医療研究開発機構
ポイント
- 臨床データに基づき3種類のリスクに分類された28種類の医薬品を用いて、ヒトiPS細胞由来心筋細胞の電気活動を記録する多点電極システム法により、医薬品の致死性不整脈の発生リスクに関する国際的な検証試験を行いました。
- 国際検証チームによって、ヒトiPS細胞由来心筋細胞を用いてヒトにおける医薬品の致死性不整脈の発生リスクを評価する方法を確立しました。
- ヒトiPS細胞由来心筋細胞が医薬品に対する安全性薬理試験のツールとして活用していくことが期待されます。
概要
国立医薬品食品衛生研究所・薬理部の諫田泰成薬理部長及び日本安全性薬理研究会澤田光平理事が主導するJapan iPS Cardiac Safety Assessment(JiCSA)は、現在AMEDから研究支援を受けて、ヒトiPS細胞由来心筋細胞を用いた試験法の開発と検証実験に取り組んでいます。当研究グループはこれまで、薬剤誘発性の致死性不整脈の発生予測に関する大規模な国内検証実験を行い、高い予測度を有することを明らかにしてきました。
本研究では、米国食品医薬品局(FDA)を中心に組織された国際コンソーシアムCiPA注5と共同で、国際検証試験を実施しました。米国がんセンターからコード化された28化合物が提供され,日本からは、JiCSA検証試験チームとしてエーザイ、LSIメディエンスが実験データセットをFDAに提出し、検証試験を実施しました。研究グループでは、これらの検証をもとに、実験データの解析・議論を経て論文を作成し,ヒトiPS細胞由来心筋細胞を用いた薬剤誘発性の致死性不整脈の発生リスクに関する試験法の有用性を明らかにしました。本研究により、ヒトiPS細胞由来心筋細胞は、医療の場において懸念される薬剤誘発性の致死性不整脈を高精度に予測し、薬物による死亡事故を未然に防ぐための有効なツ-ルになりうることを示すことができました。本研究の成果は、ヒトiPS細胞由来心筋細胞を用いた新たな試験法の再現性や信頼性を担保する科学的根拠となり、今後のヒトiPS細胞由来心筋細胞を用いた試験法の議論に大きな影響を与えるものと期待されます。
ヒトiPS細胞の実用化に関して、分化細胞を移植する再生医療等製品の活用のほか、医薬品の開発段階における有効性/安全性評価での利用が期待されています。本研究では、ヒトiPS心筋細胞が予測性の高い安全性評価法として実用可能であることを国際検証試験として初めて示したものです。AMEDにおいても画期的な成果と捉えており、今後、ヒトiPS細胞技術を用いた安全性評価法の確立に向けて、レギュラトリーサイエンス研究がさらに進展し、安全性担保の観点から創薬ストラテジーに変革が起こることを期待しています。
なお、この成果に関する論文は、「Cell Reports」のオンライン版に9月25日に掲載されました。
本研究は、国立医薬品食品衛生研究所・前薬理部長・関野祐子および現薬理部長・諫田泰成が代表をつとめた日本医療研究開発機構 医薬品等規制調和・評価研究事業 「ヒトiPS分化細胞技術を活用した医薬品の次世代毒性・安全性評価試験系の開発と国際標準化に関する研究」で行われた研究成果です。
背景
医薬品を開発する際の承認審査プロセスは、薬効や毒性・安全性について動物や細胞などを用いて評価する非臨床試験と、実際に医薬品をヒトに投与して有効性を判断する臨床試験に分けられます。このうち非臨床試験では様々な臓器に対する安全性の確保が求められており、特にICH(医薬品規制調和国際会議)の非臨床試験ガイドラインの安全性薬理試験(S7B)では、心筋など循環器機能に対する作用を詳細に調べることが義務付けられています。
心電図のQT間隔を延長させる薬剤の中には、Torsades de Pointes (TdP)注1といわれる致死性不整脈を誘発するものがあり、これが原因で市場から撤退した薬剤が数多くあります。このため、医薬品候補化合物のTdP誘発リスクを、創薬プロセスの早期の段階から高精度に予測することは、患者さんに対する安全性の担保並びに医薬品開発の成功確率を上げるために極めて重要です。そのため、現行のS7Bガイドラインでは、医薬品のhERG(human ether-a-go-go related gene)チャネル注2に対する影響を調べ、動物を用いて心電図のQT間隔を評価することにより、致死性不整脈を引き起こす可能性が高い医薬品をチェックしています。しかし、これまでの研究によりhERGチャネル阻害作用の強い化合物がすべて致死性不整脈を引き起こすわけではないことなどが明らかになり、新たな科学技術の導入によるヒトTdPリスクの予測性向上が期待されています。
2007年にヒトiPS細胞が発見されたことを契機に、ヒトiPS細胞から様々な臓器細胞に分化させた細胞を創薬へ利活用する動きが加速しています。ヒトiPS細胞由来心筋細胞 (ヒトiPS心筋細胞)注3はヒトの心臓に発現している複数のイオンチャネルを兼ね備えていることから、医薬品による重篤な致死性不整脈の発生リスクを予測できるツールとして期待されています。とりわけ日本は、オールジャパン体制のコンソーシアムであるJapan iPS Cardiac Safety Assessment (JiCSA)注4を組織し、これまでに国内における大規模検証試験を実施して、ヒトiPS心筋細胞を用いた催不整脈リスク予測法の有用性を提示してきました(Ando et al., J Pharmacol Toxicol Method, 2017)。さらに、ヒトiPS心筋細胞株を追加して、催不整脈リスクの予測ができることを示しました(Yamazaki et al., J Pharmacol Sci, 2018)。一方で、コード化した化合物の使用、統計処理などの点で検証方法に課題が残されていました。
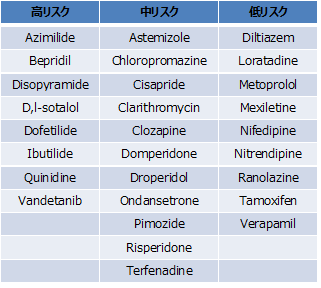
本研究グループは、ヒトでのTdPリスクをもとにして28薬剤を選定して3つのリスクに分類し(表1)、多点電極システム、光学測定による大規模検証試験を行いました。統計的な解析を行い、薬剤のヒトでのTdPの発生状況を比較した結果、ヒトiPS細胞由来心筋細胞を用いた方法は再現性が高く、高精度(AUC=0.8722)にヒトの薬剤誘発性のTdPリスクを分類できることが示されました(図1)。以上のように、研究グループは、国際検証試験により、ヒトiPS細胞由来心筋細胞を用いたヒトでの薬剤誘発性の致死性不整脈のリスクを評価できることを明らかにし、その有用性を示しました。現在、ICHガイドラインS7Bの改訂に向けて議論が行われておりますが、本研究成果により科学的な根拠を取得することができました。今後、ヒトiPS細胞由来心筋細胞を用いた医薬品安全性試験への利用が、飛躍的に進むことが期待されます。
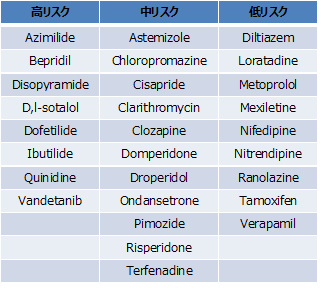
表1. 国際検証試験で用いた28種類の医薬品とリスク分類
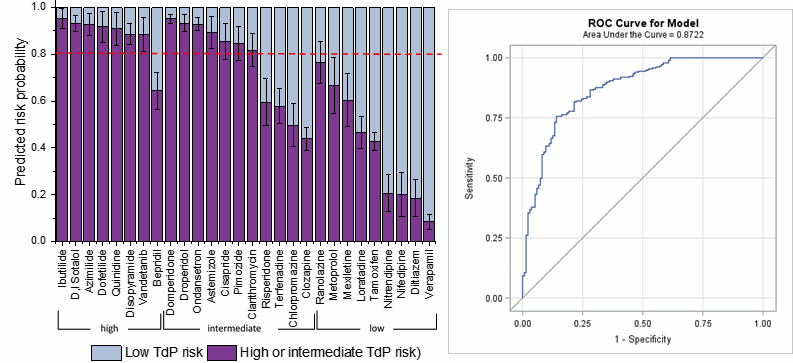
図1. ヒトiPS心筋細胞を用いた医薬品による致死性不整脈の発生リスクの予測
(左)催不整脈リスクの異なる医薬品28種類を高リスク(8種類)、中リスク(10種類)、低リスク(9種類)に分類し、それぞれ予想リスク確率の高い順番に並べた。
(右)棒グラフから算出したROC(Receiver Operatorating Characteristic、受信者動作特性)曲線と曲線下面積(AUC=0.8722)を示す。AUCの値が予測精度を意味する。
効果
本研究成果により、ヒトiPS細胞技術を活用することにより、医療の場において懸念される医薬品によって誘発される致死性不整脈を再現性よく高精度に予測できることを明らかにしました。ヒトiPS細胞由来心筋細胞は薬剤性の致死性不整脈を予測する研究ツールとなり得るため、被験者の安全性を確保するための有効な手法であることが示唆されます。さらに、創薬においてヒトiPS細胞由来心筋細胞の利用が促進されることが期待されます。
今後の展望
現在、ICH S7Bガイドラインの改訂に関する国際的な議論が行われており、ヒトiPS細胞技術を活用した試験法のS7Bガイドラインでの記載が提案されています。本研究成果は、その提案を支持するための科学的根拠になるものと考えます。
論文
- 論文誌:Cell Reports(2018年9月25日オンライン掲載)
- 著者:Ksenia Blinova, Qianyu Dang, Daniel Millard, Godfrey Smith, Jennifer Pierson, Liang Guo, Mathew Brock, Hua Rong Lu, Udo Kraushaar, Haoyu Zeng, Hong Shi, Xiaoyu Zhang, Kohei Sawada, Tomoharu Osada, Yasunari Kanda, Yuko Sekino, Li Pang, Tromondae K. Feaster, Ralf Kettenhofen, Norman Stockbridge, David G. Strauss, Gary Gintant
- タイトル:International Multisite Study of Human-Induced Pluripotent Stem Cell-Derived Cardiomyocytes for Drug Proarrhythmic Potential Assessment
(薬剤誘発性不整脈発生リスク評価のためのヒトiPS細胞由来心筋細胞を用いた国際多施設検証試験) - Doi:10.1016/j.celrep.2018.08.079
用語解説
- 注1.Torsades de pointes(TdP)
- 致死性の心室性不整脈の1つで、突然死の原因になり得ます。心電図のQT間隔延長がTdPにつながるマーカーとして使用されています。
- 注2.hERGチャネル
- 心筋細胞に存在するカリウムチャネルの1つです。hERGチャネルが阻害されると、心電図のQT時間が延長し、不整脈が起こる可能性が高くなります。
- 注3.ヒトiPS細胞由来心筋細胞
- ヒトiPS細胞から分化誘導により作成された心筋細胞で、ヒト細胞として利用されています。
- 注4.JiCSA(Japan iPS Cardiac Safety Assessment)
- ヒトiPS細胞由来心筋細胞を医薬品の安全性評価に応用することを目的に、産・官・学で構成されたオールジャパン体制の研究グループです。国立医薬品食品衛生研究所・薬理部長の諫田泰成が研究代表を務めています。
- 注5.CiPA(Comprehensive in vitro Proarrhythmia Assay)
- 米国FDA(食品医薬品局)を中心に組織された国際コンソーシアムで、ヒトiPS心筋細胞などを含めた統合的な催不整脈リスク予測法の確立を目指しています。諫田泰成はCiPA運営委員のメンバーを務めて、JiCSAはCiPAと共同研究を行っています。
お問い合わせ先
本研究成果に関するお問い合わせ先
諫田 泰成(かんだ やすなり)
国立医薬品食品衛生研究所 薬理部
澤田 光平(さわだ こうへい)
国立大学法人東京大学 大学院薬学系研究科
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
創薬戦略部 医薬品等規制科学課