脳内タウ病変の可視化により病期の客観的評価法を確立、治療薬開発を促進
2019-03-27 量子科学技術研究開発機構
発表のポイント
- 運動機能障害と認知機能障害が急速に進行する進行性核上性麻痺1)患者の生体脳に蓄積したタウタンパク質2)(以下、タウ)を可視化し、その量や分布を調べた
- タウ蓄積の量が運動機能障害や認知機能障害の重症度と関連し、タウ蓄積がみられる脳領域の分布を評価することで病気の進行度を客観的に評価できることがわかった
- タウを生体で可視化する技術は、同様の病気を持つ患者の診断に有用であるのみならず、さまざまな認知症や神経難病で神経障害に関与するタウの蓄積を抑える治療薬の効果を確認する技術としても有用と期待され、現在臨床試験を実施中である
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫、以下「量研」)放射線医学総合研究所脳機能イメージング研究部の遠藤浩信客員協力研究員と島田斉主幹研究員らは、千葉大学大学院医学研究院・神経内科学の桑原聡教授らと共同で、運動および認知機能の障害が急速に進行する進行性核上性麻痺患者の生体脳に蓄積するタウを可視化し、その蓄積量が神経症状の重症度と関連すること、タウ蓄積が見られる脳領域の広がりが病期の客観的な指標となることを明らかにしました。
進行性核上性麻痺は40歳以降、平均60歳代で発症し、大脳基底核3)、脳幹部4)、小脳5)といった部位の神経細胞が減少して、転びやすい、下方を見ることが難しい、しゃべりにくい、飲み込みにくいなどの症状がみられる疾患です。パーキンソン病6)と似た症状が現れますが、パーキンソン病にはよく効く薬があまり効かず、病気の進行も早くしばしば早期から寝たきりになるため、新しい診断法や治療法の開発が切望されている神経難病のひとつです。
これまで、進行性核上性麻痺患者の死後脳を解析した研究では、脳内の病理変化としてタウ蓄積が認められることが確認されていましたが、臨床症状や病気の進み具合(病期)との関連は十分には明らかとなっていませんでした。そこで、量研で開発した生体脳でタウを可視化するPET7)技術を用いて、進行性核上性麻痺の患者を対象にタウ蓄積の量や分布と、臨床症状や病期との関連を調べました。
その結果、進行性核上性麻痺患者においては前頭頭頂葉8)、大脳基底核、脳幹部、小脳などを含むさまざまな脳部位にタウ蓄積が認められることがわかりました。さらに、前頭頭頂葉のタウ蓄積が運動機能障害や認知機能障害の重症度と関連しており、重度の機能障害を呈する進行した患者においては、タウ蓄積の量だけでなく蓄積している脳領域の範囲もより広範となっていることを見出しました。これらのことは、タウの脳内蓄積が進行性核上性麻痺の多様な臨床症状に関与していることを示すだけでなく、PETを用いたタウの脳内蓄積の評価が、病期の客観的な評価指標になり得ることを示唆するものです。
本成果により、今後、タウ蓄積を認める進行性核上性麻痺を含む多くの認知症や神経難病において、多様な臨床症状をもたらす脳の病態解明に加えて、早期診断や重症度判定、神経障害に関与するタウの蓄積を抑える治療薬の効果判定ならびにその開発が促進されると期待されます。現在我々は、この技術を用いて、脳内にタウが蓄積することで認知機能障害と運動障害が出現する神経難病を対象に、脳内タウ蓄積を抑えることが期待される薬物の治療効果を調べる臨床試験を行っています。
本研究は、日本医療研究開発機構(AMED)革新的技術による脳機能ネットワークの全容解明プロジェクト「脳老化病態カスケードのトランスレータブルなイメージングとメカニズム制御の研究開発」および「精神疾患の神経回路-分子病態解明とモデル化」、認知症研究開発事業「タウを標的とする新規画像診断法と治療法の研究開発コンソーシアム構築」、MEXT科研費JP26713031、脳タンパク質老化と認知症制御「脳イメージングを基軸としたタンパク質老化モデルの治療評価系の開発」、脳内環境・恒常性維持機構とその破綻「毒性伝達機構の分子イメージングを基軸とした神経変性疾患研究」などの支援を受けて実施されたもので、当該分野においてインパクトの大きい論文が数多く発表されている米国の科学誌「Movement Disorders」のオンライン版に2019年3月27日(水)14:00(日本時間)に掲載されます。
研究開発の背景と目的
近年、先進各国では軒並み高齢化率9)が高くなり続けています。中でも日本は高齢化率が世界で一番高く、今後も総人口に占める高齢者人口の割合は増え続けると推定されています。高齢者が増えていることで、高齢者に多いアルツハイマー型認知症10)に代表される認知症やパーキンソン病などさまざまな神経難病の患者数も、近年右肩上がりに増加しています。
認知症や神経難病においては、さまざまな認知機能障害や運動機能障害が出現しますが、異なる病気であってもしばしば似たような症状が出るために正確な診断をすることが困難です。ところが、病気によって薬の効果や適切な治療法は異なるため、誤った診断が不適切な治療やケアにつながるという危険性があります。
進行性核上性麻痺は、眼球運動の障害、左右対称性の運動障害、前頭葉機能障害を認め、発症早期から転倒を繰り返す進行性の神経難病で、指定難病11)のひとつです。日本における患者数は、人口10万人あたり10~20人程度と推測されています。病早期はパーキンソン病とよく似た症状を呈しますが、パーキンソン病で用いられる治療薬はほとんど効果がありません。また、パーキンソン病との区別が難しい上に症状の進行が早く、発症後2~3年で車いす、4~5年程度で寝たきりになると報告されています。原因についてもわからないことが多く、いまだに確立した治療法がありません。
これまで、進行性核上性麻痺患者の死後脳を解析した研究では、脳内の病理変化としてタウ蓄積が認められることが確認されていました。これまでに脳内にタウ蓄積を認めるさまざまな認知症や神経難病において、タウ蓄積が神経障害に密接に関連していることが報告されており、タウはこれらの疾患における新たな治療標的として注目されています。しかし、進行性核上性麻痺においては、生体脳でのタウ蓄積と臨床症状との関連は十分には明らかとなっていませんでした。
研究グループはこれまでに、量研が開発したPETにより生体脳でタウを可視化する技術を用いて、アルツハイマー型認知症でみられる意欲低下の症状や、特定地域で多発する認知症で現れるさまざまな症状、前頭側頭型認知症の病気の進行度、それぞれについてタウ蓄積の関係などを明らかにしてきました。そこで本研究では、この技術を用いて、進行性核上性麻痺患者を対象に、タウ蓄積の量ならびに分布と、臨床症状との関連を明らかにする研究を行いました。
研究の手法と成果
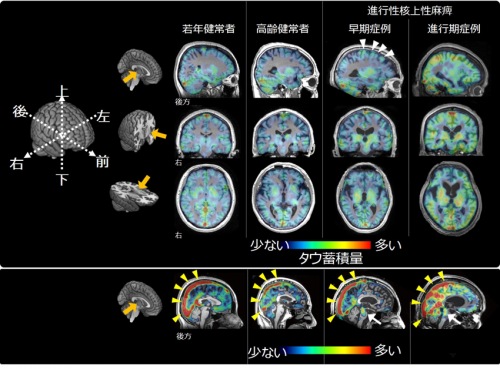
本研究では、進行性核上性麻痺患者13名、健常高齢者13名を対象に、PET薬剤である11C-PBB312)を用いてタウ蓄積が認められる脳部位とその量を調べました。その結果、進行性核上性麻痺患者では前頭頭頂葉、大脳基底核、脳幹部、小脳などを含むさまざまな脳部位にタウ蓄積を認めました(図1)。
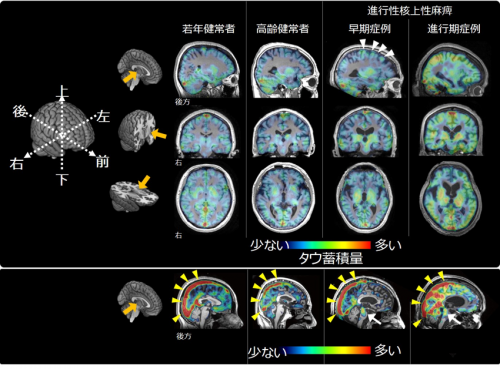
図1 代表的な進行性核上性麻痺患者におけるタウ蓄積
11C-PBB3 PETで調べた結果、進行性核上性麻痺患者においては、健常高齢者と比較して、
脳幹部(白矢印)、大脳基底核、前頭頭頂葉(白矢頭)を含む脳領域にタウが多く蓄積していた。
(※黄色矢頭は静脈の信号)
次に進行性核上性麻痺患者を運動機能障害が軽度の症例と重度の症例に分けると、運動機能障害が重度な症例では軽度な症例と比較して、タウ蓄積を認める脳部位がより広範な領域となっており、タウ蓄積の量も多くなっていました(図2)。
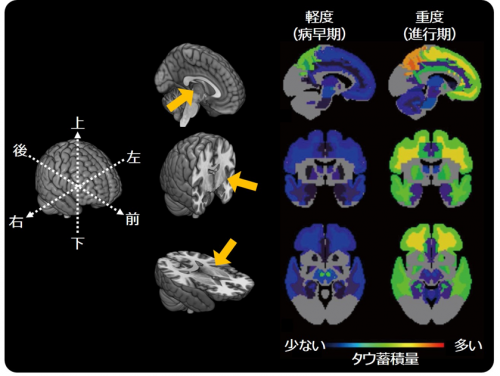
図2 病期と脳内タウ蓄積の関連
運動機能障害が重度なより病期が進行している症例では、運動機能障害が軽度な病早期症例と比べて、
脳の広い領域に多くのタウ蓄積を認める。
さらに脳の各領域におけるタウ蓄積と、臨床症状との関連を調べました。その結果、前頭頭頂葉のタウ蓄積量が多いほど、運動および認知機能の障害が重度でした(図3)。
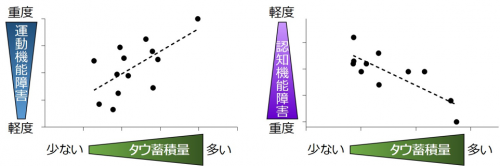
図3 脳内タウ蓄積と運動および認知機能の障害の関連
前頭頭頂葉のタウ蓄積量が多いほど運動と認知機能の障害も重度となっている。
今回PET検査を行った症例とは異なる、すでに亡くなっている進行性核上性麻痺患者の脳を用いて、脳内のPBB3結合と脳病理の関連を検討すると、PET検査の結果と同様、前頭葉の運動皮質には多量の脳内タウ蓄積を認め、PBB3が結合していることが確認されました(図4)。
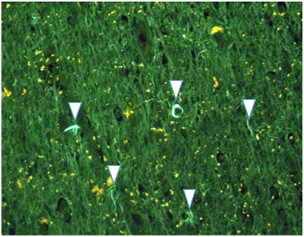
図4 死後脳におけるタウ蓄積とPBB3集積
前頭葉の運動機能に関連する脳領域には、脳内タウ蓄積が多数存在し、PBB3が結合している
今後の展開
本研究で進行性核上性麻痺患者におけるタウ蓄積は運動と認知機能の障害に密接に関連していること、ならびに症状が重度な進行例においてはタウ蓄積を認める脳部位が広がっていることがわかりました。これにより、今後、タウ蓄積を認める多くの認知症や神経難病において多様な臨床症状をもたらす脳の病態解明や進行性核上性麻痺の早期診断法、重症度判定法の開発が進むと期待されます。
また、生体脳でタウを可視化する技術は、タウの脳内蓄積を認めるさまざまな認知症や神経難病の診断や、神経障害に関与するタウの蓄積を抑える治療薬の開発における有用性が期待されています。本研究でも、PETで評価したタウの蓄積領域の広がりが、進行性核上性麻痺の病期の客観的な指標になることが示されました。そこで現在我々は、この技術を用いて進行性核上性麻痺ならびに単一の遺伝子異常によりタウの脳内蓄積が起こる遺伝性の前頭側頭型認知症を対象に脳内タウ蓄積を抑えることが期待される薬物の治療効果を調べる臨床試験(UMIN試験ID:UMIN000030527)を行っています。
このプレスリリースは『Movement Disorders』のオンライン版に掲載される「Endo H, et al. In vivo binding of a tau imaging probe, [11C]PBB3, in patients with progressive supranuclear palsy (邦題:進行性核上性麻痺患者におけるタウイメージング用製剤[11C]PBB3の生体内結合に関する検討)」に基づいて作成されています。
用語解説
1)進行性核上性麻痺
眼球運動障害、左右対称性の運動障害、前頭葉機能障害を認め、転倒を繰り返すパーキンソン病類縁疾患。神経難病の一つで、病初期はパーキンソン病との区別が困難なこともあるが、パーキンソン病ではよく効く薬もほとんど効果を示さず症状進行も急速で、確立した治療法はない。
2)タウタンパク質
神経系細胞の骨格を形成する微小管に結合するタンパク質。細胞内の骨格形成と物質輸送に関与している。アルツハイマー型認知症をはじめとする様々な精神神経疾患において、タウが異常にリン酸化して細胞内に蓄積することが知られている。
3) 大脳基底核
脳の表面(大脳皮質)と脳幹部などを結ぶ神経細胞が集まる脳部位。運動の調節にかかわるほか、認知機能や感情、動機付けなどさまざまな機能を担っている。
4)脳幹部
脳の中でも重要な機能が集中している部位。意識と覚醒、運動機能、感覚機能、自律神経機能などに関わるさまざまな神経回路が存在している。
5)小脳
大脳の下部で脳幹部の背側に位置する脳部位。知覚と運動機能を統合する機能を担っており、精緻な運動の制御のほか、自転車の乗り方などに代表される運動学習にかかわる機能を担っている。
6)パーキンソン病
手足がふるえる、体の動きがゆっくりとぎこちなくなる、転びやすくなるなどの症状が順次進行性に出現する神経難病。かなりの割合の患者で認知機能障害も出現する。
7)PET
陽電子断層撮影法(Positron Emission Tomography)の略称。身体の中の生体分子の動きを生きたままの状態で外から見ることができる技術の一種。特定の放射性同位元素で標識したPET薬剤を患者に投与し、PET薬剤より放射される陽電子に起因するガンマ線を検出することによって、体深部に存在する生体内物質の局在や量などを三次元的に測定できる。
8)前頭頭頂葉
脳の前方に位置する前頭葉とその後方に位置する頭頂葉のこと。進行性核上性麻痺で障害されやすい脳領域で、前頭葉は運動、言語処理、思考や判断など、頭頂葉は空間感覚などを中心とした感覚情報の統合などの機能を担っており、さらに前頭葉と頭頂葉が結びついて運動の発現や調節、注意の制御などが行われるとされている。
9) 高齢化率
総人口に占める65歳以上人口の割合のこと。7-14%で高齢化社会、14-21%で高齢社会、21%を超えると超高齢社会と呼ばれるが、日本は2010年に超高齢社会に突入している。2018年度高齢社会白書によれば、2017年10月1日時点での高齢化率は27.7%で、2065年には38.4%に達して、国民の約2.6人に1人が65歳以上の者となる社会が到来すると推計されている。
10)アルツハイマー病
認知症の原因として最も多い病気。脳内に異常タウタンパクやアミロイドが蓄積して、進行性に物忘れなどが目立つ認知機能障害が出現する。
11) 指定難病
「難病の患者に対する医療等に関する法律」(難病法)により規定される難病のうち、「患者数が本邦において一定の人数(人口の約0.1%程度、およそ12万人強)に達しないこと」、「客観的な診断基準(またはそれに準ずるもの)が成立していること」の2要件を満たす疾患。平成31年2月1日現在では331疾患が指定難病とされており、公的な医療費助成の対象となる。
12)11C-PBB3
量研が開発した、脳内に蓄積したタウに対して選択的に結合する薬剤。PBB3のPBBはPyridinyl-Butadienyl-Benzothiazoleの略称。蛍光物質であることから、生体蛍光画像を得るのにも利用できるが、PBB3を放射性同位元素で標識することにより、PET薬剤として使用できる。生体蛍光画像は細胞レベルの詳細な観察を可能にするが、脳の深部を観察することは困難である。PETは脳の深部観察を可能にし、ヒトにも応用可能である。