骨格筋疾患の病態解明、治療薬の開発に期待
2018-01-30 慶應義塾大学医学部 国立研究開発法人日本医療研究開発機構
慶應義塾大学医学部坂口光洋記念講座(システム医学教室)の洪実教授らは、ヒト多能性幹細胞であるES細胞、iPS細胞(以下、多能性幹細胞)(注1)から、5日間で80%以上という、短期間かつ高い確率で骨格筋細胞に分化させる「細胞分化RNAカクテル」を開発することに成功しました。
この「細胞分化RNAカクテル」は転写因子の合成RNAと低分子二本鎖RNA(以下、siRNA)を合わせたもので、多能性幹細胞に添加するだけで、筋線維を形成する単位であるサルコメア構造や細胞の融合能を有する機能的な骨格筋細胞を作製することができます。
この方法は、細胞のゲノムDNAを損傷することがないため、ゲノムに遺伝子を挿入して多能性幹細胞を目的の細胞に分化させる方法に比べて、より安全であると考えられます。また、転写因子を単独で導入する従来の方法に比べ、効率を大きく高めることに成功し、細胞移植や創薬スクリーニングに必要とされる大量の骨格筋細胞の生産が可能となりました。本研究の成果は、骨格筋細胞の基礎研究のみならず、骨格筋の異常で起こるさまざまな病気の病態解明、治療薬の開発などに役立つことが期待されます。
この結果は、2018年1月19日(英国時間)に『Scientific Reports』のオンライン版に掲載されました。
研究の背景と概要
多能性幹細胞は、体を構成するさまざまな細胞に分化可能であり、再生医療や新薬の開発研究への応用が期待されています。多能性幹細胞を目的の組織や器官の細胞へと分化させる方法のひとつに、分化に必要な遺伝子群の働きをオンにする転写因子(注2)を人工的に細胞へ導入させる方法があります。この分化誘導法の優れた点は、転写因子の導入を介して遺伝子の発現パターンを、目的の細胞へ直接的に転換できるところであり、短期間に均一な分化細胞を作り出すことが可能です。
近年では、転写因子をコードする合成RNA(注3)を試験管内で作製し、多能性幹細胞に導入する方法が開発され、ゲノム改変を伴わない簡便かつ安全な分化誘導系として広く普及しつつあります。しかしながら、多能性幹細胞には、高い未分化維持性が存在し、分化に関わる転写因子を導入しても、迅速な分化が行われないという問題点がありました。事実、比較的分化誘導を起こしやすい線維芽細胞を骨格筋へと形質転換させるマスター転写因子MYOD1の導入による分化誘導にすら、多能性幹細胞は高い抵抗性を示すことが知られています。
今回、研究グループでは、多能性幹細胞が分化誘導に示す抵抗性の原因の1つを解明し、この知見をもとに合成RNAを用いた分化誘導法を改良し、多能性幹細胞から骨格筋細胞を効率よく分化誘導することに成功しました。まず、従来通り筋細胞分化のマスター転写因子であるMYOD1の合成RNAを単独で多能性幹細胞に導入したところ、分化誘導がほとんど起こらないことが確認されました。分化誘導を阻害する遺伝子を特定するため免疫化学染色法によりMYOD1の導入された細胞に存在する複数の未分化関連因子の発現を調べた結果、未分化性を担う遺伝子POU5F1(OCT3/4)(以下、POU5F1)が残存していることがわかりました(図1)。また、POU5F1があるとMYOD1が遺伝子を制御するゲノム領域に結合できないことも明らかとなり、この分子がMYOD1の働きを妨げている可能性が考えられました。
【図1】
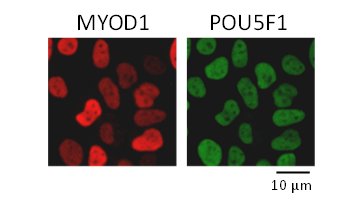
図1.MYOD1の合成RNAを導入した多能性幹細胞。MYOD1を赤の蛍光標識、POU5F1を緑の蛍光標識でラベルした。MYOD1の導入が確認された(左)とともに、POU5F1が残存していることを確認した(右)。MYOD1を導入しても多能性幹細胞の未分化性を担うPOU5F1が残存しているため、MYOD1は機能することができない。
そこでPOU5F1を選択的に抑制するsiRNAと MYOD1の合成RNAを合わせたカクテル(「細胞分化RNAカクテル」)を作成し、多能性幹細胞に添加したところ、分化誘導開始から5日目に80%の細胞が骨格筋マーカーであるMyHCを発現していました。また、この細胞はサルコメア構造や融合能を有する機能的な骨格筋細胞であることがわかりました。従来のMYOD1の合成RNAを単独で導入する手法ではMyHC発現を指標にした分化効率が6%であったことから、今回の手法は、機能的な骨格筋細胞の生産性の効率を大きく向上させたということができます(図2)。
なお、さらに網羅的な遺伝子発現解析を行った結果、POU5F1の抑制は骨格筋細胞分化に必須な成長因子の発現を促していることを発見しました。このことから、POU5F1の抑制は多能性幹細胞の未分化性を解除するだけでなく、多元的に分化誘導をサポートすることが示唆されました。
【図2】
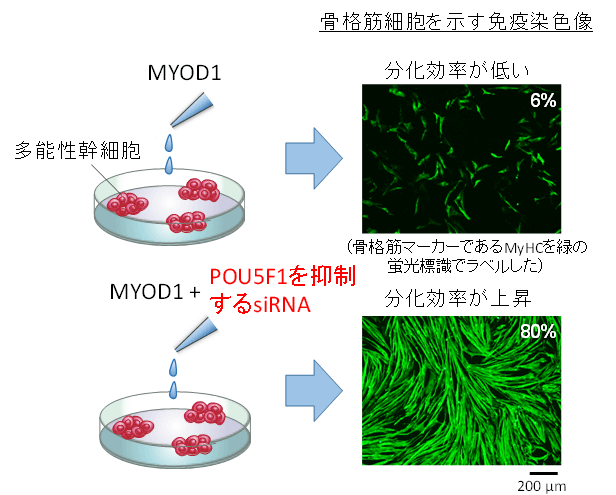
図2.MYOD1の合成RNAを添加しても多能性幹細胞から骨格筋細胞はほとんどできないが、POU5F1を抑制する低分子二本鎖RNA(siRNA)と、MYOD1を同時に添加すると分化効率が上昇する。MYOD1MYOD1 +分化効率が低い分化効率が上昇多能性幹細胞POU5F1を抑制するsiRNA200 μm骨格筋細胞を示す免疫染色像6%80%(骨格筋マーカーであるMyHCを緑の蛍光標識でラベルした)
研究の成果と意義・今後の展開
今回の研究では、①多能性幹細胞を、転写因子MYOD1の合成RNA導入により分化誘導させる際、POU5F1が骨格筋分化を妨げていることの発見、②POU5F1を抑制するsiRNAを加えることにより多能性幹細胞を短期間・高効率に骨格筋細胞へ分化させる「細胞分化RNAカクテル」開発の成功、③POU5F1の抑制が骨格筋細胞分化に必須な成長因子の発現を促進していることの発見という成果を得られました。
「細胞分化RNAカクテル」を用いて、骨格筋細胞へと分化誘導した場合、複数の多能性幹細胞株で効率よく、短期間で骨格筋細胞を得ることができます。今回の結果は、骨格筋細胞の基礎研究のみならず、骨格筋の異常で起こるさまざまな病気の病態解明、治療薬の開発などに役立つことが期待されます。
特記事項
論文
- タイトル:
- Efficient differentiation of human pluripotent stem cells into skeletal muscle cells by combining RNA-based MYOD1-expression and POU5F1-silencing
- 日本語訳:
- RNAを介するMYOD1の発現およびPOU5F1の抑制によるヒト多能性幹細胞から骨格筋細胞への効率のよい分化誘導
- 著者名:
- 秋山 智彦、佐藤 紗恵子、近澤-納富 奈々、相馬 淳美、木村 寛美、若林 俊一、洪 繁、洪 実
- 掲載誌:
- Scientific Reports
用語解説
- (注1)ヒト多能性幹細胞:
- 発生初期の細胞のように、体を構成するさまざまな細胞に分化する能力を持つ培養細胞で、胚盤胞に由来する胚性幹細胞(ES細胞)と体細胞に 由来する人工多能性幹細胞(iPS細胞)がある。
- (注2)転写因子:
- DNAに結合するタンパク質で特定の遺伝子発現レベルを調節する。
- (注3)合成RNA:
- 遺伝子DNAを型枠に見立てて、試験管の中で合成される。細胞の中に導入されると自然に存在するmRNAと同じように、タンパク質の合成が行われる。
本発表資料のお問い合わせ先
坂口光洋記念講座(システム医学教室)
教授 洪 実(こう みのる)
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構
(AMED)戦略推進部 再生医療研究課
関連リンク