アルツハイマー病の治療への応用の可能性も
2020-03-19 京都大学
片平正人 エネルギー理工学研究所教授、真嶋司 同助教らの研究グループは、岐阜大学らと共同で、プリオン病に繋がる蛋白質の構造変化を抑制するRNA分子(RNAアプタマー)の開発に成功しました。
狂牛病やヒトのクロイツフェルトヤコブ病等のプリオン病は、プリオン蛋白質が正常型(PrPC)から異常型(PrPSC)へ構造変化する事で生じます。開発したRNAアプタマーは、プリオン蛋白質の正常型に強く結合して異常型への変化を抑制します。ある種の抗体を除けば、これまでに知られている物質の中で最も高い抑制能を有します。
本研究では、このRNAアプタマーの立体構造を、核磁気共鳴(NMR)法によって決定しました。得られた特異な構造から、高い結合能ひいては高い抑制能を示すメカニズムがわかりました。
プリオン蛋白質はアルツハイマー病に関連するアミロイドβ蛋白質の受容体として、病因性シグナルの伝達にも関与しています。従って本RNAアプタマーは、プリオン病及びアルツハイマー病治療薬として応用できる可能性があります。
本研究成果は、2020年3月18日に、国際学術誌「Scientific Reports」のオンライン版に掲載されました。

図:本研究のイメージ図
書誌情報
【DOI】 https://doi.org/10.1038/s41598-020-61966-4
【KURENAIアクセスURL】 http://hdl.handle.net/2433/246239
Tsukasa Mashima, Joon-Hwa Lee, Yuji O. Kamatari, Tomohiko Hayashi, Takashi Nagata, Fumiko Nishikawa, Satoshi Nishikawa, Masahiro Kinoshita, Kazuo Kuwata & Masato Katahira (2020). Development and structural determination of an anti-PrPC aptamer that blocks pathological conformational conversion of prion protein. Scientific Reports, 10:4934.
詳しい研究内容について
狂牛病を引き起こすプリオン蛋白質の異常化を抑制する RNA 分子の開発
―アルツハイマー病の治療への応用の可能性も―
概要
京都大学エネルギー理工学研究所 片平正人 教授、真嶋司 同助教らの研究グループは、岐阜大学等と共同で、プリオン病に繋がる蛋白質の構造変化を抑制する RNA 分子(RNA アプタマー)の開発に成功しました。
狂牛病やヒトのクロイツフェルトヤコブ病等のプリオン病は、プリオン蛋白質が正常型 (PrPC)から異常型 (PrPSC)へ構造変化する事で生じます。開発した RNA アプタマーは、プリオン蛋白質の正常型に強く結合して異常型への変化を抑制します。ある種の抗体を除けば、これまでに知られている物質の中で最も高い抑制能を有します。
本研究では、この RNA アプタマーの立体構造を、核磁気共鳴(NMR)法によって決定しました。得られた特異な構造から、高い結合能ひいては高い抑制能を示すメカニズムが分かりました。
プリオン蛋白質はアルツハイマー病に関連するアミロイドβ蛋白質の受容体として、病因性シグナルの伝達にも関与しています。従って本 RNA アプタマーは、プリオン病及びアルツハイマー病治療薬として応用できる可能性があります。
本成果は、2020 年 3 月 18 日に国際学術誌「Scientific Reports」のオンライン版に掲載されました。

1.背景
プリオン病は重篤な神経変性障害で、この一種である海綿状脳症(通称狂牛病)に罹ったウシがふらふらとして立っていられずに倒れてしまう映像を見た方もおられると思います。ヒトにおいてもウシと似たような症状がでるクロイツフェルトヤコブ病というプリオン病があります。プリオン病は、哺乳類が有するプリオン蛋白質が正常型から異常型へ構造変化する事で生じます。そこでプリオン病の治療薬を開発する為に、この構造変化を抑制する効果がある物質(低分子化合物、抗体、ナノボディ、アプタマー)を見出す研究が為されてきました。
2.研究手法・成果
本研究グループは今回、正常型のプリオン蛋白質に強く結合する RNA 分子(RNA アプタマー)を探索・デザイン・取得しました。得られた RNA アプタマーは正常型に強く結合してこれを安定化する事で、異常型への構造変化を抑制する事が期待できます。そこでまずこの RNA アプタマーの抗プリオン効果を、細胞実験によって検証しました。次に RNA アプタマーの立体構造を決定する事で、高い結合能ひいては高い抗プリオン効果を発揮するメカニズムを解明しました。
プリオン蛋白質に強く結合する RNA アプタマーを探索・デザインした結果、24 残基及び 25 残基からなる以下の二つの RNA アプタマーを得ました。R24: r(GGAGGAGGAGGAGGAGGAGGAGGA)及び R12-A-R12: r(GGAGGAGGAGGAAGGAGGAGGAGGA)。
異常型のプリオン蛋白質を定常的に産生する細胞に上記の RNA アプタマーを添加したところ、異常型プリオン蛋白質の生成量が劇的に抑制されました。即ちこれらの RNA アプタマーが高い抗プリオン活性を有する事が、細胞レベルの実験で証明されました。抑制活性の強さの指標である IC50(50%阻害濃度 異常型プリオン蛋白質の生成量を半分まで抑制するのに必要な RNA アプタマーの濃度)の値は 100 nM (ナノモーラー 1 リットルあたり 10 億分の 1 モルの濃度を表す)でした。これはある種の抗体を除けば、これまでに知られている抗プリオン物質の中で最も低い値であり、即ち非常に高い抑制活性を有する事が分かりました。
次に RNA アプタマーの立体構造を、核磁気共鳴(NMR)法によって決定しました。分子内に形成された二つの 4 重鎖が積み重なった特異な構造である事が分かりました。得られた立体構造に基づいたモデルビルディングの結果、積み重なった 4 重鎖の両端がプリオン蛋白質中の 2 箇所と同時に結合する事で、プリオン蛋白質へ
の高い結合能、ひいては高い抗プリオン活性がもたらされている事が合理的に説明されました(図 1)。
3.波及効果、今後の予定
本 RNA アプタマーが、異常型プリオン蛋白質の生成を抑制する高い活性を有する事が細胞実験で示されましたので、この分子をベースとした抗プリオン病治療薬の開発が期待されます(図 2)。
プリオン蛋白質は、アルツハイマー病に関連するアミロイドβ蛋白質の受容体として、病因性シグナルの神経細胞内への伝達に関与しています(図 2)。RNA アプタマーはプリオン蛋白質に強く結合する事でプリオン蛋白質の受容体能を不活性化し、病因性シグナルの神経細胞内への伝達をブロックできる可能性があります。従って本 RNA アプタマーは、アルツハイマー病治療薬への応用も期待されます(図 2)。
4.研究プロジェクトについて
本研究は、文部科学省科学研究費補助金 18H04550 及び 18K19397)の支援を受けて行われました。
<研究者のコメント>
探索・デザインした RNA アプタマーが非常に高い抗プリオン活性を有する事を細胞実験で確認できた時には、とてもうれしく思いました。また、立体構造決定によって高い活性が発現されるメカニズムが分かった時には、すっきりとした気分になりました。この分子をベースとした治療薬が今後開発される事を大いに期待しています。
<論文タイトルと著者>
タイトル: Development and structural determination of an anti-PrPC aptamer that blocks pathological conformational conversion of prion protein (病気に繋がるプリオン蛋白質の構造変化を抑制する抗プ リオン RNA アプタマーの開発と構造決定)
著 者 :Tsukasa Mashima, Joon-Hwa Lee, Yuji O. Kamatari, Tomohiko Hayashi, Takashi Nagata, Fumiko Nishikawa, Satoshi Nishikawa, Masahiro Kinoshita, Kazuo Kuwata, and Masato Katahira
掲 載 誌: Scientific Reports DOI 10.1038/s41598-020-61966-4
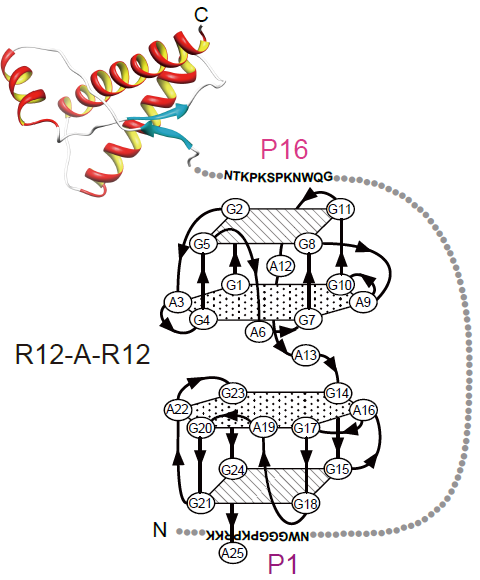
図1 NMR 法によって決定された RNA アプタマー(R12-A-R12)とプリオン蛋白質の結合様式.RNA アプタマーは、分子内に形成された二つの 4 重鎖が積み重なった特異な立体構造を形成する事が分かりまし た. 積み重なった4重鎖の両端がプリオン蛋白質のN 端側のディスオーダー領域中の 2 箇所(P1 と P16)と 同時に結合する事で、プリオン蛋白質への高い結合 能、ひいては高い異常化抑制活性がもたらされる事が 分かりました.
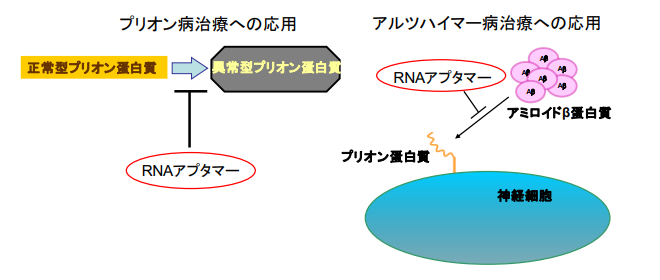
図 2 RNA アプタマーのプリオン病及びアルツハイマー病の治療への応用. (左)RNA アプタマーが正常型プリオン蛋白質に強く結合してこれを安定化し、異常型プリオン蛋白質の生成を抑制する事による抗プリオン病活性. (右)RNA アプタマーが神経細胞表面上のプリオン蛋白質に強く結合する事で、アミロイド β 蛋白質がプリオン蛋白質に結合する事を阻害する。これによりアミロイドβ蛋白質の病因性シグナルが、プリオン蛋白質の受容体能を介して細胞内へ伝達されるのをブロックする事による抗アルツハイマー病活性.