2020-07-16 熊本大学,日本医療研究開発機構
ポイント
- 老化細胞において酵素「NSD2※1」の量が著しく減少すること、また、正常な細胞でNSD2を阻害すると速やかに老化することから、NSD2が細胞老化を防ぐ役割を持つ酵素であることが分かりました。
- 老化細胞でNSD2が減少することにより、細胞増殖に関わる遺伝子群の発現が低下した結果、細胞増殖が持続的に停止することが分かりました。
- 細胞老化が促進されるメカニズムを明らかにしたことから、老化のしくみの解明および制御法の開発、発生過程の病態解明につながることが期待されます。
概要説明
熊本大学発生医学研究所細胞医学分野の中尾光善教授、田中宏研究員、井形朋香研究員(日本学術振興会特別研究員 令和2年3月まで)らは、網羅的な遺伝子解析を用いて、細胞老化をブロックする酵素「NSD2」とその働きを初めて解明しました。NSD2は細胞増殖や数多くの遺伝子の働きを調節する酵素です。今回、老化細胞においてNSD2の量が著しく減少すること、また、正常な細胞でNSD2の働きを阻害すると細胞が速やかに老化することが分かりました。さらに、細胞増殖の過程でNSD2の量が増加して、増殖を促進する遺伝子群の働きを活発化する役割をもつことも解明しました。
この成果は、NSD2が減少することで細胞老化が促進されるメカニズムを明らかにしたことから、老化のしくみの解明および制御法の開発、発生過程の病態解明につながることが期待されます。
本研究成果は、文部科学省科学研究費補助金、日本医療研究開発機構(AMED)革新的先端研究開発支援事業、内藤記念振興財団研究助成、武田科学振興財団研究助成などの支援を受けて、老化分野の科学雑誌「Aging Cell」オンライン版に英国(GMT)時間の令和2年6月22日(日本時間の6月23日)に掲載されました。
研究の内容及び成果
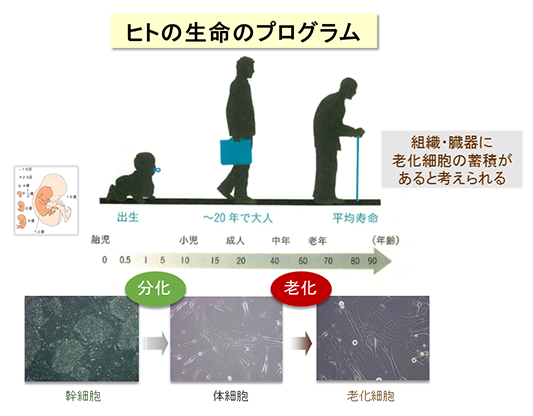
我が国の高齢化は、世界に類を見ないスピードで進展し、今後も高齢化と平均寿命の延長が予測される中、“健康を維持しながら老いる”ことが重要になっています。身体を構成する多くの細胞は、分裂を繰り返して増えると、やがてその機能が低下して増殖を停止します。これを「細胞老化」と呼んで、健康と寿命に関わる重要な要素と考えられています(図1)。細胞老化は、放射線や紫外線などの物理的なストレス、薬剤などの化学的なストレスによってゲノムDNAが損傷を受けると促進されることが知られていますが、老化のメカニズムはまだよく分かっていません。細胞老化には良い点も悪い点もあります。細胞ががん化を始めると、細胞老化が生じてがんの発生を防ぐ役割をしています。他方、細胞老化によって多くの病気が起こりやすくなります。したがって、細胞老化は適切に制御されることが重要です。
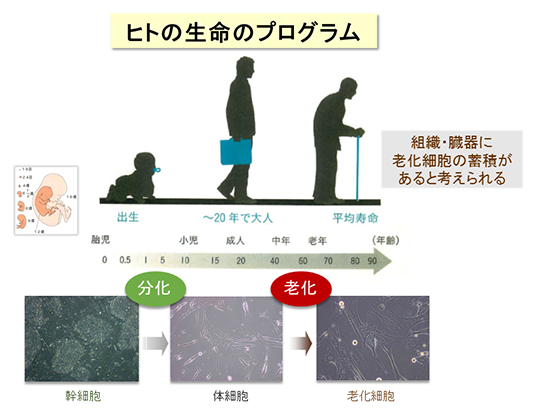
図1 ヒトの生命のプログラム
私たちの身体及び構成する細胞は老化のプログラムをもつ。
老化細胞自身は増殖能を失いますが、近年、老化細胞がさまざまなタンパク質を分泌して周囲の細胞に働きかけて、慢性的な炎症やがん細胞の増殖をかえって促進することに注目されています。予想される以上に、老化細胞はアクティブに働いていますので、細胞老化は、身体全体の老化の原因になると考えられるようになりました。例えば、老齢マウスの体内には老化細胞が蓄積していきますが、これらを除去すると全身の老化が抑えられるという報告があります。つまり、細胞老化を制御できれば、全身の老化の進度を調節できる可能性があります。
本研究グループは、「エピジェネティクス」とよばれる学問の観点から、細胞老化のメカニズムについて研究を進めています。エピジェネティクスは、すべての遺伝子の働き方(ON/OFF)を明らかにする研究分野であり、生命現象や病気の発症、さらに老化にも密接に関わると考えられます。ヒトの設計図に当たるゲノムには、約2万5千個の遺伝子があります。現在までに、我々はヒト線維芽細胞(すべての組織・器官に存在する細胞種)の老化に関わる因子を幅広くスクリーニングして、複数の因子を同定しました。
正常な細胞は、数多く分裂して複製した後に増殖を停止します(複製後の老化)。また、がん遺伝子が活性化してがん化が始まると、それを阻止するために老化がおこります(がん遺伝子で誘導される老化)。本研究グループは、これまでに老化細胞ではミトコンドリアの代謝機能が著しく上昇していること、「SETD8メチル基転移酵素」が細胞老化を防ぐ酵素であることを報告しており、今回の研究では、「NSD2メチル基転移酵素」が細胞老化を防ぐ役割をもつことを発見しました。これまで、NSD2は遺伝子の働きを調節することが報告されており、とりわけ、ゲノムDNAに巻き付くヒストンタンパク質をメチル化して、その近傍の遺伝子の働きを高めると考えられています。しかし、細胞老化との関連性は知られていませんでした。そこで、線維芽細胞において、NSD2の遺伝子の働きを抑えるノックダウン(RNA干渉法)を行ったところ、細胞老化が誘導されて、老化細胞の典型的な特徴が現れたことから、NSD2は細胞老化を防ぐ役割をもつことが分かりました(図2)。
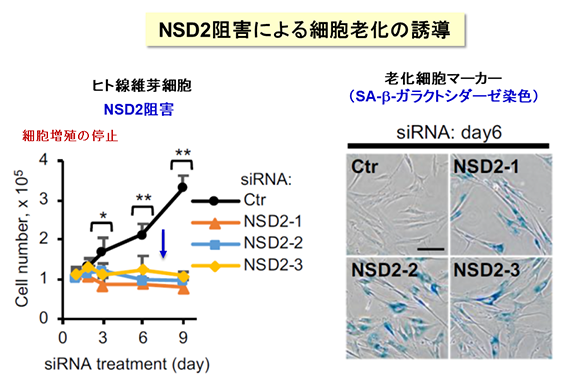
図2 NSD2阻害による細胞老化の誘導
NSD2酵素は細胞老化を防ぐ働きをしている。
次に、NSD2が減少した老化細胞を詳しく調べるために、最新のシークエンサー※2を用いて、すべての遺伝子発現を網羅的に解析しました。その結果、細胞老化に関わる遺伝子群の発現が増加するとともに、とりわけ、細胞増殖を促進するタンパク質の遺伝子群の働きが低下していました。これらの遺伝子群に位置するヒストンは、増殖中の細胞ではNSD2によってメチル化を受けていますが、NSD2が減少した老化細胞ではメチル化が低下していました。つまり、NSD2の減少によって、細胞増殖に関わる遺伝子群の働きが不活性化して、増殖が停止することが示されました。
さらに、血清応答実験により、どのようにNSD2の働きが調節されているのかを検討しました。通常、細胞は血中(正確には血清中)の増殖因子(増殖を促進するタンパク質)が作用することで増殖を行います。一方で老化細胞は増殖を不可逆的に停止ししており再び増えることはないと予想されます。血清飢餓で前培養した細胞は増殖を停止し、血清を添加すると速やかに増殖を再開します。実験の結果、血清を添加するとNSD2の量が速やかに増加すること、そして、増殖促進の遺伝子の発現と細胞増殖にNSD2が必要であることが分かりました。さらに、NSD2が低下した老化細胞では血清による増殖能を完全に欠いていることが分かりました。つまり、NSD2は細胞増殖と血清応答を維持することで、細胞老化を防ぐと考えられます(図3)。
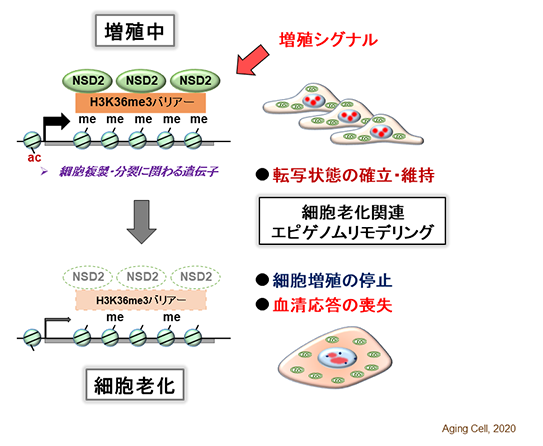
図3 NSD2は細胞老化のプログラムを形成するNSD2によるヒストンのメチル化(H3K36me3バリアー)が細胞増殖に関わる遺伝子の働きを促進している。老化細胞では、NSD2が低下するため、エピゲノムと遺伝子発現の変化がおこり、細胞増殖と血清応答は失われる。
今回の研究成果は、本研究グループが同定した4つ目の細胞老化の防御因子になります。NSD2が細胞老化を防御するという発見を契機として、老化の基本メカニズムを明らかにしたものであり、老化のしくみ解明および酵素の活性を調節した制御法の開発に役立つと期待できます。
用語解説
- ※1:NSD2
- 標的のタンパク質にメチル基(CH3)を付けることで、遺伝子の働きを調節する酵素。とりわけゲノムDNAを取り巻くヒストンタンパク質をメチル化して、近傍遺伝子の働きを活性化する。遺伝子機能のON/OFFを化学修飾によって後天的に調節する仕組み「エピゲノム」の修飾酵素のひとつ。「ウォルフ・ヒルシュホーン(Wolf-Hirschhorn)症候群」とよばれる成長障害・精神遅滞などをもつ先天性の発生異常症の原因遺伝子としても知られる。
- ※2:シークエンサー
- DNAなどの塩基配列を解析するための装置。
論文情報
- 論文名
- The NSD2/WHSC1/MMSET methyltransferase prevents cellular senescence-associated epigenomic remodeling
(NSD2/WHSC1/MMSETメチル基転移酵素は、細胞老化に関わるエピゲノムリモデリングを防御している) - 著者名(*責任著者)
- Hiroshi Tanaka, Tomoka Igata, Kan Etoh, Tomoaki Koga, Shin-ichiro Takebayashi, and Mitsuyoshi Nakao*
- 掲載雑誌
- Aging Cell
- URL
- https://onlinelibrary.wiley.com/doi/full/10.1111/acel.13173
- DOI
- 10.1111/acel.13173
お問い合わせ先
内容に関するお問い合わせ
熊本大学発生医学研究所 細胞医学分野
担当:教授 中尾光善(なかおみつよし)
AMEDの事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構
シーズ開発・研究基盤事業部 革新的先端研究開発課