2021-02-26 東京大学,千葉大学,日本医療研究開発機構
発表者
藤生克仁(東京大学医学部附属病院 循環器内科/東京大学大学院医学系研究科 先進循環器病学 特任准教授)
小室一成(東京大学医学部附属病院 循環器内科/東京大学大学院医学系研究科 循環器内科学 教授)
真鍋一郎(千葉大学大学院医学研究院 長寿医学 教授)
発表のポイント
- 心臓が正常に脈を刻み続けるために必要な新しい仕組みを発見しました。
- 心臓突然死しないように心臓の免疫細胞が分泌するタンパク質が常に心臓を保護していることを見出しました。
- 本成果は心臓突然死を生じる不整脈の新しい診断・治療・予防法の開発に貢献すると考えられます。
発表概要
心臓が血液を送り出すポンプとして正常に動き続けるためには、心臓を構成する多数の心筋細胞が同期して、正しいリズムで収縮することが必要です。
心臓へのストレスやさまざまな心臓病によって、この同期が保てなくなり、心臓が正常の動きでなくなるために、心臓のリズムが狂ってしまう不整脈が出現し突然死につながることが知られています。
しかし、そもそも、どのように心筋細胞どうしの収縮の同期が維持され、正常な心臓の動きが維持されているのかについては、よく分かっていませんでした。
東京大学医学部附属病院の藤生克仁特任准教授、小室一成教授、および千葉大学大学院医学研究院の真鍋一郎教授らの研究グループは、心臓に存在している免疫細胞に注目して、この細胞が分泌するタンパク質が、心筋細胞どうしの小さな穴を通したつながりに必要であることを世界で初めて発見しました。この免疫細胞や、免疫細胞が分泌するタンパク質をなくしたマウスでは、心筋細胞どうしの同期が失われ、さまざまな不整脈が出現し、わずかなストレスで高率に心臓突然死を起こしました。
心臓が正常に働くために必要な新しい仕組みが分かったことで、今後、不整脈や心臓突然死の新しい診断・治療・予防へつながることが期待されます。
本研究成果は、日本時間2021年3月26日に英国科学誌Nature Communications(オンライン版)に掲載されます。
発表内容
心臓突然死は、心疾患患者の主な死因であり、社会的損失の大きい疾患です。米国では毎年40万人以上、日本では6~8万人が心臓突然死で亡くなっており、今後高齢者人口が増えるとともにさらに増加することが予想されます。
心臓突然死は、重症な不整脈が続くことで生じますが、全く前兆なく急に不整脈が出現して、残念ながら突然死してしまうことがあります。また、不整脈が起こる可能性が高いことが分かっている心臓病の患者さんであっても、心臓の不整脈の起源となる部分をカテーテルで焼灼・冷凍するカテーテル治療、不整脈が出現した際に電気ショックでもとに戻す植込み型除細動器治療がありますが、いずれも患部の除去療法・対症療法であり、根本的な原因への治療ではありません。その原因として、未だ、どのように心臓の正常な動きが作られるか?について不明な点が多いことが挙げられます。
心臓突然死の研究は、心臓の主なポンプである左心室を中心に展開されてきましたが、最近、右心室の機能が低下していると突然死が増えるという臨床報告があったことから、本研究グループは、右心室に着目しました。
まず、マウスの右心室に圧力ストレスを与えて観察したところ、多種の免疫細胞が増加していることを見出しました。それぞれの免疫細胞を一種類ずつ無くしたマウスを用いて、同様に右心室へのストレスを与えたところ、免疫細胞の一つであるマクロファージ(注1)を無くしたマウスだけが重症な不整脈を生じ、短時間で突然死することを見出しました。このことは、心臓の中のマクロファージ(心臓マクロファージ)が突然死を予防していることを意味しています。
次に、心臓マクロファージはどのように不整脈を予防しているのかを検討しました。心臓は多数の心筋細胞から構成されます。心筋細胞は1個の心筋細胞でも収縮することができますが、心臓全体が血液を送り出すポンプとして働くためには、一つの心筋細胞が収縮したあとに、その隣の心筋細胞がすぐに収縮することが必要です。このように心筋細胞どうしが同期して収縮することで、心臓の正常な動きが作られます。
この心筋細胞の収縮の同期は、心筋細胞と心筋細胞がギャップジャンクション(注2)と呼ばれる小さな穴を通じてつながっていることが必要であるということが知られていました。今回、研究グループは、心臓マクロファージが、このギャップジャンクションを正常に作るために必要であることを発見しました(図1)。
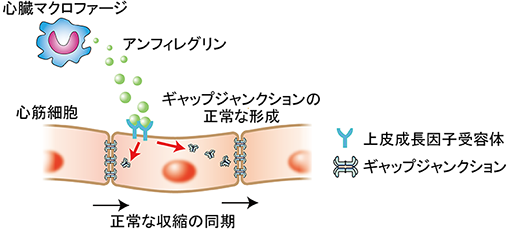
図1 心臓マクロファージが分泌するアンフィレグリンが心臓突然死を防いでいる心筋細胞と心筋細胞のすきまに存在する免疫細胞において、心臓特有の新しい働きを探索するなかで、アンフィレグリンが突然死を予防する働きがあることを発見した。
さらに、心臓マクロファージは心筋細胞に比べると圧倒的に数が少なく、心筋細胞100個に対して、心臓マクロファージは1個程度しか存在しません。そこで、心臓マクロファージが多数の心筋細胞をコントロールする仕組みとして、心臓マクロファージが分泌するタンパク質を探索しました。その結果、アンフィレグリン(注3)と呼ばれるタンパク質が、心筋細胞に存在する上皮成長因子受容体(注4)を介して、ギャップジャンクションの形成に必要であることを発見しました。
アンフィレグリンを心臓マクロファージから無くしたマウスは、ギャップジャンクションが正常に形成されず、さまざまな種類の不整脈が出現し、さらに心臓へのストレスを加えると、心室頻拍・心室細動と呼ばれる重症な不整脈が出現し、高率に突然死が生じました。
この心筋細胞どうしの同期性を増加させることで、正常な心臓の動きを保ち、不整脈が起こらないようにしている心臓マクロファージの機能は、右心室だけでなく全ての心臓の部位で働いていることも分かりました(図1)。
本研究により、正常に心臓が動くメカニズムに、心臓マクロファージが分泌するアンフィレグリンの作用機序が加わったことで、現在未解決となっている心臓突然死の診断・治療・予防法の確立へ大きく貢献することが期待されます。
なお本研究は、日本医療研究開発機構(AMED)の革新的先端研究開発支援事業ソロタイプ(PRIME)「全ライフコースを対象とした個体の機能低下機構の解明」研究開発領域における研究開発課題「組織マクロファージの変遷による個体の機能低下機構の解明」(研究開発代表者:藤生克仁)ならびに革新的先端研究開発支援事業ユニットタイプ(AMED-CREST)「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域における研究開発課題「心筋メカノバイオロジー機構の解明による心不全治療法の開発」(研究開発代表者:小室一成)、ゲノム医療実現推進プラットフォーム事業「マルチオミックス連関による循環器疾患における次世代型精密医療の実現」(研究代表者:小室一成)、難治性疾患実用化研究事業希少難治性疾患の克服に結びつく病態解明研究における研究課題「ゲノム分子病理解析による難治性心筋症における精密医療の実現」(研究代表者:小室一成)、老化メカニズムの解明・制御プロジェクト個体・臓器老化研究拠点(研究開発分担者:真鍋一郎)、日本学術振興会科学研究費助成事業基盤研究B「臓器間連携を介したストレスメモリ―による循環器疾患発症機序の解明」(研究代表者:藤生克仁)、日本学術振興会科学研究費助成事業挑戦的研究(萌芽)「組織免疫細胞の機能不全による新規心疾患発症機序の解明と治療法の開発」(研究代表者:藤生克仁)、日本学術振興会科学研究費助成事業基盤研究B「メカノエイジングによる心不全発症機序解明と治療法開発」(研究代表者:真鍋一郎)、新学術領域研究(研究領域提案型)複合領域「心臓恒常性とリモデリングを制御する炎症細胞社会の相互作用ネットワーク解明」(研究代表者:真鍋一郎)等の支援により行われました。
発表雑誌
- 雑誌名
- Nature Communications(オンライン版:2021年3月26日)
- 論文タイトル
- Cardiac Macrophages Prevent Sudden Death During Heart Stress
- 著者
- Junichi Sugita, Katsuhito Fujiu*, Yukiteru Nakayama, Takumi James Matsubara, Jun Matsuda1, Tsukasa Oshima, Yuxiang Liu, Yujin Maru, Eriko Hasumi, Toshiya Kojima1, Hiroshi Seno, Keisuke Asano, Ayumu Ishijima, Naoki Tomii, Masatoshi Yamazaki, Fujimi Kudo, Ichiro Sakuma, Ryozo Nagai, Ichiro Manabe*, Issei Komuro (*責任著者)
- DOI番号
- 10.1038/s41467-021-22178-0
用語解説
- (注1)マクロファージ
- 免疫細胞の一種。死細胞や細菌などの異物を食べて除去する細胞。
- (注2)ギャップジャンクション
- 心筋細胞と心筋細胞をつなぐタンパク質で、その中央に穴が開いており、心筋細胞と心筋細胞の細胞の中をつないでいる。この穴によって、心筋細胞の収縮が隣の心筋細胞に伝達される。
- (注3)アンフィレグリン
- 心臓の中では、マクロファージが常時発現しているタンパク質。心臓へのストレスなどで増加する。
- (注4)上皮成長因子受容体
- 心筋細胞の表面に存在し、アンフィレグリンが結合することができ、結合した場合、心筋細胞内にそのシグナルを伝える。
お問い合わせ先
研究内容に関するお問い合わせ先
東京大学医学部附属病院 循環器内科
特任准教授 藤生克仁(ふじうかつひと)
千葉大学大学院医学研究院 長寿医学
教授 真鍋一郎(まなべいちろう)
取材に関するお問い合わせ先
東京大学医学部附属病院 パブリック・リレーションセンター
担当:渡部、小岩井
千葉大学 広報室
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
シーズ開発・研究基盤事業部 革新的先端研究開発課