2021-05-24 東京大学,日本医療研究開発機構
発表のポイント
- 脳腫瘍で高頻度にみられる神経膠腫(グリオーマ)のうち、最も悪性度の高い膠芽腫を、手術中に「色をつける」ことで識別しやすくする、世界初の局所投与型蛍光プローブ(注1)を開発しました。
- 今回開発した蛍光プローブはわずか数分で蛍光を発します。また繰り返し投与が可能であることが特徴です。既存の術中蛍光プローブの主な問題点であった術前経口内服が必要な点と、手術が長時間になると有効性が低下する点を克服しました。
- 日本発のこの技術が、難治な脳腫瘍である神経膠腫の手術戦略の革新的な一手となり、手術摘出度の向上と治療成績の改善をもたらすことが期待されます。
発表概要
東京大学大学院医学系研究科脳神経外科学の田中將太講師、北川陽介大学院生(研究当時)、齊藤延人教授および同大学院薬学系研究科薬品代謝化学・医学系研究科生体情報学の浦野泰照教授らの研究グループは、腫瘍細胞における酵素活性を利用する仕組みを応用することで手術中に脳腫瘍を蛍光標識できる(蛍光を発することで識別しやすくする)、局所投与型の蛍光プローブを開発しました。
脳腫瘍で最も多く見られる神経膠腫の治療では、手術によって腫瘍を摘出する際の取り残しをできる限り無くすことが極めて重要ですが、染み込むように発育する腫瘍のため肉眼では非腫瘍部分との判別が難しく、脳を闇雲に大きく取り除くこともできません。患者さんの術後の状態を悪くせずに腫瘍を最大限摘出するために、術中に蛍光プローブによる腫瘍の可視化することが有効です。現在、5-アミノレブリン酸(5-ALA)が唯一保険収載されている薬剤として使用されていますが、蛍光を示すまでに時間がかかるため術前内服が必要であり、手術終盤で蛍光が弱まりがちであるといった難点があります。そこで、開発済みであったHydroxymethyl Rhodamine Green(HMRG)を蛍光母核(注2)とした300種類以上のアミノペプチダーゼ型蛍光プローブライブラリーを用いて、がん部位イメージング法を応用した新しい蛍光プローブPR-HMRGを開発しました(国際特許出願済)。手術中いつでもその場で腫瘍に「色をつける」ことが可能となり、肉眼では判別困難な腫瘍を容易に認識できるため摘出度が向上し、神経膠腫治療の成績が改善することが期待されます。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)「橋渡し研究戦略的推進プログラム」(東京大学拠点、シーズA)「革新的がん医療実用化研究事業」、および文部科学省科学研究費助成事業「若手研究(B)」「基盤研究(C)」(15K19952、20K09365)の支援により行われ、日本時間2021年5月24日に「Clinical Cancer Research, a journal of the American Association for Cancer Research」に掲載されました。
発表内容
研究背景
神経膠腫は最もよく見られる原発性脳腫瘍で(25%を占める)、世界保健機構(World Health Organization, WHO)によりその悪性度はグレードIからIVに分類されます。最も悪性度の高いグレードIVの神経膠腫は膠芽腫と呼ばれ、5年生存率は10%未満と非常に予後(注3)が不良な脳腫瘍です。予後を決める因子として年齢やいくつかの遺伝子異常の他に、手術による摘出度が知られています。ただし、脳には運動や言語など重要な機能を司る部分があるため、腫瘍を取りきるためとは言え重要な脳の部分を含めて広範囲に摘出することはできません。したがって神経膠腫の手術では、患者さんの術後の状態を悪くしない範囲で最大限に腫瘍を摘出することが重要で、そのために様々な手術支援技術が開発され使用されています。蛍光により腫瘍を識別する蛍光プローブはその一つで、脳に浸潤しながら発育する神経膠腫は肉眼的には正常脳組織との判別が困難であるため、腫瘍摘出に際して蛍光標識は非常に有効です。
5-アミノレブリン酸(5-aminolevulinic acid, 5-ALA)は正常細胞内にも存在するアミノ酸の一種で、腫瘍細胞に5-ALAの代謝物が蓄積することが分かっており、励起光(注4)が当たるとその代謝物が蛍光を発するため、腫瘍が標識されます。日本で光線力学診断用剤として承認に至ったドイツにおける大規模臨床試験では、5-ALAを使用した手術の場合、5-ALAを使用しない従来の手術に比べ有意に腫瘍摘出率が高く、6か月間腫瘍の再増大なく経過する患者さんの割合も有意に高まりました。5-ALAは現在国内で悪性神経膠腫を対象に保険収載された唯一の蛍光プローブですが、標識率や投与方法などに課題も抱えています。具体的には、5-ALAは手術開始 3 時間前の内服投与が必要なため手術開始後には再投与できないこと、手術時間が長くなると代謝され手術の最終局面で蛍光が薄れてしまうこと、光への感受性が増強するため患者さんは術後明るい光への露出を控える必要があることなどがあります。
本研究グループにより開発された、Hydroxymethyl rhodamine green(HMRG)という蛍光母核に種々のアミノ酸を付加して作成した(アミノペプチダーゼ型)蛍光プローブは、がん細胞で亢進している酵素活性を特異的に検出することができます。既に計300種類以上が生合成されており、そのプローブライブラリーを活用し、脳腫瘍の術中標識に有用で、5-ALAの課題を克服するような新規蛍光プローブの開発研究を開始しました。
開発内容
蛍光プローブライブラリーを用いて、組織を破砕したライセート(破砕した腫瘍細胞を溶かした液)による一次スクリーニング、手術で得られた新鮮検体による二次スクリーニングを行い、これらのデータを統合的に解析した数理的計算の三次スクリーニングを経て、膠芽腫を標識可能な蛍光プローブとして、プロリン(P)―アルギニン(R)のアミノ酸の組み合わせがHMRGに結合したPR-HMRGを選出しました(図1)。
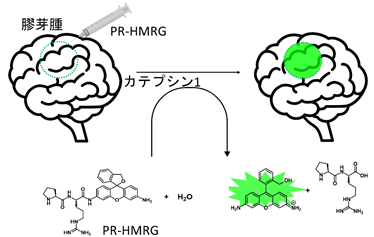
図1. PR-HMRGプローブの使用イメージ手術中にPR-HMRGプローブを噴霧することで腫瘍を蛍光させ、腫瘍摘出しやすくする。
続いてプロテオーム解析(注5)により、この蛍光プローブに酵素反応を引き起こした標的酵素として4つの酵素を選出しました。そして阻害薬実験や精製酵素による実験から、カルパイン1が標的酵素として同定されました。ヒト膠芽腫のライセートを用いたリアルタイムPCRによるRNA発現の検証、病理組織学切片の免疫組織染色等によるタンパク質発現の検証からも、標的酵素はカルパイン1として矛盾しない結果でした。
さらに、ヒトの膠芽腫から樹立された培養細胞U87を用いてPR-HMRGプローブを検証し、培養細胞をマウス脳内に移植した動物実験にて、実際にPR-HMRGプローブが腫瘍をきれいに蛍光標識できることを確認しました(図2)。
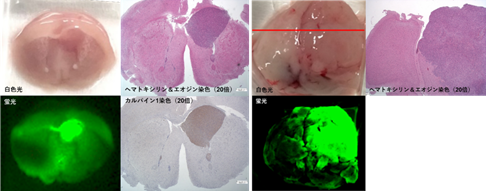
図2. 膠芽腫細胞株を用いたマウスモデルによる検証(蛍光の位置が腫瘍の部位を示す)左:細胞株を移植したマウスの脳腫瘍断面にPR-HMRG(50μM)を投与後の、白色光、蛍光、および病理学的所見.腫瘍部位に一致して強い蛍光がみられ、標的酵素であるカルパイン-1の強い発現がみられた
右:細胞株を移植したマウスの全脳にPR-HMRG(50μM)を投与後の、白色光、蛍光、および赤線での断面における病理学的所見.右大脳半球に腫瘍がみられ、腫瘍部位と一致した強い蛍光がみられた
この蛍光プローブは、局所に直接投与後わずか数分で腫瘍を識別可能という即時性を持ち合わせ、微量投与のため安全で、かつ繰り返し使用可能という利点を有しているため、実際の手術において局所投与で使用可能であろうと考えられました。
社会的意義
本研究では引き続き、PR-HMRGプローブの有効性と安全性を非臨床試験の形で検証中であり、将来的には実際に患者さんに投与する臨床試験を経て、臨床応用を目指しています。この先進的な医用イメージング技術を既存の5-ALAと併用することで、蛍光波長も蛍光メカニズムも異なる二つの蛍光プローブにより腫瘍を特異的に標識し、より精度の高い術中蛍光標識が可能になると考えられます。膠芽腫の手術において腫瘍摘出度が上昇し腫瘍残存が低減することで、患者さんの予後が改善することが期待されます。
脳外科手術で用いられている通常の顕微鏡に特殊なフィルターを装着するだけで、励起光は簡単に用意できます。既に5-ALA用のフィルターは多くの顕微鏡に搭載されているので、臨床応用は比較的容易であると思われます。
今後、PR-HMRGプローブは脳腫瘍手術のブレークスルーになり得ると期待されます。
発表者
田中 將太(東京大学大学院医学系研究科脳神経医学専攻脳神経外科学/東京大学医学部附属病院脳神経外科 講師)
北川 陽介(東京大学大学院医学系研究科脳神経医学専攻脳神経外科学 大学院生:研究当時)
浦野 泰照(東京大学大学院薬学系研究科薬学専攻薬品代謝化学/東京大学大学院医学系研究科生体物理医学専攻生体情報学 教授)
齊藤 延人(東京大学大学院医学系研究科脳神経医学専攻脳神経外科学/東京大学医学部附属病院脳神経外科 教授)
発表雑誌
- 雑誌名
- 「Clinical Cancer Research, a journal of the American Association for Cancer Research」(オンライン版:5月24日)
- 論文タイトル
- A Novel Topical Fluorescent Probe for Detection of Glioblastoma
- 著者
- Yosuke Kitagawa, Shota Tanaka*, Mako Kamiya, Yugo Kuriki, Kyoko Yamamoto, Takenori Shimizu, Takahide Nejo, Taijun Hana, Reiko Matsuura, Tsukasa Koike, Erika Yamazawa, Yoshihiro Kushihara, Satoshi Takahashi, Masashi Nomura, Hirokazu Takami, Shunsaku Takayanagi, Akitake Mukasa, Yasuteru Urano*, and Nobuhito Saito
用語解説
- (注1):蛍光プローブ
- タンパク質・アミノ酸・酵素など特定の分子と反応すると、分子構造が変化することによって強く蛍光を発する、または色調が変化する、機能性分子の総称。
- (注2):蛍光母核
- 蛍光プローブの設計に際して、その中心となる蛍光性を持った物質の総称。
- (注3):予後
- 患者さんの状態や病気に関する将来的な予測や見込みを意味する医学用語。
- (注4):励起光
- 蛍光物質は外部から照射された光のエネルギーを吸収し、それが元に戻るときに蛍光を発する。その蛍光物質に励起を引き起こす光の総称。
- (注5):プロテオーム解析
- Protein(タンパク質)と接尾辞ome(全て)を組み合わせた造語であり、細胞内で発現しているまたは発現する可能性をもつ全タンパク質の相互関係を解析する手法。
お問い合わせ先
研究内容に関するお問い合わせ先
東京大学医学部附属病院 脳神経外科
講師 田中 將太(たなか しょうた)
広報担当者連絡先
東京大学医学部附属病院 パブリック・リレーションセンター
担当:渡部、小岩井
AMEDの事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
ゲノム・データ基盤事業部 医療技術研究開発課
革新的がん医療実用化研究事業