分子疫学研究から見えてきた加熱式タバコによる生体分子の変化
2021-11-04 岩手医科大学,慶應義塾大学医学部,国立がん研究センター
発表のポイント
- 岩手医科大学は、慶應義塾大学医学部および国立がん研究センターとの共同研究において、地域コホート研究の参加者を対象に加熱式タバコがDNAメチル化*1および遺伝子発現パターンへ与える影響を解析しました。
- 火を使い燃焼させる従来型の紙巻きタバコ(従来型タバコ)*2から加熱式タバコへ切り替えた人のDNAメチル化および遺伝子発現パターンは、従来型タバコ喫煙者よりも程度は低いものの、非喫煙者と比べて喫煙に関わるDNAの低メチル化や遺伝子発現の増減が多く見られることが明らかになりました。
- 今回の解析では、先行研究で喫煙との関連が報告されているDNAメチル化部位のみを解析しました。加熱式タバコによるDNAメチル化パターンへの詳細な影響を調べるには、今後はゲノムの網羅的な解析が必要です。
- 本研究で解析した加熱式タバコ使用者は、従来型タバコから使用を切り替えて平均約2年しか経っていない方々でした。加熱式タバコの長期的な影響については本研究では明らかにできていません。今後、長期的な追跡調査を行い、加熱式タバコによる長期的な影響を調べる必要があります。
概要
岩手医科大学いわて東北メディカル・メガバンク機構生体情報解析部門の大桃秀樹 講師、同部門部門長の清水厚志 教授、慶應義塾大学医学部衛生学公衆衛生学教室の武林亨 教授、原田成 専任講師、国立がん研究センターがん対策研究所予防検診政策研究部の片野田耕太 部長らの研究グループは、従来型タバコから加熱式タバコへの切り替え(平均約2年間)により、血液細胞におけるDNAメチル化および遺伝子発現パターンが従来型タバコ喫煙者とは異なるパターンを示すことを明らかにしました。本研究成果は、国際科学雑誌 Cancer Epidemiology, Biomarkers & Prevention誌に2021年11月3日付(オンライン公開)で掲載されました。
https://cebp.aacrjournals.org/content/early/2021/11/01/1055-9965.EPI-21-0444
研究背景
加熱式タバコ製品は、電気的に加熱されたタバコの葉から発生するニコチンや様々な化学物質を含むエアロゾルを吸入する新しいタイプのタバコ製品です(参考文献1,2)。日本たばこ産業株式会社のPloom TECH*、米国Philip Morris International社のIQOS*、英国British American Tobacco社のglo*などの加熱式タバコは、日本を含むいくつかの国で2014年半ばから販売されています。
加熱式タバコの成分分析を行った研究により、加熱式タバコには従来型タバコと同程度のニコチンが含まれていること、従来型タバコよりも低濃度ではあるが発がん性物質が含まれていることが明らかになっていますが、それに伴うタバコ関連疾患の発症リスクはいまだに解明されていません。日本では、2015年以降急速に普及していることから、加熱式タバコの健康リスク評価の基となる疫学研究の成果が早急に求められています。
近年の次世代シーケンサー(NGS)の向上により、ゲノム、DNAメチル化、遺伝子発現などの網羅的な分子プロファイリングを安価かつ迅速に解析できるようになっています(参考文献3)。ゲノム情報は生涯を通じて基本的に変化しませんが、DNAメチル化や遺伝子発現パターンは、生活習慣や環境化学物質への曝露によって変化し、さまざまな疾患の発症に関係することが知られています。中でも、従来型タバコの喫煙によりDNAメチル化や遺伝子発現パターンが変化することは複数の研究で報告されていますが(参考文献4-7)、加熱式タバコによる影響についてはまだほとんど調べられていません。
そこで研究グループは、慶應義塾大学医学部衛生学公衆衛生学教室が中心となって進めている地域コホート研究(鶴岡メタボロームコホート研究)*3の参加者に本研究への参加を呼びかけ、参加に同意いただいた方からご提供いただいた血液検体からDNAやRNAを抽出し、加熱式タバコによるDNAメチル化や遺伝子発現への影響を調べました。
研究成果
鶴岡メタボロームコホート研究の参加者1.1万人を対象に、2018~2019年度に実施したフォローアップ調査(追跡調査)に参加し、同意を得た2,789名から血液に含まれる末梢血単核球を収集しました。2,789名の喫煙習慣の内訳は、加熱式タバコ使用者(加熱式)が53名、非喫煙者が1,657名、過去喫煙者が822名、従来型タバコ喫煙者(従来型)が257名でした。本研究における加熱式タバコ喫煙者とは、2012から2015年度のベースライン調査時には従来型タバコを喫煙していたが、今回のフォローアップ調査までに加熱式タバコへ完全に切り替えた人と定義しました。53名の加熱式タバコ使用者のうち1名は、1日1本の使用と非常に少数の使用だったため、この1名を除外した52名を解析対象の加熱式タバコ使用者としました。性別や年齢、BMI、生活習慣病罹患歴などを元に対象者の特徴を要約するプロペンシティスコア(傾向スコア)を算出し、加熱式タバコ使用者52名に対して非喫煙者、過去喫煙者、従来型喫煙者と傾向スコアでマッチングを行い、それぞれから対象者を選択しました。
加熱式タバコ使用者と他の喫煙習慣にある人との間で、これまでに報告されている喫煙関連DNAメチル化マーカーの17遺伝子29 CpGにおけるDNAメチル化パターンを比較しました(図1)。その結果、AHRR、ALPP2、F2RL3、GNG12、GPR15、LRRN3、MGAT3、MYO1G、PRSS23、RARA、SLAMF4の11遺伝子17CpGのDNAメチル化パターンにおいて、加熱式タバコ使用者と非喫煙者との間に有意な差が認められました(図1A, B, C, D, E, F, I, J, L, M, P, Q, T, V, W, X, Y)。さらに、その11遺伝子17CpGのうちMYO1Gを除く10遺伝子16CpGにおいて、従来型喫煙者よりも程度は低いものの、非喫煙者と比べて加熱式タバコ使用者で低メチル化が起こっていました。一方、加熱式タバコ使用者と従来型喫煙者との間では、AHRR、C14orf43、F2RL3、LRRN3、MGAT3、MYO1G、RARAの7遺伝子14CpG(図1.A, B, C, G, H, I, J, O, Q, R, S, T, W, X)で有意差を示しました。興味深いことに、加熱式タバコ使用者と過去喫煙者との間で有意差を示したのは、PRSS23とSLAMF4の2遺伝子2 CpGのみでした(図1.V, Y)。
続いて、4つの喫煙習慣群間において総当たりで遺伝子発現パターンを比較しました。その結果、95種類の遺伝子において、有意な遺伝子発現を示すことが明らかになりました。その95種類の遺伝子に着目して4つの喫煙習慣における遺伝子発現の特徴を比較するために主成分分析*4を行いました。その結果、従来型喫煙者と非喫煙者の遺伝子発現の特徴は分かれ、その2群間の中間ほどの位置に加熱式使用者と過去喫煙者が示されました(図2)。この結果、遺伝子発現パターンにおいても、加熱式タバコ使用者は、従来型タバコ喫煙者より程度は低いものの、非喫煙者と比べて喫煙に関わる遺伝子発現の増減が多く観察されることが示唆されました。
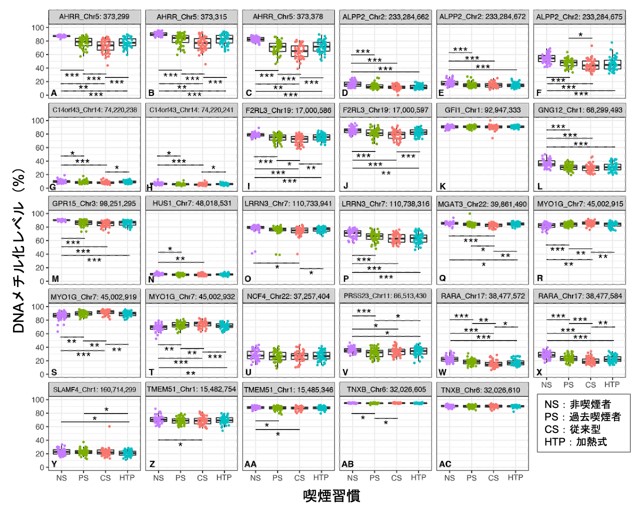
図1.喫煙と関連する17遺伝子29CpGのDNAメチル化マーカーのパターン *** p < 0.001, ** p < 0.01, * p < 0.05
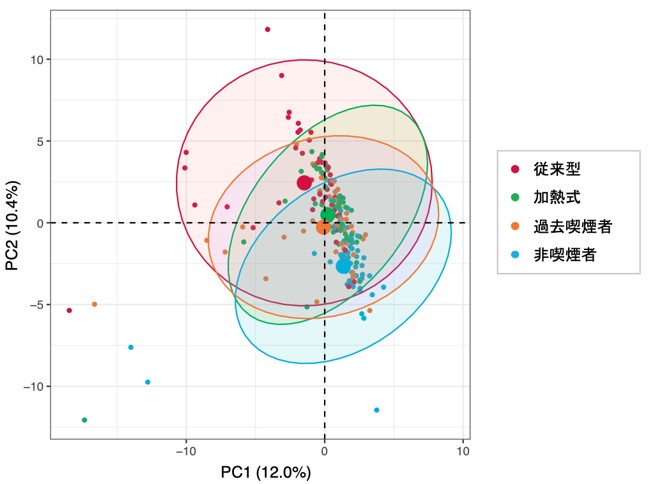
図2.遺伝子発現に有意差を示した95遺伝子に基づく主成分分析(PCA)PC1:第一主成分、PC2:第2主成分
まとめと展望
本研究は、加熱式タバコ使用者における分子遺伝学的影響を調べるため、日本人で構成されたコホート研究において、これまでに喫煙と関連すると報告されている17遺伝子(AHRR, ALPPL2, C14orf48, F2RL3, GFI1, GNG12, GPR15, HUS1, LRRN3, MGAT3, MYO1G, NCF4, PRSS23, RARA, SLAMF7, TMEM51, TNXB)のDNAメチル化マーカーに対するDNAメチル化解析と遺伝子発現解析を行いました。その結果、従来型タバコから加熱式タバコへ切り替えた人(平均約2年、約半年から3年間)では、DNAメチル化マーカーのDNA低メチル化および遺伝子発現パターンの増減は、従来型タバコ喫煙者よりも程度は低いものの、非喫煙者とは異なるパターンを示すことが明らかになりました。今回解析した加熱式タバコ使用者は、加熱式タバコへ切り替えてから3年以下でした。従って、加熱式タバコの長期使用による分子遺伝学的影響については、今後疫学的な追跡調査を実施して明らかにする必要があります。また、今回のDNAメチル化解析は過去に報告されている喫煙との関連が示唆されているDNAメチル化マーカーに限定した解析になり、それ以外のCpG部位におけるDNAメチル化パターンについては明らかになっていません。そのため、今後、ゲノム上のCpGを網羅的に解析できるマイクロアレイ解析*5や全ゲノムバイサルファイトシークエンシング解析*6などを行い、今回解析対象としていないCpG部位におけるDNAメチル化状態を解析し、加熱式タバコ使用によるDNAメチル化への影響をより詳細に調べる必要があります。
謝辞
本研究は、慶應義塾大学先端生命科学研究所教育研究事業、並びに日本医療研究開発機構(AMED):循環器疾患・糖尿病等生活習慣病対策実用化研究事業(DNAメチル化・トランスクリプトーム・血漿メタボロームの3層オミクス解析を用いた電気加熱式たばこの喫煙・受動喫煙の健康影響に関する疫学研究)の支援を受けて実施しました。本研究の実施にあたり、岩手医科大学は慶應義塾大学と研究開発契約を締結しており、また、本研究における慶應義塾大学の別研究開発契約先である国立がん研究センターの協力を得ております。
その他
*Ploom TECHは、日本たばこ産業株式会社の商標または登録商標です。
*IQOSは、Philip Morris International Inc.の商標または登録商標です。
*gloは、British American Tobacco Plc.の商標または登録商標です。
参考文献
- Schaller JP, Keller D, Poget L, et al. Evaluation of the Tobacco Heating System 2.2. Part 2: Chemical composition, genotoxicity, cytotoxicity, and physical properties of the aerosol. Regul Toxicol Pharmacol. 2016;81:S27-S47. doi:10.1016/j.yrtph.2016.10.001
- Bekki K, Inaba Y, Uchiyama S, Kunugita N. Comparison of Chemicals in Mainstream Smoke in Heat-not-burn Tobacco and Combustion Cigarettes. J UOEH. 2017;39(3):201-207. doi: 10.7888/juoeh.39.201.
- Park ST, Kim J. Trends in next-generation sequencing and a new era for whole genome sequencing. Int Neurourol J. 2016;20:76-83. doi:10.5213/inj.1632742.371.
- Zeilinger S, Kühnel B, Klopp N, et al. Tobacco Smoking Leads to Extensive Genome-Wide Changes in DNA Methylation. PLoS One. 2013;8(5). doi:10.1371/journal.pone.0063812.
- Shenker NS, Ueland PM, Polidoro S, et al. DNA methylation as a long-term biomarker of exposure to tobacco smoke. Epidemiology. 2013;24(5):712-716. doi:10.1097/EDE.0b013e31829d5cb3.
- Guida F, Sandanger TM, Castagné R, et al. Dynamics of smoking-induced genome-wide methylation changes with time since smoking cessation. Hum Mol Genet. 2015;24(8):2349-2359. doi:10.1093/hmg/ddu751.
- Fasanelli F, Baglietto L, Ponzi E, et al. Hypomethylation of smoking-related genes is associated with future lung cancer in four prospective cohorts. Nat Commun. 2015;6 :1-9. doi:10.1038/ncomms10192.
用語解説
*1 DNAメチル化
DNAを構成する塩基A(アデニン)、C(シトシン)、G(グアニン)、T(チミン)のうち、主にCとGが並ぶ部位(CpG)のCにメチル基が付くことをいう。発生時期の細胞の種類の決定や遺伝子発現の制御などに関与しており、生活習慣や環境化学物質の曝露などによって後天的に変化します。
*2 従来型タバコ
従来型の紙巻きタバコのことです。
*3 鶴岡メタボロームコホート研究
慶應義塾大学医学部と同先端生命科学研究所(山形県鶴岡市)により実施されている研究で、2012年から2015年に鶴岡市在住・在勤者を対象に約1万1千人が参加登録されている。収集した血漿および尿におけるメタボローム解析を軸に、血液におけるゲノム解析やDNAメチル化解析、遺伝子発現解析を組み合わせた「マルチオミクス解析」を実施しています。
*4 主成分分析(Principal Component Analysis; PCA)
統計学における多変量解析の1つで、多種類ある複雑なデータ(多次元データ)をその特徴を損なわずにわかりやすいデータ(低次元データ)に要約することで、視覚的にどの程度のばらつきがあるかをわかりやすく示すことができます。
*5 マイクロアレイ解析
微細なガラス基板上にプローブと呼ばれる解析対象となる配列が並んでおり、その基板上に解析サンプルを滴下し、くっつける(ハイブリダイズする)ことによって、解析することができます。マイクロアレイには、DNAメチル化解析用のみならず、遺伝子変異や一塩基多型(SNP)解析用、遺伝子発現解析用などさまざまあります。
*6 全ゲノムバイサルファイトシークエンシング解析
DNAメチル解析方法の1つです。全ゲノムには2800万から3000万ヶ所のCpG部位が存在すると考えられていますが、その全てを対象にDNAメチル化解析を行うことができる方法です。
論文情報
掲載雑誌
Cancer Epidemiology, Biomarkers & Prevention(オンライン)
論文タイトル(英語)
DNA methylation abnormalities and altered whole transcriptome profiles after switching from combustible tobacco smoking to heated tobacco products
論文タイトル(日本語)
紙巻きタバコから加熱式タバコへの切り替えによる血液細胞におけるDNAメチル化プロファイルおよびトランスクリプトームプロファイルの変化
著者名(英語)
Hideki Ohmomo, Sei Harada, Shohei Komaki, Kanako Ono, Yoichi Sutoh, Ryo Otomo, So Umekage, Tsuyoshi Hachiya, Kota Katanoda, Toru Takebayashi, Atsushi Shimizu*
*責任著者
著者名(日本語)
大桃 秀樹1、原田 成2、小巻 翔平1、小野 加奈子1、須藤 洋一1、大友 亮1、梅影 創1、八谷 剛史1、片野田 耕太3、武林 亨2、清水 厚志1*
*責任著者
著者所属
1. 岩手医科大学 いわて東北メディカル・メガバンク機構 生体情報解析部門
2. 慶應義塾大学 医学部 衛生学公衆衛生学教室
3. 国立研究開発法人 国立がん研究センター がん対策情報センター がん統計・総合解析研究部
DOI
10.1158/1055-9965.EPI-21-0444
問い合わせ先
研究内容に関して
岩手医科大学
いわて東北メディカル・メガバンク機構 生体情報解析部門
教授 清水 厚志
鶴岡メタボローム研究について
慶應義塾大学
医学部 衛生学公衆衛生学
教授 武林 亨
報道に関して
岩手医科大学
法人事務部 総務課 広報係
慶應義塾大学
信濃町キャンパス総務課
国立がん研究センター
企画戦略局 広報企画室