アルツハイマー病の治療薬開発に新たな視点を提示
2022-01-17 量子科学技術研究開発機構
発表のポイント
- アルツハイマー病などの神経変性疾患1)の原因と考えられているアミロイドタンパク質凝集体について、細胞への毒性が強いアミロイドタンパク質凝集体では、毒性が弱い凝集体よりもタンパク質の動き2)が大きく、かつ速いことを世界で初めて明らかに。
- 最先端の中性子非弾性散乱3)装置を用いて、細胞毒性の異なるアミロイドタンパク質凝集体の運動の違いを原子レベルで解析。
- 本成果はアルツハイマー病の治療薬の設計・開発に、「原子運動」という全く新しい視点から寄与すると期待。
国立研究開発法人量子科学技術研究開発機構(理事長 平野 俊夫)量子生命・医学部門 量子生命科学研究所 構造生物学研究グループの松尾 龍人主幹研究員、ラウエ・ランジュヴァン研究所(フランス)の Alessio De Francesco 博士、グルノーブル・アルプス大学(フランス)のJudith Peters 教授らは共同で、アルツハイマー病など神経変性疾患の原因とされているアミロイドタンパク質凝集体について、細胞への毒性の強さが異なる凝集体の間には、原子運動の大きさと速さに違いがあることを世界で初めて明らかにしました。
アルツハイマー病では、アミロイド原因タンパク質が集合したアミロイド凝集体が、体内に沈着および蓄積することが知られています。また、同じタンパク質であっても、凝集する時の条件によって異なる形を持つアミロイド凝集体が形成され、凝集体の種類に応じて細胞への毒性の強さが異なることが報告されていました。凝集体の運動と細胞毒性および症状の因果関係はまだ明確ではありませんが、凝集体が細胞膜に結合して病気を引き起こすこと、また一般的に、タンパク質の動きが結合に重要な役割をすることが知られています。そのため、細胞毒性の強さが異なる仕組みを明らかにするためには、まず凝集体の性質の違いを明らかにする必要がありました。これまで、このような凝集体の形の違いについての知見は得られていましたが、もう 1 つの重要な側面である凝集体の運動の違いについては詳細が不明なままでした。そこで、近年提案された「強い毒性を持つ凝集体の運動は、弱い毒性を持つ凝集体よりも激しい」という仮説のもとに、双方の凝集体の運動を詳細に解析しました。
研究チームは、アミロイド凝集研究のモデルタンパク質「リゾチーム4)」から形成した、細胞毒性が大きく異なる 2 種類の凝集体の運動を、ラウエ・ランジュヴァン研究所の中性子非弾性散乱装置を用いて解析した結果、毒性が強い凝集体の中には、毒性が弱い凝集体に比べて、大きく且つ速く運動する原子が多く存在することを発見しました。さらに、双方の凝集体間で運動の大きさが異なる原子の数が、凝集体を構成する全原子の 1 割にも満たないことを突き止めました。
本研究により前述の仮説を実証すると共に、強い細胞毒性を示す凝集体に特有の原子運動を明らかにすることができました。これは、凝集体の細胞膜への結合からアミロイド凝集による神経変性疾患発症に至るプロセスの全容を解明する上で鍵となる成果です。さらに、本研究で明らかにしたアミロイド凝集体の特定の運動を変えるような新しい薬剤分子を設計・開発することは、「原子運動」というこれまでにない視点から病気の発症や進行を抑制する、医学の新たなアプローチを開拓するものと言えます。
なお、本研究成果は令和 4 年 1 月 17 日(月)14:00(日本時間)に Frontiers in Molecular Biosciences に掲載されました。
研究開発の目的と背景
アルツハイマー病や全身性アミロイドーシスなど、いわゆる「アミロイド病 1)」では、その原因となるタンパク質が繊維状に凝集したアミロイド凝集体が、神経細胞やさまざまな臓器内へ沈着・蓄積することで発症へと至ります。しかし、その発症メカニズムはまだ解明されていません。
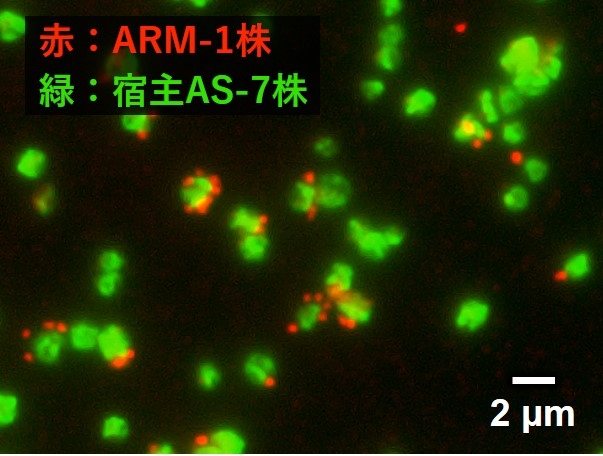
アミロイド病研究の代表的なモデルタンパク質である、ニワトリ由来のタンパク質「リゾチーム」を用いた過去の研究から、酸性条件で調製したアミロイド凝集体(以下、凝集体A)は分散して長い線維を形成し細胞毒性が弱いこと、中性条件で調製した凝集体(以下、凝集体N)は短い線維が塊を作り細胞毒性が強いことが知られていました(図 1)。凝集体N が短い線維であることは、凝集体 A よりも線維が折れやすく壊れやすい性質であることを示しています。この現象を説明するために、「凝集体 N の運動が凝集体 A よりも激しい」という仮説が最近提案されていましたが、その真偽は不明なままでした。凝集体の性質が最終的には細胞毒性の発現につながるため、この仮説の真偽を明らかにすることは、アミロイド病発症メカニズムの解明において重要な鍵になります。
そこで研究チームは、この仮説を検証するため、凝集体 A と凝集体 N の運動の違いを原子レベルで明らかにすることを試みました。

図 1. 異なる細胞毒性を示すリゾチームアミロイド凝集体
アミロイド凝集体は細胞膜に結合し、細胞膜を歪めたり破壊したりすることで細胞毒性を示し、細胞死を引き起こすと考えられている。そのため、細胞膜への結合を考える上で、凝集体の運動に関する知見が求められてきた。
研究の手法と成果
細胞毒性が異なる凝集体が得られる酸性および中性条件で調製したリゾチームのアミロイド凝集体(凝集体 A 及び凝集体 N)の運動を、中性子非弾性散乱法を用いて調べました。中性子は実験試料に含まれる水素原子に当たると散乱します。その散乱した中性子のエネルギーや速度を測定し解析することで、実験試料中の水素原子がどのように運動しているかを調べることができます。特にタンパク質では、その分子内に水素原子がほぼ均一に分布しているため、実験から得られる水素原子の動き(以下、原子運動と記述)は、タンパク質分子全体に渡って平均化された動きを表します。中性子非弾性散乱には弾性非干渉性中性子散乱(EINS) と中性子準弾性散乱(QENS)があり、今回はこの両方の手法を用いました。EINS では主に原子の運動の大きさを、QENS では主に原子の運動の速さを解析することができます。中性子散乱実験は、世界最高性能の研究用原子炉を有するフランスのラウエ・ランジュヴァン研究所にある IN13 分光器(図 2)で行いました。

図 2. フランスにあるラウエ・ランジュヴァン研究所(左)の IN13 分光器(右)
最初に、前述のリゾチーム凝集体 A および凝集体 N を実験試料として EINS 実験を行い原子運動の大きさを調べました。得られたデータから、凝集体を構成する原子運動の大きさを解析したところ、凝集体 A と比べて凝集体 N の方が、大きく運動する原子が多く含まれており、逆に小さく運動する原子の数が少ないことがわかりました(図 3)。特に、凝集体 N では約 0.3-1.0 Å (1 Å (オングストローム)は 100 億分の 1 メートル)の範囲の運動の大きさを持つ原子が増えていました。自然界に存在する最も小さな原子、水素原子の半径は約 0.5 Åです。この結果は、水素原子 1 個程度の運動の大きさの違いが、究極的には、異なる細胞毒性を示す凝集体の性質を作り出していることを示しています。さらに、双方の凝集体間で、運動の大きさが異なる原子の数を見積もったところ、それは凝集体を構成する全原子の 1 割にも満たないことがわかりました。
次に研究チームは、同じ IN13 分光器を用いて原子の運動の速さを解析できる QENS 実験を行いました。QENS 実験で得られたデータを解析したところ、凝集体 N の原子は、凝集体 A の原子よりも約1.6 倍速く動いていることがわかりました(図3)。さらに、速く動く原子は、凝集体の内側ではなく外側に集まっている可能性が高いこともわかりました。これは、凝集体が他の分子に結合したり相互作用したりするとき、直接関わる部分に原子運動の違いがあることを示しています。
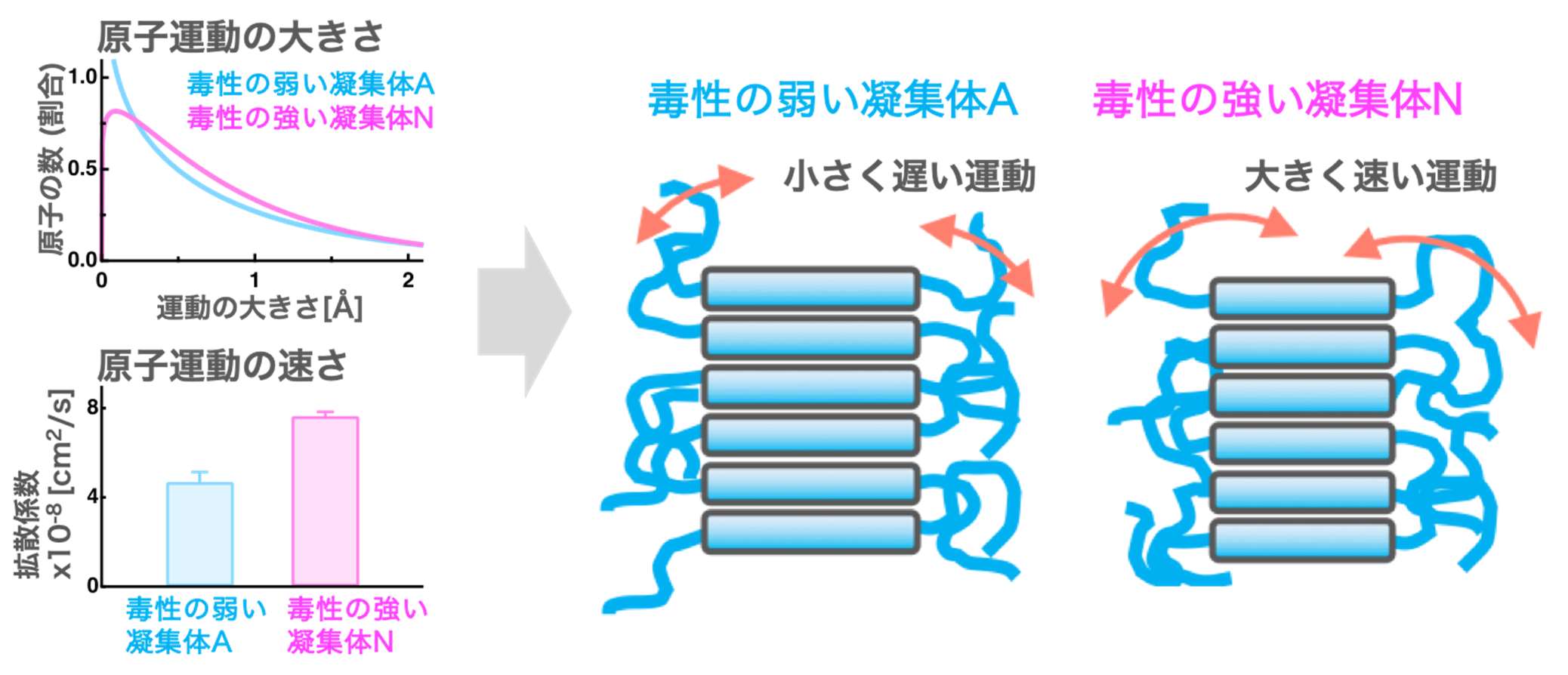
図 3. 異なる細胞毒性を示すリゾチーム凝集体を構成する原子運動の大きさ及び速さの比較
(右図)本研究で明らかになった、異なる細胞毒性を示すリゾチーム凝集体の運動の特徴。凝集体は中心部分(長方形)と外側部分(曲線)から構成される。原子運動の大きさ及び速さが、細胞毒性の強さに影響していると考えられる。
今回の研究で初めて、異なる細胞毒性を持つリゾチームアミロイド凝集体の間には、原子の運動の大きさおよび速さに違いがあることが明らかとなりました。そこで、今回明らかになった知見を基に細胞毒性が異なる仕組みを考えると、以下のようになります(図 4)。アミロイド凝集体が細胞毒性を引き起こす原因として、凝集体が細胞膜に結合し膜にダメージを与えるという現象があります。凝集体が細胞膜に結合するとき、凝集体は結合しようとする部位に適した形を取る必要があります。凝集体 N に比べて、凝集体 A の原子は運動の大きさも速さも制限されているため、その適した形に到達するまでに時間がかかる一方、原子が大きく速く運動する凝集体 N はいろいろな形を素早く取れるため、凝集体 A よりも素早く細胞膜結合に必要な形に到達できます。ここで、数多くの凝集体 A を含む細胞と数多くの凝集体N を含む細胞を考えると、ある一定の時間内に、凝集体 N の方がより多く細胞膜へ結合することができます。その結果、後者の細胞では膜のダメージも起きやすくなり、最終的には細胞毒性が強くなると考えられます。
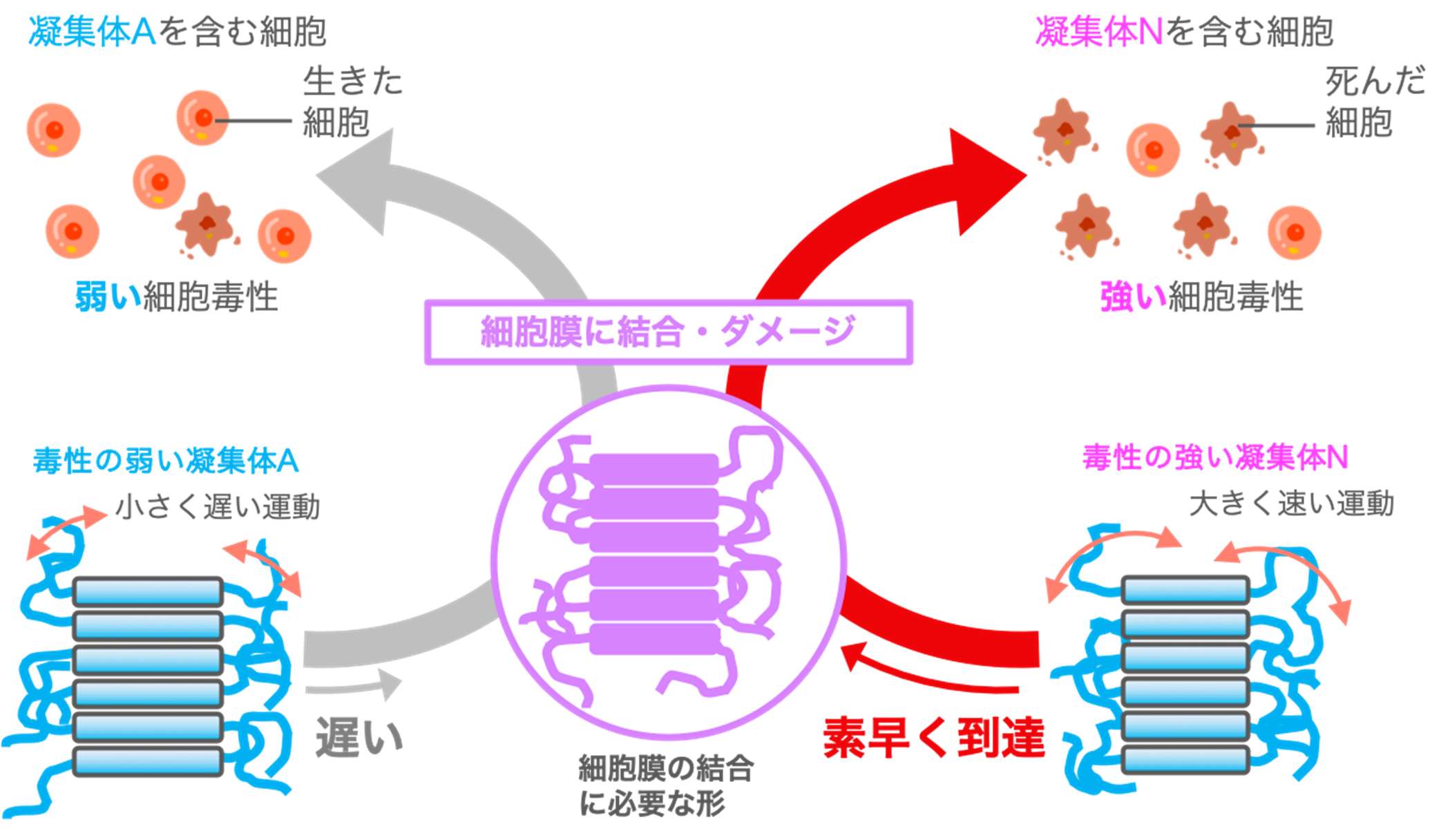
図 4. 本成果から推測される原子運動の異なる凝集体が細胞毒性の差を引き起こす仕組み
今後の展開
物質内の原子運動を調べる上で有力な方法である中性子非弾性散乱法を用いて、異なる強さの細胞毒性を示すリゾチームアミロイド凝集体の原子運動が、大きさおよび速さのいずれにおいても異なることを発見しました。また特に、凝集体の性質に関する仮説を実証すると共に、強い細胞毒性を示す凝集体に特有の原子運動を明らかにすることができました。
細胞毒性の発現には、凝集体と細胞膜の結合という過程が関係しています。本研究により、凝集体の原子運動について大きさおよび速さの両面が明らかになったことで、今後、より複 雑な現象である凝集体と細胞膜の結合の仕組みを原子レベルで解明するための道が拓けまし た。これは、細胞の毒性が決まるプロセス、ひいてはアミロイド病発症機構の全容解明につ ながります。さらに、本研究で明らかにしたアミロイド凝集体の特定の運動を変えるような 新しい薬剤分子を設計・開発することで、アミロイド病の治療法確立に向けて、原子運動と いう全く新しい視点からアプローチすることが可能になると期待されます。
論文情報
雑誌名:Frontiers in Molecular Biosciences
論文タイトル:Molecular dynamics of lysozyme amyloid polymorphs studied by incoherent neutron scattering
著者:Tatsuhito Matsuo, Alessio De Francesco, and Judith Peters DOI:10.3389/fmolb.2021.812096
用語解説
1.神経変性疾患、アミロイド病
タンパク質が繊維状に凝集したアミロイド線維が、体内のさまざまな組織に沈着および蓄積する病気をアミロイド病(またはアミロイドーシス)と呼ぶ。特に、アミロイド線維が神経細胞に沈着および蓄積する病気を神経変性疾患と言う。アミロイド線維を形成するタンパク質は、疾患ごとに異なる。社会問題にもなっているアルツハイマー病では、脳にアミロイドβ(ベータ)というタンパク質のアミロイド線維が蓄積し、思考障害や記憶障害が生じる。また、アミロイド線維が複数集まり凝集体を作ることもある。線維やこうした凝集体を含め、アミロイド凝集体またはアミロイドタンパク質凝集体と呼ぶ。
2.タンパク質の動き
一般的に「タンパク質の動き」は、タンパク質分子を構成する原子 1 個の動きからタンパク質分子全体の動きに至るまで、幅広い時間および大きさのスケールに渡る。本文には「タンパク質の動き」、「凝集体の運動」、「原子運動」といった用語が出てくる。本文中に出てくる「運動」のうち、「原子運動」と言及した箇所では、ある水素原子 1 個(本研究では水素原子の動きを観測している)に視点を当 て、それが動いているという局所的な運動の様子をイメージしている(図 5)のに対し、「タンパク質の動き」および「凝集体の運動」と言及した箇所では、凝集体全体に視点を移し、凝集体全体に渡って存在する無数の水素原子がゆらゆらと運動している様子をイメージしている。
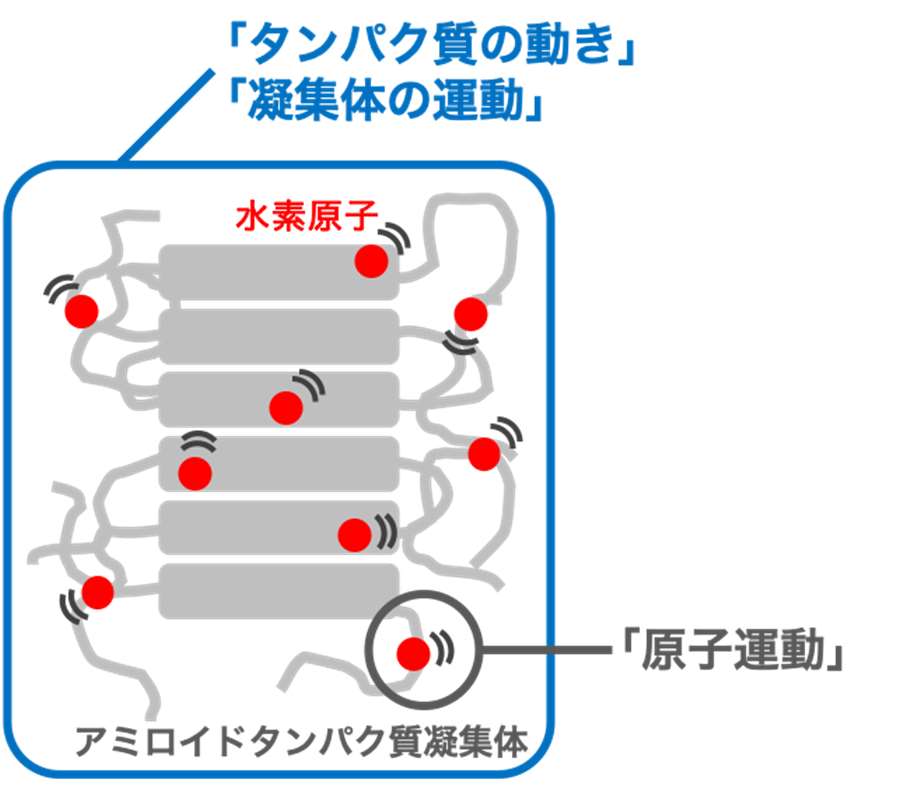
図 5. タンパク質の動き
アミロイドタンパク質凝集体を灰色で、凝集体を構成する水素原子を赤丸で示す。見やすくするために数個の水素原子しか描いていないが、実際は凝集体全体に渡って無数に存在する。
3.中性子非弾性散乱
中性子は原子核を構成する粒子の 1 つである。研究用原子炉や陽子加速器と呼ばれる大型施設で作られる中性子ビームを物質に当てると、中性子は主に物質内の水素原子と相互作用し、様々な方向へ散乱される。このとき、散乱した中性子は物質との相互作用によってエネルギーが変化しない場合や、エネルギーを獲得または損失する場合がある。複数の散乱角において散乱中性子の個数やエネルギーを詳細に調べることで、物質内の水素原子の運動の大きさや速さ等を調べることができる。物質との相互作用の前後でエネルギーが変化しない中性子のみを検出する手法を弾性非干渉性中性子散乱(EINS)と呼び、主に原子の運動の大きさが分かる。一方、物質との相互作用によってエネルギーが変化する中性子も検出する方法を中性子準弾性散乱(QENS)と呼び、主に原子の運動の速さが分かる。
4.リゾチーム
さまざまな動植物が有するタンパク質であり、細菌を保護する細胞壁を溶かすことで感染から生体を守る役目をする生体防御物質である。ヒトのリゾチームは、遺伝的な要因によって体内でアミロイド凝集体を形成し、全身性アミロイドーシス(リゾチームアミロイドーシス)を引き起こす。肝臓や腎臓にリゾチームアミロイド凝集体が蓄積し、機能不全や出血をもたらし、多くは致死的である。容易に入手可能なニワトリのリゾチームはヒトのリゾチームと形および性質が非常に良く類似しているため、アミロイドーシスの研究に昔から広く用いられている。