2022-02-08 大阪大学,日本医療研究開発機構
概要
大阪大学 微生物病研究所 遺伝子生物学分野の原 英二教授(兼:大阪大学 免疫学フロンティア研究センター、大阪大学 感染症総合教育研究拠点)、辻 竣也特任研究員らを中心とするグループは、新型コロナウイルスに感染した細胞が放出するサイトカインによって、周囲の感染していない細胞が細胞老化(注1)を起こし、ウイルスが消失した後も長期にわたり老化細胞から炎症性物質が分泌され続けることを見出しました。本研究成果は新型コロナウイルス感染症の病態の理解を深めると同時に、老化細胞の蓄積を抑制することで、新型コロナウイルス感染症(COVID-19)の後遺症の改善につながる可能性が期待されるものです。本研究成果は令和4年1月25日付けで米国の科学雑誌『Nature Aging』にオンライン掲載されました。
研究背景
近年、新型コロナウイルスに代表される世界的なアウトブレークを引き起こす感染症が社会問題になってきており、その効果的な感染予防法や治療法の開発が進められています。一方、国内外の調査から、COVID-19患者では40%以上の人がウイルスが検出されなくなった後も、倦怠感、呼吸困難、関節痛、胸痛、頭痛、味覚障害、食欲不振、めまい、筋肉痛、下痢、脱毛等、何らかの後遺症に悩まされていることが報告されていますが、そのメカニズムについては良く分かっていません。既に世界で3億人を超える人が新型コロナウイルスに感染しており、今後も感染者が増加する可能性が高いことを考えると、COVID-19の後遺症についてもその発症機序を明らかにし、効果的な予防法や治療法の開発につなげることが必要です。
研究内容
大阪大学の原 教授と辻 特任研究員らのグループは新型コロナウイルスが高齢者や糖尿病患者でより重篤な症状を引き起こすことと、それらの人に共通した現象として、体内に細胞老化を起こした細胞(老化細胞)が増加していることに着目しました。細胞老化は、発がんの危険性がある様々なストレスによってがん抑制遺伝子であるp16INK4a 等が働くことで起こる、不可逆的な細胞分裂停止状態です。このため細胞老化は長い間、がん抑制機構であると考えられてきました。しかし、近年の研究により、老化細胞は単に細胞分裂を停止しているだけではなく、炎症性サイトカインやケモカイン等、様々な炎症性物質を分泌するSASP(注2)と呼ばれる現象を起こすことで慢性炎症の原因になっていることが明らかになりつつあります。COVID-19の後遺症の多くに慢性炎症が関与している可能性が指摘されているため、原 教授と辻 特任研究員らは細胞老化がCOVID-19の後遺症に関与しているのではないかと考え、正常なヒトの培養細胞および気管支オルガノイドに新型コロナウイルスを感染させ、その反応を詳細に解析しました。その結果、新型コロナウイルス感染細胞はその殆どが数日以内に死滅しますが、感染細胞が死滅する前に分泌するTNFα等のサイトカインにより非感染細胞が細胞老化を起こし、ウイルス感染細胞が死滅した後も老化細胞がSASPを起こすことで炎症反応が持続することを見出しました。実際に、重篤なCOVID-19の後遺症を発症した患者の肺組織においてもウイルスが消失した後で細胞老化及びSASPが起こっていることが確認されました(図1a)。また、ハムスターやマウスに新型コロナウイルスを感染させた場合にも肺の非感染細胞に細胞老化が起こり、炎症反応が長期に持続することを見出しました(図1b)。更にマウスに新型コロナウイルスを感染させた後にセノリティック薬(注3)の1つであるABT-263を投与したところ、老化細胞が減少し、炎症反応も低下しました(図1b)。このことから、新型コロナウイルスの感染によって間接的に誘導される老化細胞の存在が、ウイルスが消失した後でも炎症反応が続く原因の一つになっている可能性が考えられます(図2)。
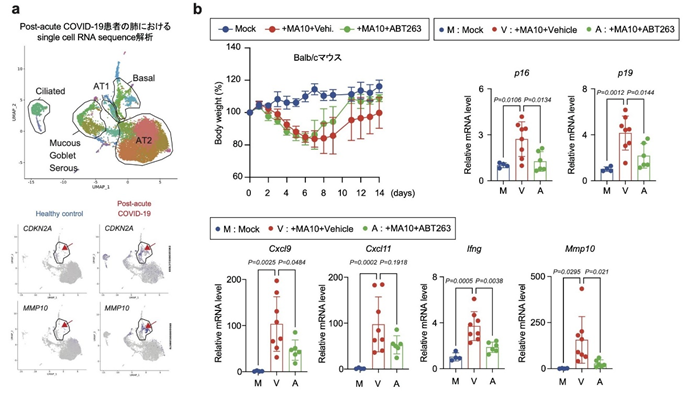
図1 ヒト及びマウスの肺組織における新型コロナウイルスによる細胞老化の誘導
- COVID-19後遺症 (Post-acute COVID-19)の患者の肺のSingle cell RNA sequence解析
- マウスに感染できる新型コロナウイルス(MA10)を感染させたBalb/cマウスにおけるセノリティック薬(ABT-263)の効果
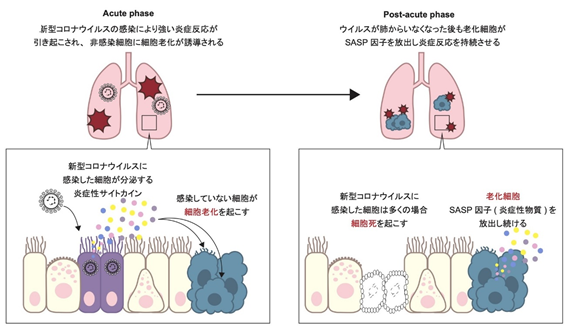
図2 新型コロナウイルスによる細胞老化の誘導と炎症反応の持続
将来の展望
上記の研究成果は、新型コロナウイルスの感染によって引き起こされる生体反応の理解を深めると同時に、これまで良く分かっていなかったCOVID-19の後遺症のメカニズムの一端を明らかにしたと考えられます。また、老化細胞を標的とすることでCOVID-19の後遺症の予防法や治療法の開発につながる可能性も期待されます。一方、老化細胞には生体機能の維持に必要な役割も担っている可能性もありますので、今後、慎重に研究を続けることで安全かつ効果的に老化細胞の蓄積を制御する方法の開発を目指していきたいと考えています。
研究支援
本研究成果は大阪大学、京都大学、大阪市立大学との共同研究によるものです。また本研究は、主に以下の研究費の支援によって行われました。
- 日本医療研究開発機構 老化メカニズムの解明・制御プロジェクト「老化機構・制御研究拠点」(研究代表者:原 英二 大阪大学 微生物病研究所 教授)
- 三菱財団 自然科学研究特別助成「新型コロナウイルス感染症及び後遺症における細胞老化の役割とメカニズムの解明」(研究代表者:原 英二 大阪大学 微生物病研究所 教授)
論文情報
- タイトル
- SARS-CoV-2 infection triggers paracrine senescence and leads to a sustained senescence-associated inflammatory response
- 著者
- Shunya Tsuji, Shohei Minami, Rina Hashimoto, Yusuke Konishi, Tatsuya Suzuki, Tamae Kondo, Miwa Sasai, Shiho Torii, Chikako Ono, Shintaro Shichinohe, Shintaro Sato, Masahiro Wakita, Shintaro Okumura, Sosuke Nakano, Tatsuyuki Matsudaira, Tomonori Matsumoto, Shimpei Kawamoto, Masahiro Yamamoto, Tokiko Watanabe, Yoshiharu Matsuura, Kazuo Takayama, Takeshi Kobayashi, Toru Okamoto and Eiji Hara
- 雑誌
- Nature Aging(2022)
- DOI番号
- 10.1038/s43587-022-00170-7
用語解説
- (注1)細胞老化
- 正常な哺乳動物の体細胞は細胞分裂を繰り返しながら増殖しますが、その多くはある一定の回数しか分裂することが出来ません。限界まで分裂した細胞は細胞分裂を不可逆的に停止し、もはや分裂を再開することはありません。この現象が「細胞老化」と呼ばれ、細胞の分裂回数を制限することで、細胞が過度に増殖してがん化することを防いでいると考えられています。また、分裂限界に達する前でも、がん遺伝子の活性化など、細胞に発がんの危険が生じると、速やかに細胞老化と同様な不可逆的な細胞分裂停止を起こすことも明らかになっています。
- (注2)SASP
- 細胞老化を起こした細胞は、単に細胞分裂を停止して増殖を抑えるだけではなく、炎症性サイトカインを含む様々な分泌性タンパク質を高発現します。この現象は、SASP(Senescence associated secretory phenotype)と呼ばれ、SASPにより分泌されるタンパク質をSASP因子と呼びます。
- (注3)セノリティック薬
- 細胞老化を起こした細胞を特異的に除去する作用がある薬剤
お問い合わせ
研究に関する問い合わせ先
大阪大学 微生物病研究所 遺伝子生物学分野 教授
原 英二
AMED事業に関する問い合わせ先
日本医療研究開発機構(AMED)
疾患基礎研究事業部 疾患基礎研究課
老化メカニズムの解明・制御プロジェクト