2022-03-30 国立感染症研究所,東京大学,日本医療研究開発機構
研究成果のポイント
- 新規抗原を用いたCD8陽性T細胞誘導HIVワクチン(注1)の経直腸粘膜感染防御効果を動物実験で明らかにしました。
- 多様性の高い表面蛋白抗原を用いないHIVワクチンで、抗体によらない粘膜感染防御効果を初めて示しました。
- 多様性の高いHIVに対する有効なワクチンとして、実用化に向けた今後の進展が期待されます。
発表概要
予防HIVワクチン開発は、国際的な重要課題です。これまでは、特に中和抗体誘導ワクチン開発が進められてきましたが、中和抗体の標的となる表面蛋白抗原は多様性が極めて高いため、多様性に富むHIV株に対応できるワクチンの開発は困難で難航してきました。俣野哲朗(国立感染症研究所エイズ研究センター長、東京大学医科学研究所附属病院エイズワクチン開発担当分野教授[委嘱])らの研究グループは、HIVの主標的となるHIV特異的CD4陽性T細胞を誘導せずにHIV特異的CD8陽性T細胞を誘導する新規抗原を設計し、動物実験でHIV経直腸粘膜感染防御効果を明らかにしました(図1)。本研究成果は、多様性の高い表面蛋白抗原を用いないHIVワクチンで初めて抗体非依存性の粘膜感染防御効果を示すものです。本研究の新規抗原設計を導入したHIVワクチンは、CD8陽性T細胞を選択的に誘導しHIVの多様性の影響が少ない有効なワクチンとして、実用化に向けた今後の進展が期待されます。
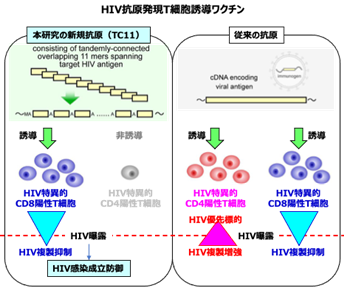
図1 本研究の新規HIVワクチン抗原の有効性を示すシェーマ従来のT細胞誘導HIVワクチンでは、HIV複製抑制能を有するHIV特異的CD8陽性T細胞だけでなく、HIVの優先標的でHIV複製増強効果を有するHIV特異的CD4陽性T細胞を誘導しています。本研究の新規抗原は、後者を誘導せず前者のみを誘導するため、感染成立防御効果が示されました。
発表内容
HIV感染症の制圧は国際的重要課題であり、予防ワクチン開発が切望されています。感染拡大の抑制には、早期診断・治療促進が重要ですが、それだけでは不十分であり、有効性50-70%のワクチンでも導入効果が期待しうることが示されています。
HIVワクチン開発においては、抗原導入のためのウイルスベクター等のデリバリープラットフォームの開発は進展してきましたが、抗原至適化が課題です。特に、多様性に富むHIVに対するワクチン抗原開発は、容易ではなく難航しています。中和抗体誘導はHIVワクチン開発の重要戦略ですが、中和抗体の標的となる表面蛋白抗原の多様性が極めて高いため、広域交差性中和抗体誘導を目指した研究が進められているものの、誘導法の確立には至っていません。
一方、T細胞誘導ワクチン開発においても、抗原至適化が課題となっています。HIV特異的CD4陽性T細胞は、HIV感染の優先標的であることが知られていましたが、近年の研究で、ワクチンによるHIV特異的CD4陽性T細胞誘導は、HIV曝露後の感染増殖を増強してしまうことがわかってきました。
そこで本研究グループでは、HIV特異的CD4陽性T細胞を誘導せずにHIV特異的CD8陽性T細胞を誘導する新規抗原を設計しました。本抗原は、CD4陽性T細胞の標的至適エピトープが12アミノ酸以上のペプチドであるのに対し、CD8陽性T細胞の標的至適エピトープが8-11アミノ酸ペプチドであることに基づき設計された11アミノ酸ペプチド断片連結抗原です。動物実験で、この新規抗原発現ウイルスベクターワクチンの接種実験を行ったところ、HIV特異的CD4陽性T細胞を誘導せずにHIV特異的CD8陽性T細胞を誘導することが確認されました。
ベクターウイルス抗原特異的CD4陽性T細胞は誘導されており、これがヘルパーとして機能的HIV特異的CD8陽性T細胞誘導に貢献していることを示唆する結果も得られています。さらに、繰り返しの経直腸ウイルスチャレンジ実験(注2)を行ったところ、8回のチャレンジに対して、ワクチン接種群の2/3で感染が防御され、統計学的にも有意な感染防御効果が示されました(図2)。特にワクチン誘導Gag抗原特異的CD8陽性T細胞が感染防御に寄与していることを示唆する結果も得られました。
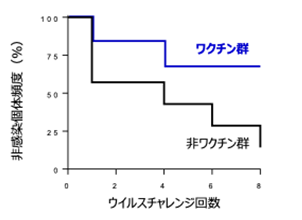
図2 ワクチン接種群における感染防御公開経直腸ウイルス接種(チャレンジ)各回毎の非感染個体の頻度を示します。2週間毎の計8回のチャレンジ後、非ワクチン接種群では7頭中6頭が感染しましたが、ワクチン接種群では12頭中8頭で感染が防御され、両群間で統計学的に優位な差が認められました。
HIVは粘膜上皮細胞には感染しませんが、トランスサイトーシス(注3)や粘膜損傷部位を介して粘膜バリアを通過し、粘膜下でCD4陽性Tリンパ球等の標的細胞に感染して増殖すると考えられています。本研究で示された結果は、ワクチン誘導CD8陽性T細胞によって、粘膜下でウイルス増殖が抑えられ、感染成立阻止にいたることを示唆しています。本研究成果は、多様性の高い表面蛋白抗原を用いないHIVワクチンで、初めて抗体非依存性の粘膜感染防御効果を示すものです。この抗原設計は、各種ウイルスベクターなどを含むワクチンシーズにも応用が可能です。本研究の新規抗原を導入したHIVワクチンは、HIVの多様性に対して交差性の高い有効なワクチンとして、臨床試験有効性評価段階への進展も含めて今後の発展が期待されます。
論文情報
- 雑誌名
- Molecular Therapy
- 論文タイトル
- Env-independent protection of intrarectal SIV challenge by vaccine induction of Gag/Vif-specific CD8+ T cells but not CD4+ T cells
- 著者
- Hiroshi Ishii, Kazutaka Terahara, Takushi Nomura, Midori Okazaki, Hiroyuki Yamamoto, Tsugumine Shu, Hiromi Sakawaki, Tomoyuki Miura, David I. Watkins, and Tetsuro Matano
- DOI
- 10.1016/j.ymthe.2022.02.023
- URL
- https://doi.org/10.1016/j.ymthe.2022.02.023
本研究への支援
本研究は、日本医療研究開発機構(AMED)エイズ対策実用化研究事業(JP21fk0410035)、地球規模保健課題解決推進のための研究事業(JP21jk0210002)などの支援で実施されました。
用語解説
- (注1)CD8陽性T細胞誘導HIVワクチン
- ウイルス感染に対するワクチンには、主にウイルスを標的としてウイルス感染を阻止する中和抗体を誘導するものが代表的ですが、さらにウイルス感染細胞を標的とするT細胞を誘導するものがあります。T細胞には、主にCD4という分子を発現するCD4陽性T細胞と、CD8という分子を発現するCD8陽性T細胞があります。後者はキラーT細胞とも呼ばれ、ウイルス感染細胞を殺傷する機能があり、前者はヘルパーT細胞とも呼ばれ、免疫反応の誘導を助ける機能があります。本研究は、HIV感染細胞を標的とするCD8陽性T細胞を誘導するワクチンの有効性を示すものです。
- (注2)経直腸ウイルスチャレンジ実験
- HIV性感染を反映する動物モデルで、ワクチンなどの感染防御効果の評価に用いられる代表的な実験系です。比較的低い容量のウイルスを直腸より接種することを、2週間毎に計8回繰り返し、大部分の非ワクチン群で感染成立する状況で、ワクチン群でどの程度の個体の感染が防御されるかを検証します。
- (注3)トランスサイトーシス
- 細胞に感染せずに、粘膜上皮側からウイルス粒子が取り込まれ、細胞内を通過して、粘膜下に通り抜ける機序のことです。
お問い合わせ先
本件に関する問い合わせ先
国立感染症研究所 エイズ研究センター センター長
東京大学医科学研究所附属病院 エイズワクチン開発担当分野 教授
俣野 哲朗(またの てつろう)
報道に関する問い合わせ先
東京大学医科学研究所国際学術連携室(広報)
清水 麻子(しみず あさこ)
AMED事業に関する問い合わせ先
日本医療研究開発機構
疾患基礎研究事業部 疾患基礎研究課
エイズ対策実用化研究事業
日本医療研究開発機構
国際戦略推進部 国際戦略推進課 国際連携推進室
地球規模保健課題解決推進のための研究事業