2022-06-03 群馬大学,日本医療研究開発機構
研究成果のポイント
- 腸管出血性大腸菌O157(以下、「O157」)に感染すると、重度の下痢に加え、しばしば急性腎不全や急性脳症を併発し、重症化することが知られています。現在、O157による感染症の重症化を予防、根本的に治療できる方法は確立されていません。
- 本研究では、「マクロ孔をもつ多孔質炭素(MgOC150)」を用いることで、O157が産生するベロ毒素(志賀毒素)や3型分泌タンパク質と呼ばれる病原性タンパクを吸着し無毒化することに成功しました。
- O157感染症の代替モデルであるシトロバクター菌を用いてマウス体内におけるMgOC150の効果を評価したところ、MgOC150を経口投与したマウスは、シトロバクター菌に対して抵抗性を示すことを明らかにしました。
- 一方で、MgOC150を投与したマウスでは、消化管をはじめとして異常は見られず、またヒトの大腸細胞や乳酸菌などの善玉菌の生育にも悪影響を与えませんでした。
以上の結果から、MgOC150を用いたO157感染症の新たな予防法、治療法の確立につながることが期待されます。
概要
群馬大学大学院医学系研究科細菌学講座の平川秀忠准教授らの研究グループ(富田治芳教授)は、同大大学院医学系研究科生体防御学講座の神谷亘教授、鈴江一友講師と株式会社クレハとの共同研究により、O157の無毒化に成功しました。本研究成果により、O157による食中毒の予防や治療法の発展に繋がることが期待されます(図1)。
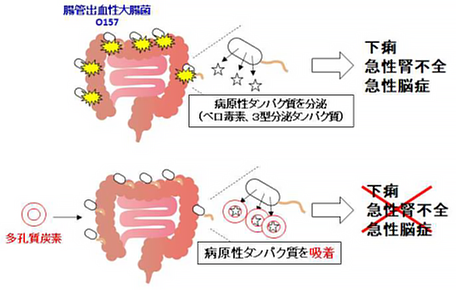
図1 多孔質炭素を利用したO157の無毒化
本研究成果は、英国時間の2022年5月6日に、国際雑誌『Frontiers in Microbiology』にオンライン掲載されました。
研究背景
O157に代表される腸管出血性大腸菌は、食中毒の原因菌として知られており、加熱が不十分な食肉や、本菌で汚染された水や調理器具、トング、箸などを介して調理された食材を摂取することで感染します。腸管出血性大腸菌による感染者は、全世界で毎年280万人以上にのぼると推定されています。
腸管出血性大腸菌に感染すると、出血性の下痢が起こるが、感染者の約5%(幼児や高齢者では約10%)が重症化し、溶血性尿毒症症候群(HUS)と呼ばれる致死性の急性腎不全や急性脳症を発症します。しかしながら、腸管出血性大腸菌感染症の治療は対症療法しかなく、HUSの発症をはじめとする本感染症の重症化を確実に予防、根本的に治療する方法は確立されていません。
腸管出血性大腸菌は、ベロ毒素(志賀毒素)や3型分泌タンパク質と呼ばれる病原性タンパク質を産生します。これらの病原性タンパク質が本感染症の重症化に寄与していることが知られています。
研究成果
本研究では、O157が産生する病原性タンパク質を吸着し解毒することを目的とし、多孔質炭素であるMgOC150(製品名:クノーベルMJ(4)150:東洋炭素株式会社)を用いました。MgOC150は、炭素表面に多数の孔(ポア)が存在し、その孔の中に様々な分子を捕捉(吸着)することができます。
多孔質炭素の仲間として「活性炭」が一般的によく知られていますが、多くの活性炭は孔の大きさが小さく低分子化合物は強く吸着可能である一方で、タンパク質性の高分子の吸着能が低いと考えられてきました。一方で、MgOC150は平均直径150 nmの孔を持つことから、タンパク質を強く吸着することが期待されています。
本研究では、MgOC150がベロ毒素と3型分泌タンパク質を強く吸着することを発見しました。さらに、O157の培養液にMgOC150を添加すると、ベロ毒素と3型分泌タンパク質が吸着され、無毒化することができました。
上記とあわせて、マウスの生体内でもMgOC150の効果を評価、検証を行いました。マウスに対する病原菌として、代替モデルのシトロバクター菌(学名:Citrobacter rodentium)を用いました。このシトロバクター菌をマウスに経口感染させたところ、感染後4日目以降に下痢に伴う体重減少が見られ、9日目までに全頭のマウスが死亡しました。一方で、MgOC150を経口投与したマウスでは、感染後9日目までは体重減少が観察されず、感染後14日まで延命させることができました。
シトロバクター菌を感染させていないマウスにMgOC150を経口投与し3週間経過観察を行ったところ、一過的な体重減少や生育遅延、消化管の損傷などといった異常は観察されませんでした。さらに、ヒトの大腸上皮細胞や乳酸菌、腸球菌といった善玉菌の生育にも悪影響を及ぼしませんでした。
以上の結果から、MgOC150は腸管出血性大腸菌感染症に対する重症化予防、治療効果を持つことが示唆されました(図2)。
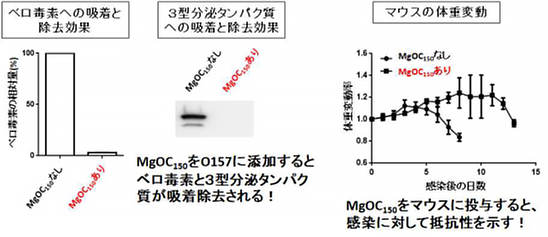
図2 多孔質炭素(MgOC150)によるベロ毒素と3型分泌タンパク質の吸着除去効果
今後への期待
1.腸管出血性大腸菌感染症の予防、治療法確立への足がかり
本研究で用いたMgOC150は、腸管出血性大腸菌O157が産生するベロ毒素と3型分泌タンパク質を吸着除去できることが示されました。従って、本物質は腸管出血性大腸菌感染症に対する予防、治療効果を有することが示唆されます。
本研究を足がかりとして、腸管出血性大腸菌感染症の予防、治療法の確立につながると期待されます。
2. 多孔質炭素の感染症(薬剤耐性菌感染症も含む)治療への適用の可能性
MgOC150を含む多孔質炭素は、これまでに酵素触媒の固定化や電極といった主に工業用としての用途で使用されてきました。一方で、多孔質炭素の医療目的での使用は一部に限られ、感染症への適用例はありません。MgOC150は、O157以外にも様々な細菌が産生する病原性タンパク質を吸着できる可能性があります。例えば、赤痢菌やコレラ菌などが産生する毒素は、ベロ毒素と類似した構造を有するため、MgOC150はこれらの毒素も吸着できることが期待されます。
また、近年、様々な既存の抗菌薬に対して耐性を持つ薬剤耐性菌の蔓延が社会的に大きな問題となっています。MgOC150により、薬剤耐性菌が産生する病原性タンパク質を吸着し、無毒化することができれば、薬剤耐性菌感染症に対する新たな治療オプションとして適用できる可能性があります。今後は、MgOC150の医薬品としての臨床応用に向けた課題の解決のため、さらに検討を進める必要があると考えます。
研究費
本研究は、日本学術振興会科学研究費助成事業及び日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業(22fk0108604h0901)による支援を受けて行われました。
論文情報
- 掲載雑誌
- Frontiers in Microbiology, 06 May 2022
- タイトル
- A Macroporous Magnesium Oxide-Templated Carbon Adsorbs ShigaToxins and Type III Secretory Proteins in Enterohemorrhagic Escherichia coli, Which Attenuates Virulence.
- 著者名
- Hidetada Hirakawa1, Kazutomo Suzue2, Motoyuki Uchida3, Ayako Takita1, Wataru Kamitani2 and Haruyoshi Tomita1,4
- 所属
- 1Department of Bacteriology, Gunma University, Graduate School of Medicine
2Department of Infectious diseases and host defense, Gunma University, Graduate School of Medicine
3R&D Strategy & Planning Department, Kureha Corporation
4Laboratory of Bacterial Drug Resistance, Gunma University, Graduate School of Medicine - doi
- 10.3389/fmicb.2022.883689
- 群馬大学プレスリリース
- https://www.gunma-u.ac.jp/information/129879
本件に関するお問い合わせ先
研究に関すること
群馬大学昭和地区事務部総務課法規・広報係
AMED事業に関すること
日本医療研究開発機構(AMED)
創薬事業部 創薬企画・評価課
新興・再興感染症に対する革新的医薬品等開発推進研究事業