- 幹細胞の働きを解明、加齢性疾患の新薬につながる可能性
Two new studies build knowledge upon how stem cells work; could lead to new drugs for age-related diseases
- メチオニンアデノシルトランスフェラーゼ2A阻害による代謝の回復で、老化した骨格筋の再生能力と筋力を向上させる。 Methionine adenosyltransferase2A inhibition restores metabolism to improve regenerative capacity and strength of aged skeletal muscle
- グルタミン酸分解の阻害は老化幹細胞のミトコンドリア機能を回復させる。 Inhibition of glutaminolysis restores mitochondrial function in senescent stem cells
幹細胞の働きを解明、加齢性疾患の新薬につながる可能性 Two new studies build knowledge upon how stem cells work; could lead to new drugs for age-related diseases
2023-02-16 バッファロー大学(UB)
◆バッファロー大学のステリオス・アンドレディス教授は、胚性遺伝子「NANOG」が老化した成体幹細胞や骨格筋細胞を再プログラムし、老化の特徴を逆転させることを明らかにしたのである。NANOGが具体的にどのように作用するのかは、これまで謎であった。
◆このたび、アンドレディスの研究室から新たに2つの研究結果が発表され、この疑問に対する答えが得られつつある。1つは『Cell Reports』誌で、老化した幹細胞のミトコンドリア機能を回復させる上でNANOGが果たす役割について調べたものである。もうひとつは、2月16日発行の『Nature Communications』誌で、NANOGが骨格筋の老化をどのように逆転させるかに光を当てたものである。
◆NANOGは、アイルランドに伝わる神話の「青春の地」にちなんで命名されましたが、今回の研究成果は、NANOGに対する科学界の理解を深めるとともに、この遺伝子を模倣した医薬品の開発につながる可能性があります。
◆老化した幹細胞でミトコンドリア機能を回復させる:Cell Reportsの研究チームは、老化した間葉系幹細胞に注目した。この細胞は、分裂や増殖の能力が著しく低下した老化細胞である。この細胞では、解糖とミトコンドリア呼吸が損なわれていることが判明した。この状態により、細胞は新たなエネルギー源を探すために、グルタミンと呼ばれるアミノ酸を分解するように代謝を再配線することになった。その結果、細胞内に尿素が蓄積され、ミトコンドリアがエネルギーを供給する能力がさらに低下し、老化が進むことになったのです。
◆そこで研究チームは、この代謝の乱れに対処するため、グルタミナーゼ1という酵素を抑制し、細胞がグルタミンを分解するのを阻害した。研究チームは、ハッチンソン・ギルフォード・プロジェリア症候群の患者の細胞でも、同様の結果が得られることを確認した。
◆骨格筋の老化を逆転させる:Nature Communications誌では、筋組織を構成する細胞である筋芽細胞の加齢と若返りによる代謝の変化を調査した。in vitroとin vivoの老化モデルを用いた実験から、筋芽細胞は解糖の障害とインスリン抵抗性に苦しんでいることが明らかになった。また、筋芽細胞は、肉や魚、乳製品に含まれる必須アミノ酸であるメチオニンを分解して、アデノシン三リン酸(細胞活動のエネルギー源となる有機化合物)を生成することも明らかになった。
◆この過程で大量のアンモニウムが生成され、細胞の老化を促進する可能性がある。この問題に対処するため、研究チームは、遺伝子にコードされた情報が機能に変換される過程であるNANOGを発現させました。すると、メチオニン経路の最初の酵素であるメチオニンアデノシルトランスフェラーゼ2Aの産生が抑制され、アンモニウムの減少、インスリン感受性の回復、グルコース取り込みの増加、損傷後の筋肉の再生が促進されました。
◆また、メチオニンアデノシルトランスフェラーゼ2Aを阻害すると、インスリンシグナルに関与する酵素であるAkt2のシグナル伝達が活性化することがわかりました。さらに、ピルビン酸キナーゼを修復し、解糖を回復させ、再生を促進することで、早老モデルマウスの筋力を著しく向上させることを明らかにしました。
<関連情報>
- https://www.buffalo.edu/news/releases/2023/02/011.html
- https://www.nature.com/articles/s41467-023-36483-3
- https://www.sciencedirect.com/science/article/pii/S2211124722016229?via%3Dihub
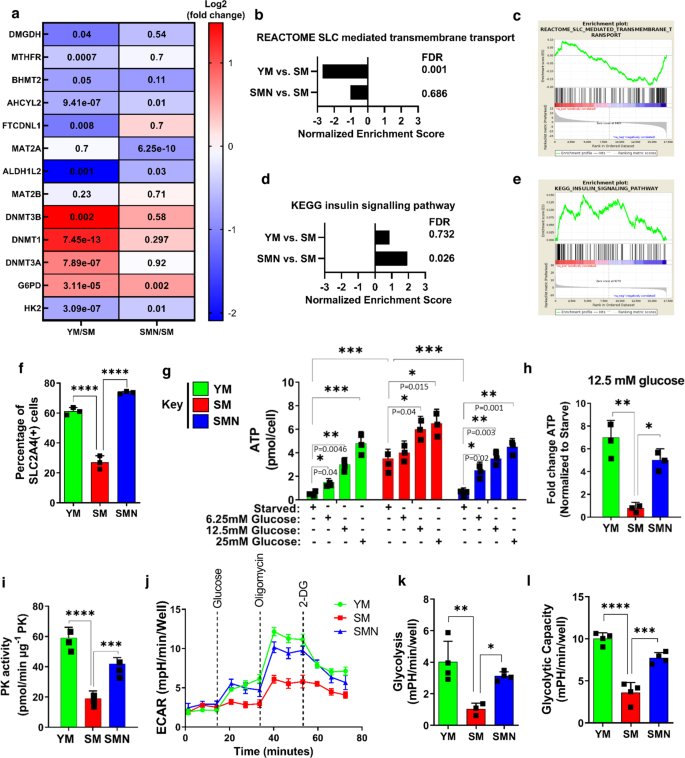
メチオニンアデノシルトランスフェラーゼ2A阻害による代謝の回復で、老化した骨格筋の再生能力と筋力を向上させる。 Methionine adenosyltransferase2A inhibition restores metabolism to improve regenerative capacity and strength of aged skeletal muscle
Nika Rajabian,Izuagie Ikhapoh,Shahryar Shahini,Debanik Choudhury,Ramkumar Thiyagarajan,Aref Shahini,Joseph Kulczyk,Kendall Breed,Shilpashree Saha,Mohamed Alaa Mohamed,Susan B. Udin,Aimee Stablewski,Kenneth Seldeen,Bruce R. Troen,Kirkwood Personius & Stelios T. Andreadis
Nature Communications Published:16 February 2023
DOI:https://doi.org/10.1038/s41467-023-36483-3
Abstract
We investigate the age-related metabolic changes that occur in aged and rejuvenated myoblasts using in vitro and in vivo models of aging. Metabolic and signaling experiments reveal that human senescent myoblasts and myoblasts from a mouse model of premature aging suffer from impaired glycolysis, insulin resistance, and generate Adenosine triphosphate by catabolizing methionine via a methionine adenosyl-transferase 2A-dependant mechanism, producing significant levels of ammonium that may further contribute to cellular senescence. Expression of the pluripotency factor NANOG downregulates methionine adenosyltransferase 2 A, decreases ammonium, restores insulin sensitivity, increases glucose uptake, and enhances muscle regeneration post-injury. Similarly, selective inhibition of methionine adenosyltransferase 2 A activates Akt2 signaling, repairs pyruvate kinase, restores glycolysis, and enhances regeneration, which leads to significant enhancement of muscle strength in a mouse model of premature aging. Collectively, our investigation indicates that inhibiting methionine metabolism may restore age-associated impairments with significant gain in muscle function.
グルタミン酸分解の阻害は老化幹細胞のミトコンドリア機能を回復させる。 Inhibition of glutaminolysis restores mitochondrial function in senescent stem cells
Debanik Choudhury, Na Rong, Izuagie Ikhapoh, Nika Rajabian, Georgios Tseropoulos, Yulun Wu, Pihu Mehrotra, Ramkumar Thiyagarajan, Aref Shahini, Kenneth L. Seldeen , Bruce R. Troen, Pedro Lei, Stelios T. Andreadis
Cell Reports Published: November 29, 2022
DOI:https://doi.org/10.1016/j.celrep.2022.111744

Highlights
- •Overactivated glutaminolysis leads to increased urea production in senescent cells
- •Loss of urea transporter leads to urea accumulation causing mitochondrial dysfunction
- •JNK pathway positively regulates GLS1 expression
- •Inhibiting GLS1 improves mitochondrial function and ameliorates aging hallmarks
Summary
Mitochondrial dysfunction, a hallmark of aging, has been associated with the onset of aging phenotypes and age-related diseases. Here, we report that impaired mitochondrial function is associated with increased glutamine catabolism in senescent human mesenchymal stem cells (MSCs) and myofibroblasts derived from patients suffering from Hutchinson-Gilford progeria syndrome. Increased glutaminase (GLS1) activity accompanied by loss of urea transporter SLC14A1 induces urea accumulation, mitochondrial dysfunction, and DNA damage. Conversely, blocking GLS1 activity restores mitochondrial function and leads to amelioration of aging hallmarks. Interestingly, GLS1 expression is regulated through the JNK pathway, as demonstrated by chemical and genetic inhibition. In agreement with our in vitro findings, tissues isolated from aged or progeria mice display increased urea accumulation and GLS1 activity, concomitant with declined mitochondrial function. Inhibition of glutaminolysis in progeria mice improves mitochondrial respiratory chain activity, suggesting that targeting glutaminolysis may be a promising strategy for restoring age-associated loss of mitochondrial function.

