2023-08-01 東京大学
発表のポイント
- 東京大学発の核酸アプタマー選抜技術”MACE®-SELEX法”で獲得したDNAアプタマー”M08s-1″がもつ、DNAアプタマー史上最高の抗血液凝固活性の要因を明らかにしました。
- M08s-1がもつ極めて珍しい”分子内屈曲構造”が、高い抗血液凝固活性を示す要因であることを発見しました。
- 創薬分野における MACE®-SELEX 法の利用拡大が期待できるとともに、分子標的薬としての核酸アプタマー医薬の研究開発に新たな設計指針を提供します。
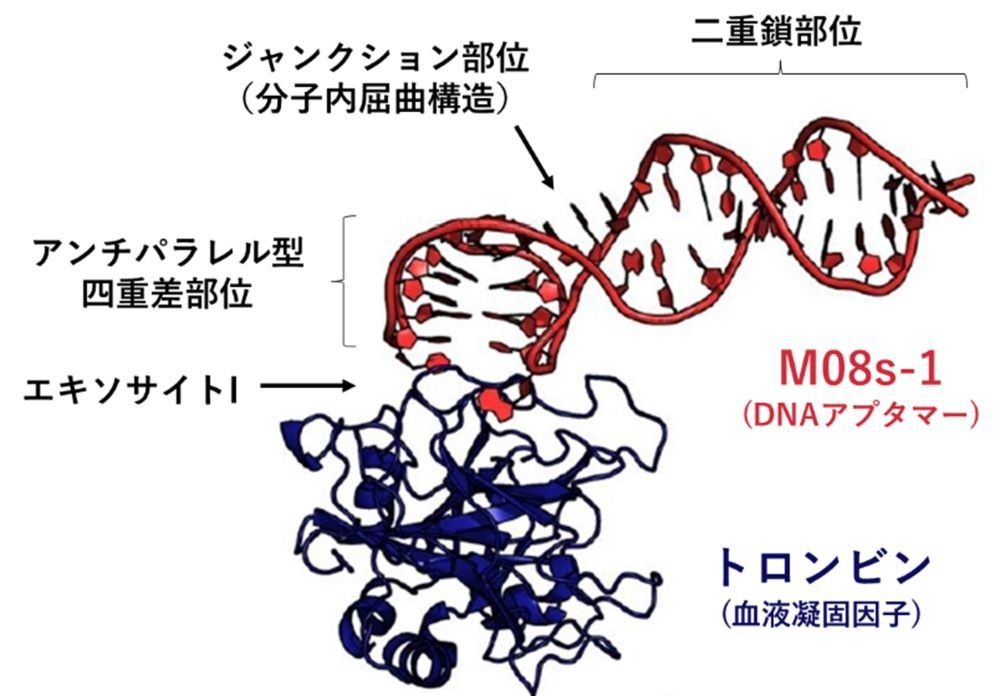
明らかとなった核酸アプタマーM08(赤)と血液凝固因子トロンビン(青)との複合体の立体構造
Protein Data Bank ID: 8BW5
発表内容
東京大学大学院総合文化研究科の吉本敬太郎准教授と、フェデリコ2世・ナポリ大学(イタリア)のFilomena Sica 教授、ヘルムホルツセンター・ミュンヘン(ドイツ)のGrzegorz M. Popowiczグループリーダー、株式会社リンクバイオのWaleed Osman研究員らによるグループは、DNAアプタマー史上最高の抗血液凝固活性(以下、抗凝固活性)をもつDNAアプタマー”M08″の立体構造を世界で初めて明らかにしました。
〈研究の背景〉
血液凝固反応が血管内で暴走すると血栓症のリスクが高まります。心筋梗塞、脳梗塞、肺血栓塞栓症に加え、近年では新型コロナウイルス感染症(COVID-19)が血栓症疾患を高確率で引き起こすことなど、血栓症は今まで以上に我々の身近に潜む血液凝固異常疾患です。 血栓症の予防や治療時に用いられる薬剤は抗凝固薬と呼ばれ、生体内の血液凝固因子に結合して血液凝固を抑制する分子からなります。図1は、血液凝固因子の一つであるトロンビンが、基質であるフィブリノーゲンと反応して血液凝固を起こすまでの反応経路です。トロンビンに結合し、トロンビンとフィブリノーゲン間のタンパク質-タンパク質相互作用を阻害する分子は、血液凝固を抑制する分子標的薬として大きなポテンシャルをもちます。
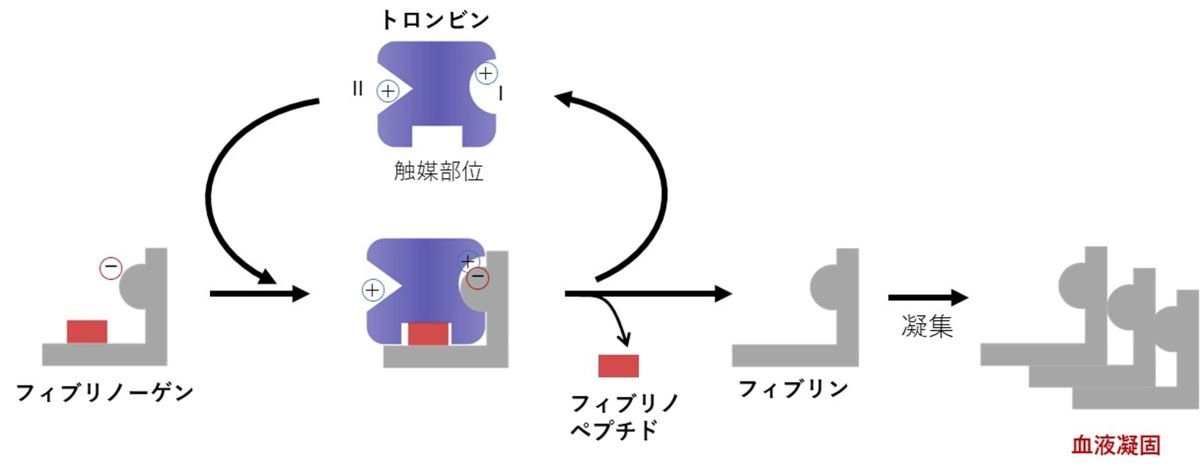
図1:トロンビンとフィブリノーゲンの結合がもたらす血液凝固反応の概略図トロンビンには、カチオン性アミノ酸残基が集中したエキソサイトIとエキソサイトIIの二つの領域が存在します。基質であるフィブリノーゲンはトロンビンに対して触媒部位とエキソサイトIの2箇所で結合し、限定分解を受けた後にフィブリノペプチドとフィブリンが遊離します。遊離したフィブリンは自己凝集し、フィブリンポリマーを形成することで血液凝固を誘起します。フィブリノーゲンとトロンビンの複合体形成を阻害することで、血液凝固の抑制が可能となります。
中分子型分子標的薬の一つである核酸アプタマー(注1)は、分子認識能をもつ一本鎖核酸であり、①製造コストが安価、②輸送・保管時の低温管理が不用、③相補鎖で薬効の停止(中和)が可能、などの特長をもちます。特に③は、抗凝固薬利用時に懸念される出血リスク(注2)を低減することができる核酸アプタマー特有のもので、安全性の高い血栓症治療の開発に繋がります。
東京大学大学院総合文化研究科の吉本准教授らの研究グループは、2019年当時、独自に開発した核酸アプタマー選抜技術(MACE®-SELEX法・注3)を用いてトロンビンに対する10個のDNAアプタマー群”Mシリーズ”の獲得に成功しました。さらに、Mシリーズの中から、DNAアプタマー史上最高の抗凝固作用を示すM08を発見しましたが、M08が示す高い抗凝固活性の要因は不明のままでした。
〈研究の内容〉
本研究では、トロンビンと抗凝固アプタマーM08s-1(M08の塩基配列から不要な部分を取り除いて短くしたアプタマー)との相互作用を、X線結晶構造解析、NMR、円偏光二色性スペクトル測定、ゲル電気泳動分析、分子間相互作用解析などを用いて調査し、M08がもつ極めて高い抗凝固活性の要因が、分子内の屈曲構造にあることを突き止めました。
まず、円偏光二色性スペクトル測定とゲル電気泳動分析の結果から、溶液中でM08s-1は四重鎖構造(注4)をもち、パラレル型とアンチパラレル型の2種類の四重鎖構造が共存する平衡状態にあることがわかりました。さらに結晶構造解析の結果から、アプタマーはトロンビンのエキソサイトI領域に結合すること、トロンビンと結合するアプタマーの構造はアンチパラレル型の四重鎖であることが明らかとなりました(図2)。M08の構造をもう少し詳しく説明するため、M08 の塩基配列情報と立体構造をそれぞれ図3Aと3Bに示します。M08は、四重鎖部位(図3C・青)、二重鎖部位(図3D・緑)、さらに四重鎖部位と二重鎖部位をつなぐジャンクション構造(図3E・ピンク)の3つで構成されることが明らかとなりました。
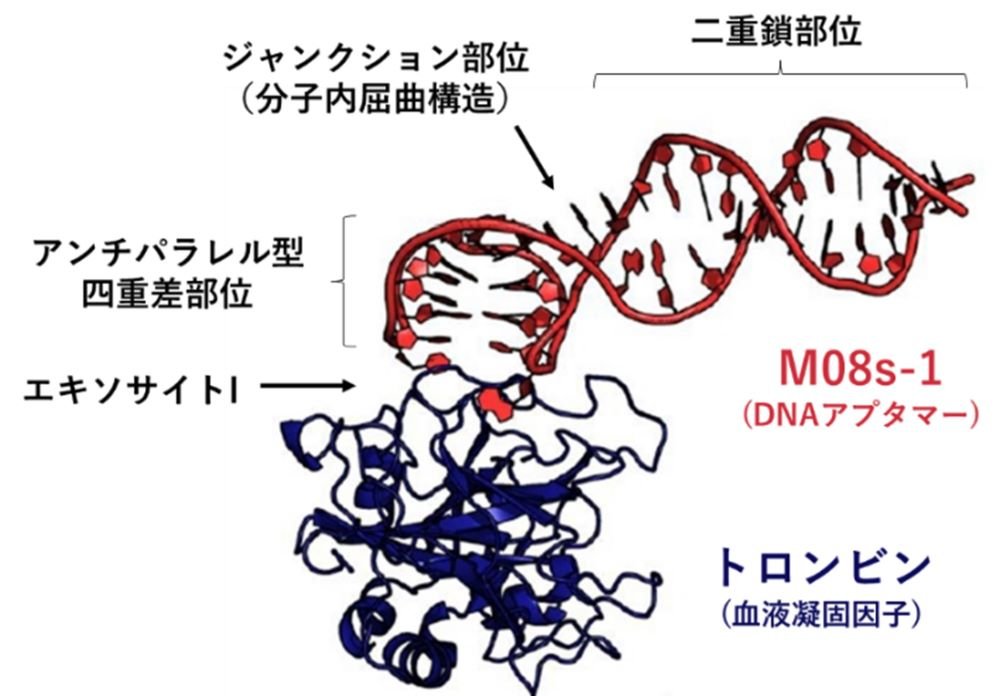
図2:核酸アプタマーM08(赤)と血液凝固因子トロンビン(青)との複合体の立体構造M08は四重鎖部位と二重鎖部位からなり、NU172やRE31などの既報DNAアプタマーと同様に四重鎖構造部位でトロンビンのエキソサイトIに結合することが明らかとなった(図3参照)。Protein Data Bank ID: 8BW5
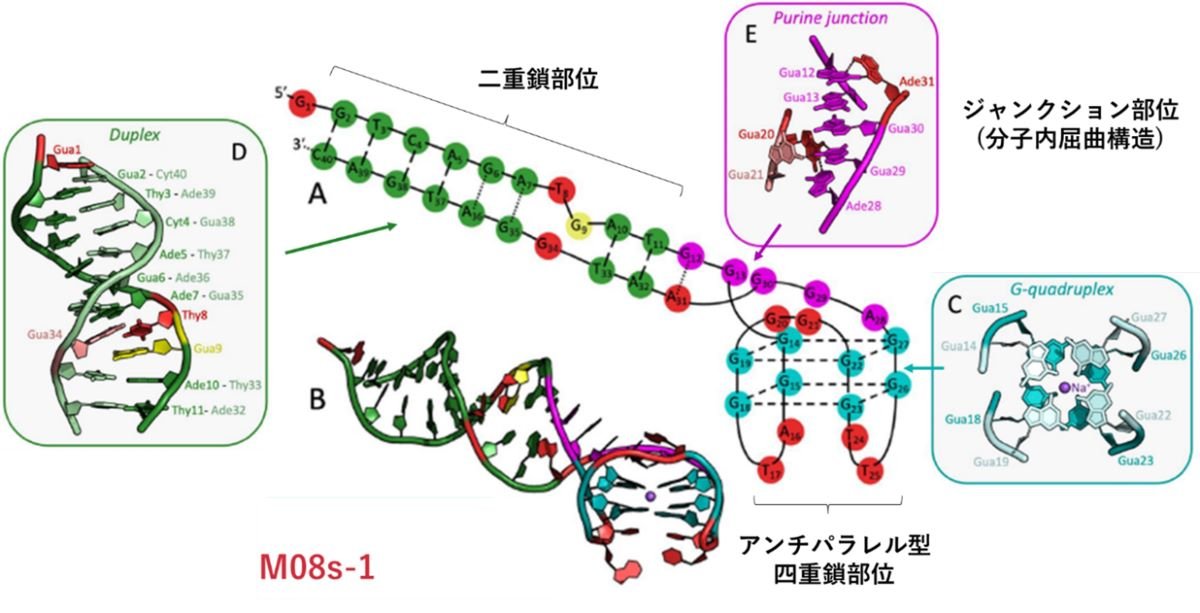
図3:トロンビン結合性DNAアプタマー M08s-1 の立体構造の詳細(A)塩基配列と立体構造の概略図 (B)結晶構造 (C)四重鎖部位におけるGカルテット構造 (D)二重鎖部位 (E)四重鎖部位と二重鎖部位をつなぐジャンクション部位(ここに屈曲構造がある)
M08以外にも、トロンビンのエキソサイトIに結合するアンチパラレル型四重鎖型のDNAアプタマーは過去に報告されています。例えばRE31やNU172などがあり、M08s-1と同様に四重鎖構造部分と二重鎖構造部分をもつDNAアプタマーであることが、結晶構造解析の結果から明らかとなっています。これらのアプタマーとM08s-1との決定的な相違点は、二重鎖部位の空間的配置の違いにあることが本研究により明らかとなりました。図4Aと4Bに、RE31とトロンビンとの複合体(黄色)、NU172とトロンビンとの複合体(青色)をそれぞれM08s-1(赤色)と重ね合わせた結果を示します。RE31、NU172、M08s-1の四重鎖部位はエキソサイトIに結合するため全て重なっていますが、二重鎖の配置が大きく異なっていることがわかります。RE31やNU172の二重鎖はトロンビンの上方向に伸びる形でトロンビンの分子表面から遠いところに位置していますが、M08s-1がもつ二重鎖はRE31やNU172の二重鎖より長く、またトロンビンの右上方向に位置しており、トロンビン表面にある触媒部位に近いところに位置しています。分子間相互作用の解析結果から、NU172とM08s-1のトロンビンに対する結合親和性はほぼ同じであることがわかっていることから、NU172とM08s-1で発現する抗凝固活性の差は、基質であるフィブリノーゲンのトロンビンの活性部位への接近し易さの差により発現することが示唆されました。M08s-1がもつ二重鎖部位の独特な空間的配置は、四重鎖部位と二重鎖部位をつなぐ屈曲したジャンクション構造(図3E)にあり、同部位の屈曲がM08やM08s-1の高い抗凝固活性を生み出している要因であることが明らかとなりました。
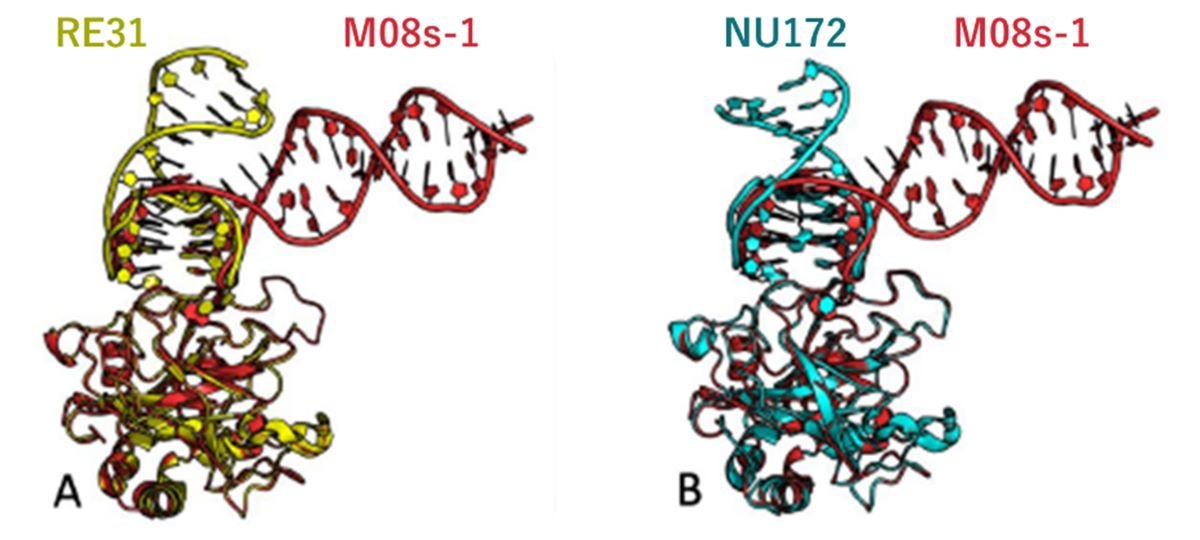
図4:M08s-1と(A)RE31-トロンビン複合体との重ね合わせ図および(B)NU172-トロンビン複合体との重ね合わせ図トロンビンンに結合しているRE31(黄色)とNU172(青色)の四重鎖と二重鎖部位は図の上方向を向いているが、M08s-1(赤色)の四重鎖部位と二重鎖部位は図の右方向に屈曲しているため、トロンビンの触媒活性部位に近い位置に二重鎖部位が位置するある。
〈今後の展望〉
本研究の成果から、分子内に屈曲構造をもたせることでトロンビン結合性DNAアプタマーの抗凝固活性を向上させることができる、という新たな分子設計指針が得られました。1992年に初めてHD1と呼ばれる15の塩基配列からなるトロンビン結合性DNAアプタマーが SELEX 法(注5)で発見されて以降、様々な配列をもつトロンビン結合性アプタマーが獲得・報告されてきました。RE31とNU172は、二重鎖部位を導入し四重鎖構造の熱力学的安定性を高めることで、HD1の抗凝固活性を向上させるために開発されたDNAアプタマーです。多くの研究者がトロンビンに対するDNAアプタマーの獲得に挑戦・成功してきたにもかかわらず、HD1の発見から四半世紀が経過した2019年にMACE®-SELEX法を用いて史上最高の活性をもつM08が発見されたことはとても興味深く、核酸アプタマー選抜法としてMACE®-SELEX法がこれまでの選抜法と一線を画する手法であることを意味しています。
今回の研究成果から、創薬分野における MACE®-SELEX 法の利用拡大が期待できるとともに、分子標的薬としての核酸アプタマー医薬の研究開発に新たなアプローチを提供します。
〈関連のURL〉
「教養学部報645号:核酸アプタマーと事業化」(2023/5/8)
https://www.c.u-tokyo.ac.jp/info/about/booklet-gazette/bulletin/645/open/645-7-02.html
「東京大学大学院総合文化研究科:バイスペシフィックアプタマーを用いる抗体に依存しない抗がん剤検出法の開発」(2023/01/23)
https://www.c.u-tokyo.ac.jp/info/news/topics/20230123000000.html
発表者
東京大学 大学院総合文化研究科
吉本 敬太郎(准教授)
長野 正展(研究当時:特任助教)〈現:田辺三菱製薬 研究員〉
和久井 幸二(学術専門職員)
フェデリコ2世・ナポリ大学
Filomena Sica(教授)
Romualdo Troisi(博士研究員)
Emanuele Rossitto1(博士研究員)
ヘルムホルツセンター・ミュンヘン
Grzegorz M. Popowicz(グループリーダー)
Valeria Napolitano(博士研究員)
株式会社リンクバイオ
Waleed Osman(研究員)
論文情報
雑誌:Nucleic Acids Research(オンライン版:7月28日付)
題名:Steric hindrance and structural flexibility shape the functional properties of a guanine-rich oligonucleotide
著者:Romualdo Troisi, Valeria Napolitano, Emanuele Rossitto, Waleed Osman, Masanobu Nagano, Koji Wakui, Grzegorz M. Popowicz, Keitaro Yoshimoto and Filomena Sica*
DOI:10.1093/nar/gkad634
研究助成
本研究は、厚生労働省・国立研究開発法人日本医療研究開発機構(AMED)の令和2年度創薬基盤推進研究事業「血液凝固因子を標的とする中和可能な核酸アプタマー創薬基盤技術の開発」(課題番号22ak0101130h0003)、日本学術振興会・科研費・学術変革領域研究(B)「精密高分子による次世代医薬開拓」(課題番号:JP22H05049)、公益財団法人・先進医薬研究振興財団の支援により実施されました。
用語説明
(注1)核酸アプタマー:
標的分子に対して結合親和性をもつ核酸分子の総称。DNAからなるDNAアプタマー、RNAからなるRNAアプタマーなどがある。
(注2)抗凝固薬利用時に懸念される出血リスク:
抗血液凝固薬は、血液の凝固過程に関与する血液凝固因子の働きを阻害することで、血液凝固を抑制します。この結果、血液が通常よりも長い時間で凝固せず、血管からの出血が持続しやすくなります。外傷や手術などがなくても、内臓や粘膜などの組織内で微小な損傷が生じることがあります。通常、血液凝固機構によってこれらの出血は迅速に止まりますが、抗血液凝固薬を使用していると、慢性的な出血がおこり、重篤な症状を引き起こす可能性が高まります。
(注3)MACE®-SELEX法:
吉本准教授らが開発した、微粒子支援型キャピラリー電気泳動法(micro-beads assisted capillary electrophoresis: MACE)を導入した核酸アプタマー選抜法(systematic evolution of ligands by exponential enrichment)のことで、従来のSELEX法よりも効率よく複数の核酸アプタマーを獲得する分子進化工学的手法。現在、米国、日本、中国、台湾、で特許が成立しており、株式会社リンクバイオで同手法を用いる核酸アプタマー探索サービスを提供している(詳細:(株)リンクバイオウェブサイト、フナコシ(株)ウェブサイト)。参考文献は以下の通り。
参考文献 (1) Analytical Chemistry, 94 (49), 17255-17262 (2022).
参考文献 (2) ChemBioChem, 22, 3341-3347 (2021).
参考文献 (3) Analytical Sciences, 35, 585-588 (2019).
参考文献 (4) Molecular Therapy Nucleic Acids, 16, 348-359 (2019).
(注4)核酸の四重鎖構造:
核酸の四重鎖構造は、DNAやRNAなどが形成する特殊な高次構造で、パラレル型とアンチパラレル型が存在します。パラレル型は、四重鎖を形成する四つの塩基配列の向きが同じですが、アンチパラレル型は逆方向を向いています。四重鎖構造は、細胞内の特定の遺伝子や制御領域で見られ、遺伝子の調節やゲノムの熱力学的な安定性に重要な役割を果たすと考えられています。核酸アプタマーの中には、四重鎖構造をもつものが多く発見されています。
(注5)SELEX法:
核酸アプタマー選抜法(Systematic Evolution of Ligands by Exponential enrichment, SELEX)は、特定のターゲット分子に高い結合親和性をもつ核酸(DNAまたはRNA)の配列を「選抜」するための分子進化工学的実験手法です。同手法は1990年代初頭にアメリカの化学者ラリー・ゴールドとジャック・ショスタクによって開発されました。

