2023-12-11 マックス・プランク研究所
◆最新の研究では、Rasと呼ばれるがん関連のタンパク質を標的にした新しいProtacが開発され、これにより独自のリガーゼを利用してより効果的な治療が期待されます。この手法は将来的に他のタンパク質や組織にも拡大され、がん治療の進展に寄与する可能性があります。
<関連情報>
- https://www.mpg.de/21238538/1211-moph-new-way-to-force-pathogenic-proteins-into-degradation-151445-x1
- https://www.nature.com/articles/s41467-023-43657-6
医薬品に類似した天然物由来のDCAF11リガンド化学型の発見 Discovery of a Drug-like, Natural Product-Inspired DCAF11 Ligand Chemotype
Gang Xue,Jianing Xie,Matthias Hinterndorfer,Marko Cigler,Lara Dötsch,Hana Imrichova,Philipp Lampe,Xiufen Cheng,Soheila Rezaei Adariani,Georg E. Winter & Herbert Waldmann
Nature Communications Published:30 November 2023
DOI:https://doi.org/10.1038/s41467-023-43657-6
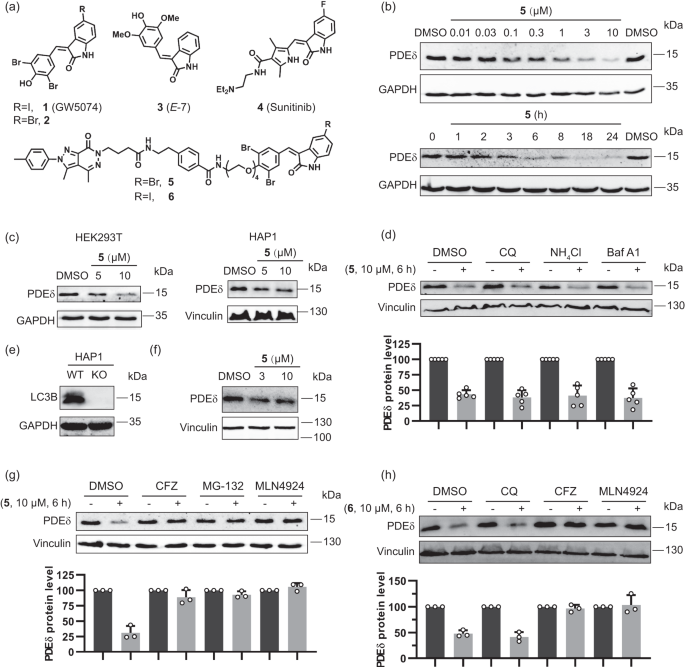
Abstract
Targeted proteasomal and autophagic protein degradation, often employing bifunctional modalities, is a new paradigm for modulation of protein function. In an attempt to explore protein degradation by means of autophagy we combine arylidene-indolinones reported to bind the autophagy-related LC3B-protein and ligands of the PDEδ lipoprotein chaperone, the BRD2/3/4-bromodomain containing proteins and the BTK- and BLK kinases. Unexpectedly, the resulting bifunctional degraders do not induce protein degradation by means of macroautophagy, but instead direct their targets to the ubiquitin-proteasome system. Target and mechanism identification reveal that the arylidene-indolinones covalently bind DCAF11, a substrate receptor in the CUL4A/B-RBX1-DDB1-DCAF11 E3 ligase. The tempered α, β-unsaturated indolinone electrophiles define a drug-like DCAF11-ligand class that enables exploration of this E3 ligase in chemical biology and medicinal chemistry programs. The arylidene-indolinone scaffold frequently occurs in natural products which raises the question whether E3 ligand classes can be found more widely among natural products and related compounds.