2020-10-12 九州大学,日本医療研究開発機構
研究概要
今から約160年前、グリア細胞(※1)の一つであるアストロサイトは神経と神経のすき間を埋めるものと考えられ、長らくその役割は不明のままでした。しかし近年になり、アストロサイトは神経の働きに大切な細胞であることが分かりはじめ、病気にも深い関わりを有することが徐々にわかってきました。脳や脊髄は多くの場所で区分けされており、神経の種類と役割もそれぞれで異なります。それでは、脳や脊髄全体に分布しているアストロサイトも、神経のようにそれぞれの場所で種類と役割が違うのでしょうか?
九州大学大学院薬学研究院ライフイノベーション分野・薬理学分野の津田誠主幹教授、高露雄太特任助教、松田烈士大学院生(当時)、吉原康平大学院生らの研究グループは、皮膚の感覚信号を脳へ伝える脊髄の後角という場所の「表層」に他の層とは違うアストロサイトサブセット(※2)が存在することを世界で初めて発見しました。さらに、この細胞を刺激すると痛覚過敏を起こすことを明らかにしました(※3)。しかし不思議なことに、このアストロサイトは、これまで痛みを抑えるとされてきた下行性ノルアドレナリン神経(青斑核から脊髄に投射する)で刺激されることがわかりました。また、このアストロサイトサブセット選択的にノルアドレナリン神経シグナルを抑制したマウス(※4)では、カプサイシン(※5)による痛覚過敏反応が顕著に抑制されました。すなわち、これまで痛みを抑える作用が常識であったノルアドレナリン神経に、まったく逆の作用があることがこのアストロサイトの発見により明らかとなったのです(図1)。
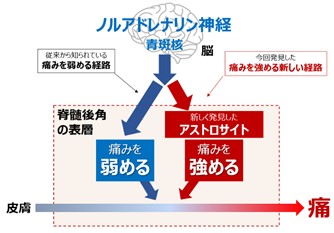
鎮痛薬として処方されるデュロキセチンは下行性ノルアドレナリン神経に作用すると考えられています。もし今回の発見が本当であれば、このアストロサイトの働きを弱めることで、デュロキセチンの鎮痛作用を高めることができるはずと考え、私たちはこの仮説を検証することにしました。その結果、アストロサイトでのノルアドレナリン作用を弱めたマウスでは、確かにデュロキセチンの鎮痛作用が高まることを実証しました。
今回の研究で、私たちは新しいアストロサイトサブセットを発見し、その細胞の研究から新しい痛覚制御メカニズムを明らかにしました。この成果により、鎮痛薬のポテンシャルを効率よく引き出す新しい医薬品の開発に繋がることが期待されます。
本研究成果は、2020年10月5日(月)(米国時間)に米国科学誌「Nature Neuroscience」でオンライン公開されました。
発表論文
- 雑誌名
- Nature Neuroscience(2020年10月5日(米国時間)にオンライン版掲載)
- タイトル
- Spinal astrocytes in superficial laminae gate brainstem descending control of mechanosensory hypersensitivity
- 著者
- Yuta Kohro*, Tsuyoshi Matsuda*, Kohei Yoshihara*, Keita Kohno, Keisuke Koga, Ryuichi Katsuragi, Takaaki Oka, Ryoichi Tashima, Sho Muneta, Takuya Yamane, Shota Okada, Kazuya Momokino, Aogu Furusho, Kenji Hamase, Takumi Oti, Hirotaka Sakamoto, Kenichiro Hayashida, Ryosuke Kobayashi, Takuro Horii, Izuho Hatada, Hidetoshi Tozaki-Saitoh, Katsuhiko Mikoshiba, Verdon Taylor, Kazuhide Inoue, Makoto Tsuda** (* Equal contributors, **Corresponding author)
- DOI
- 10.1038/s41593-020-00713-4
研究支援
本研究は、科学研究費補助金(基盤研究(S)JP19H05658、挑戦的研究(萌芽)JP19K22500、若手研究JP18K14821)、日本医療研究開発機構(AMED)・革新的先端研究開発支援事業(代表:上口裕之)JP20gm0910006、AMED・免疫アレルギー疾患実用化研究事業JP17ek0410034、AMED・創薬等ライフサイエンス研究支援基盤事業JP20am0101091(※3)・JP20am0101120(※4)、中冨健康科学振興財団助成金、内藤記念科学振興財団助成金等からの支援を受けて行われたものです。
補足説明
(※1)グリア細胞は神経系を構成する非神経細胞です。これまでは神経細胞を補佐する細胞とされてきましたが、近年は神経活動や神経疾患に大きく関与することが次々と報告され、世界の注目を集めています。
(※2)転写因子HES5を発現するアストロサイトサブセット。本研究では、同サブセットの解析を主にHes5-CreERT2マウス(共同研究者のVerdon Taylor教授(バーゼル大学)から提供)を用いて行いました。
(※3)AMED創薬等ライフサイエンス研究支援基盤事業・ケミカルシーズ・リード探索ユニット(ライブラリー・スクリーニング領域)での九州大学の研究課題「グリーンファルマを基盤にした創薬オープンイノベーションの推進」(代表:大戸茂弘JP20am0101091)の支援を受け、新規アストロサイトサブセットの刺激による新しい疼痛評価モデルの開発に成功しました。
(※4)AMED創薬等ライフサイエンス研究支援基盤事業・バイオロジカルシーズ探索ユニット「次世代型疾患モデル動物作出」(代表:畑田出穂JP20am0101120)からの支援を受け、群馬大学・畑田出穂教授らの研究グループが作製したAdra1a-FLマウスを使用しました。
(※5)カプサイシンはトウガラシの辛みの主成分で、一次求心性痛覚神経に発現する興奮性イオンチャネルTRPV1タンパク質を刺激して痛みを発生させます。
お問い合わせ先
研究内容に関すること
九州大学大学院薬学研究院薬理学分野
主幹教授 津田誠
九州大学 広報室
AMED事業に関する連絡先
日本医療研究開発機構(AMED)創薬事業部 医薬品研究開発課
創薬等ライフサイエンス研究支援基盤事業(BINDS)