2024-12-12 金沢大学,科学技術振興機構
金沢大学 ナノ生命科学研究所(WPI-NanoLSI)/医薬保健研究域附属サピエンス進化医学研究センターの奥田 覚 准教授と同 大学院新学術創成研究科 ナノ生命科学専攻 博士前期課程2年/ナノ精密医学・理工学卓越大学院プログラム履修者の寺西 亜生らの共同研究グループは、上皮シートの折り目がL字金具のようなアクチン分子の集積構造によって不可逆的に作られる仕組みを解明しました。
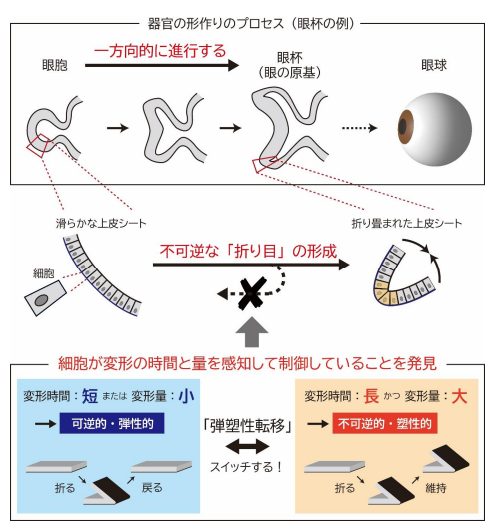
私たちの身体が作られる発生の過程において、シート状の上皮組織(以下、上皮シート)がまるで折り紙のように複雑に折り畳まれることで、各器官の「形」が作られます。この過程で重要なのは、上皮シートに「折り目」が一度形成されるとそれが元に戻らないという不可逆性を持つ点です。もし、この折り目が元に戻ると、複雑な形状が単純なシートに戻ってしまい、正常な器官の構造が形成できなくなってしまいます。そのため、この折り目の不可逆性は、身体や器官が正しく形作られるために不可欠な性質といえます。ところが、これまで生物学の歴史において、この「形が元に戻らない」という現象は当然の事実として捉えられ、その仕組みについては長い間、不明のままでした。
本研究グループは、この折り目の不可逆性を計測するための新しい実験装置を開発し、培養した上皮シストや脊椎せきつい動物の目の元となる眼杯がんぱいのオルガノイド、マウス胚の眼組織に適用しました。その結果、上皮シートの折り目が不可逆となる過程は、加えられた変形の「時間」と「変形量」によって、スイッチのように変化することを、初めて明らかにしました。さらに、その仕組みは、加えられた変形の時間と変形量を細胞が感知して、L字金具のような「アクチンブラケット」構造を形成することで実現されることも発見しました。
これらの結果は、器官の形が不可逆に作られる根本的な仕組みを示しており、発生・再生現象の理解に加え、組織工学・再生医療分野において貢献が期待されます。
本研究成果は、2024年12月12日(英国時間)に英国科学誌「Nature Communications」に掲載される予定です。
本研究は、文部科学省 「世界トップレベル研究拠点プログラム(WPI)」および「卓越大学院プログラム(WISE program)-金沢大学 ナノ精密医学・理工学卓越大学院プログラム-」、科学技術振興機構(JST) 「戦略的創造研究推進事業 CREST」(JPMJCR1921)、日本医療研究開発機構(AMED) 「再生・細胞医療・遺伝子治療実現加速化プログラム-幹細胞・再生医学イノベーション創出プログラム-」(23bm0704065h0003)、日本学術振興会 科学研究費助成事業(21H01209、21KK0134、22K18749、22H05170、24H01398、24H01937)の支援を受けて実施されました。
<プレスリリース資料>
- 本文 PDF(941KB)
<論文タイトル>
- “Epithelial Folding Irreversibility is Controlled by Elastoplastic Transition via Mechanosensitive Actin Bracket Formation”
- DOI:10.1038/s41467-024-54906-7
<お問い合わせ先>
<研究に関すること>
奥田 覚(オクダ サトル)
金沢大学ナノ生命科学研究所(WPI-NanoLSI)/
医薬保健研究域附属サピエンス進化医学研究センター 准教授
<JST事業に関すること>
沖代 美保(オキシロ ミホ)
科学技術振興機構 戦略研究推進部 ライフイノベーショングループ
<報道担当>
金沢大学 先端科学・社会共創推進機構 特任准教授 山崎 輝美(ヤマザキ テルミ)
金沢大学 ナノ生命科学研究所 事務室 今永 藤子(イマナガ フジコ)
科学技術振興機構 広報課