2026-03-30 京都大学
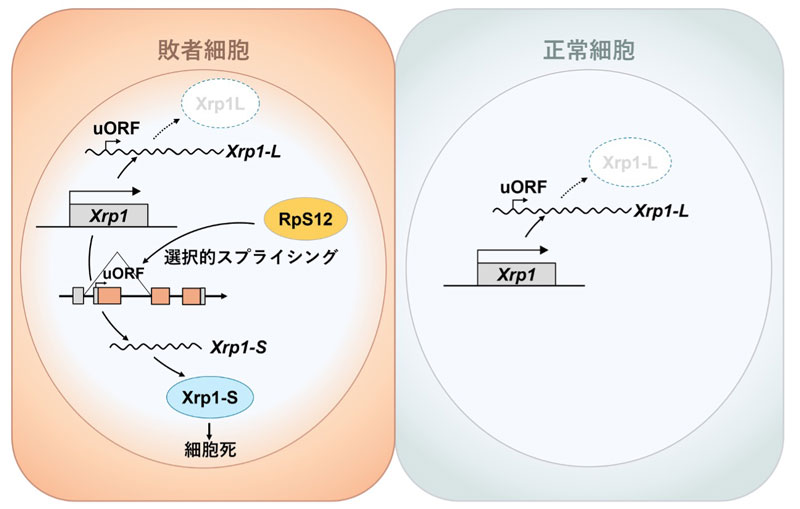
本研究で明らかとなった不良細胞が決まる仕組みのモデル(京都大学 作成:掛村文吾 京都大学大学院生命科学研究科システム機能学分野)
<関連情報>
- https://www.kyoto-u.ac.jp/ja/research-news/2026-03-30-1
- https://www.kyoto-u.ac.jp/sites/default/files/2026-03/web_2603_Kakemura-2d106af3bef872bacb519b35d45202e8.pdf
- https://www.cell.com/cell-reports/fulltext/S2211-1247(26)00233-0
細胞の適応度はリボソームタンパク質RpS12を介した短鎖型Xrp1の誘導によって決定される Cellular fitness is determined by ribosomal protein S12-mediated release of a truncated Xrp1
Bungo Kakemura ∙ Hiroshi Kanda ∙ Ryo Matsumoto ∙ … ∙ Makoto Matsuyama ∙ Yasuhiro Murakawa ∙ Tatsushi Igaki
Cell Reports Published:March 25, 2026
DOI:https://doi.org/10.1016/j.celrep.2026.117155
Highlights
- Xrp1, a key determinant of cell competition, is upregulated post-transcriptionally
- Xrp1 mRNA is abundantly expressed, but its translation is inhibited by upstream ORF
- Unfit cells cause splicing-mediated skipping of Xrp1 uORF via ribosomal protein S12
- uORF skipping of Xrp1 mRNA generates a truncated Xrp1 protein that causes cell death
Summary
Multicellular tissues require continuous optimization to maintain their integrity by eliminating viable but unfit cells through cell competition. During this process, unfit “loser” cells upregulate the C/EBP-family transcription factor Xrp1, which drives their elimination and thus determines cellular fitness. However, the mechanism underlying Xrp1 upregulation remains unclear. Here, we show that Xrp1 is upregulated through a post-transcriptional mechanism mediated by ribosomal protein S12 (RpS12). Although Xrp1 mRNA is abundantly expressed in wild-type cells, its translation is repressed by an upstream open reading frame (uORF) in the 5′ UTR. In unfit cells, RpS12 promotes splicing-mediated skipping of the uORF-containing exon, enabling the use of an alternate start codon that produces a short Xrp1 isoform triggering cell death. Structural analysis reveals strong similarity between RpS12 and the spliceosomal component SNU13, suggesting a direct role for RpS12 in alternative splicing. Our findings provide mechanistic insight into how cellular fitness is determined.