2019-08-22 がん研究会,熊本大学,九州大学,理化学研究所
1.概要
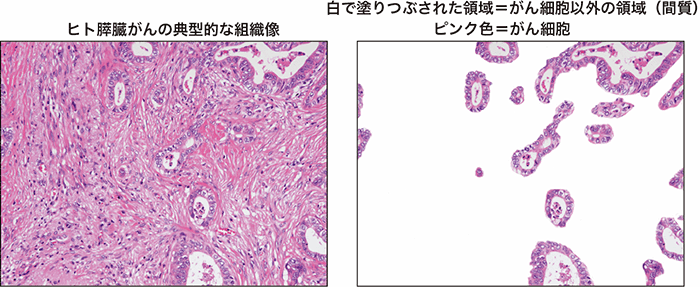
乳がんの約7割は、女性ホルモンのエストロゲンと結合してがんを増殖させるエストロゲン受容体(ER)を多く生産するER陽性型です。そのため、エストロゲンの作用を抑える内分泌療法が効果的ですが、治療中に細胞の中で遺伝子の使われ方が変遷することがあり、その効果がなくなり再発することが問題です。これを解決するために、がんのゲノムDNAの性質、特に立体的な構造を詳細に理解して再発乳がんの特性を読み解くことは、世界的にもまだ新しく、重要な取り組みです。
がん研究会の斉藤典子らの研究グループは、熊本大学、九州大学、理化学研究所らとの共同研究により、長期の内分泌療法中に治療が効かなくなり、再発した乳がんのモデル細胞にて、タンパク質をつくらない非コードRNA分子であるエレノアの役割を調べました。その結果、エレノアは、細胞が死ぬために使うFOXO3遺伝子と増殖のために使うESR1遺伝子(ERをつくるための遺伝子)を立体的に近づけて、どちらも使われるようにしているという、一見相反する現象を明らかにしました。
エレノアを消失させると、近接していた遺伝子同士が離れ、ESR1遺伝子は細胞内で使われなくなりました。その一方で、FOXO3遺伝子は使われたままとなり、その結果、細胞死が誘導されました。これらの結果は、がん細胞が治療環境をかいくぐって増殖するためには、エレノアを使ってゲノムの立体構造を変換し、遺伝子の使い方を変えて細胞死を克服する、という再発乳がんで今まで知られていなかった新しい仕組みを示します。
エレノアをターゲットにした核酸医薬やレスベラトロールは、遺伝子の使われ方のバランスを崩してがん細胞を死の方向に導くため、再発乳がんの治療につながる可能性があります。
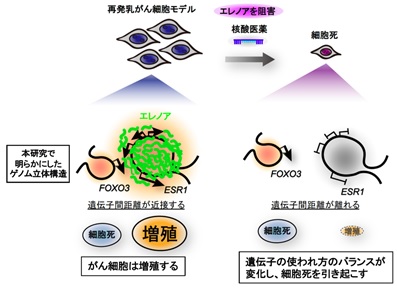
(本研究のまとめ)
本研究の成果は、Nature Publishing Groupオープンアクセス誌Nature Communicationsに、2019年8月 日付で公開されます。
2.ポイント
●ポイント1: 内分泌療法(注1)が効かなくなった再発乳がん細胞は、実は細胞死をおこしやすい脆さを併せ持ちます
●ポイント2: エレノアRNA(注2)は細胞の核の中でゲノムDNAの立体構造をつくり、増殖と細胞死に関わる遺伝子間のバランスをとります
●ポイント3: エレノアを標的とした核酸医薬(注3)やレスベラトロール(注4)は、この増殖と死のバランスを崩し、再発乳がん細胞を細胞死に誘導することから、治療薬としての可能性があります
3.論文名、著者およびその所属
○論文名
The Eleanor ncRNAs activate the topological domain of the ESR1 locus to balance against apoptosis.
○ジャーナル名
Nature Communications (Nature Publishing Groupのオープンアクセス誌)
(※2019年8月22日付でオンラインに掲載されます。)
○著者
Mohamed Osama Ali Abdalla2, Tatsuro Yamamoto1, 2, 3, Kazumitsu Maehara4, Jumpei Nogami4, Yasuyuki Ohkawa4, Hisashi Miura5, Rawin Poonperm5, Ichiro Hiratani5, Hideki Nakayama3, Mitsuyoshi Nakao2*, and Noriko Saitoh1, 2*
* 責任著者
○著者の所属機関
1. 公益財団法人がん研究会がん研究所
2. 国立大学法人熊本大学発生医学研究所
3. 国立大学法人熊本大学大学院生命科学研究部
4. 国立大学法人九州大学生体防御医学研究所
5. 国立研究開発法人理化学研究所生命機能科学研究センター
4.研究の詳細
背景と経緯
乳がんは日本人女性の約11人に1人がかかる、女性の部位別罹患率が第1位のがんであり、患者数は増加傾向にあります。乳がんの約7割は、女性ホルモンのエストロゲンと結合してがんの増殖に働くエストロゲン受容体(ER)を多く生産するER陽性型です。そのため、エストロゲンの作用を抑える内分泌療法が効果的ですが、治療抵抗性を獲得することで、治療効果がなくなり、再発することが問題です(図1)。
内分泌療法が効かなくなったER陽性乳がんを模した細胞では、タンパク質をつくらない非コードRNA分子であるエレノアが、細胞核内に留まった塊の構造体(エレノアクラウド)をつくり、そこで、ERをつくるESR1遺伝子を活性化し、細胞を増殖に導きます。また、再発乳がんモデル細胞に、エストロゲンやその類似薬剤であるレスベラトロールを投与すると、がん細胞が細胞死を引き起こします(図1)。したがって、再発過程で乳がん細胞は、増殖する能力を備えると同時に、細胞死をおこしやすくなる、という脆さも併せ持つようになることが考えられました。そしてこの危うさが治療のヒントになることが期待されましたが、その詳細な仕組みは不明でした。
ゲノムDNAは本来長い紐のような形をしていますが、実際の細胞の核の中では、何層にも複雑に折りたたまれて、立体構造をとっています。近年、染色体コンフォメーション捕捉法と呼ばれる技術により、ゲノムの立体的な位置が明らかになりました。ゲノム領域の2次元的な配置に加え、細胞核内での3次元的な配置が遺伝子の使われ方を決める、といったことも提唱され始めています。
ゲノムDNAには、タンパク質をつくるRNAと、つくらない非コードRNAが記述されています。最近になって、エレノアを含む様々な非コードRNAが、がんに関わることが明らかになり、治療の標的となることが期待されていますが、そのためにはそれぞれの働きを明らかにすることが必要です。
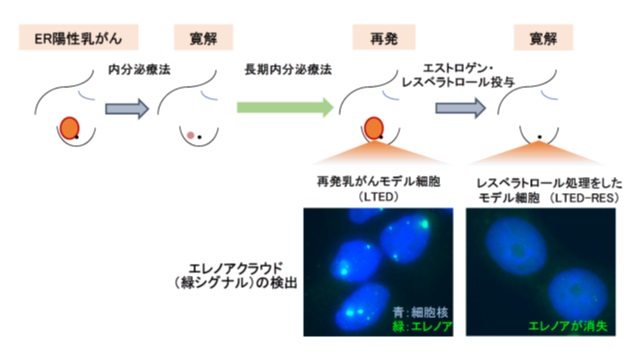
(図1)
研究内容
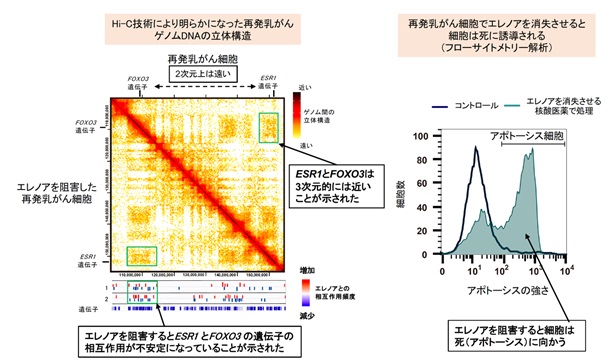
本研究者らは、治療が効かなくなったER陽性再発乳がんのモデル細胞(LTED細胞)を用いて、エレノアを阻害し、染色体コンフォメーション捕捉法を用いてゲノム立体構造を解析し、同時に遺伝子の使われ方を調べるRNA-Seq解析を行いました。その結果、再発乳がん細胞では、細胞死に関わるFOXO3遺伝子がさかんに使われており、あたかも細胞は死ぬ準備ができているようでした。しかし、FOXO3遺伝子ゲノム領域には、増殖に関わるESR1遺伝子ゲノム領域がエレノアにとり囲まれる形で近接し、両者が一緒に活性化していることが分かりました。そこで、エレノアを阻害する薬剤であるレスベラトロールを投与した細胞(LTED-RES細胞)を観察したところ、エレノアによって近接していた2つのゲノム領域の距離は不安定となることで離れ、ESR1遺伝子は使われなくなり、しかしFOXO3遺伝子は使われたままとなり、その結果、細胞死を引き起こしました(図2)。
同様に、エレノアを標的とした核酸医薬の効果も調べました。核酸医薬の投与は、レスベラトロール処理と同様の効果を認めました。エレノアが消失し、FOXO3遺伝子とESR1遺伝子のゲノム領域間が離開し、細胞は死に誘導されました(図2)。核酸医薬を用いた治療は、現在注目されている次世代の抗がん剤であり、レスベラトロール処理よりも特異的にエレノアを阻害することができるため、副作用などが少ないことが予想されます。このため、今後期待できる治療薬になり得る可能性があります。
(図2)
まとめ
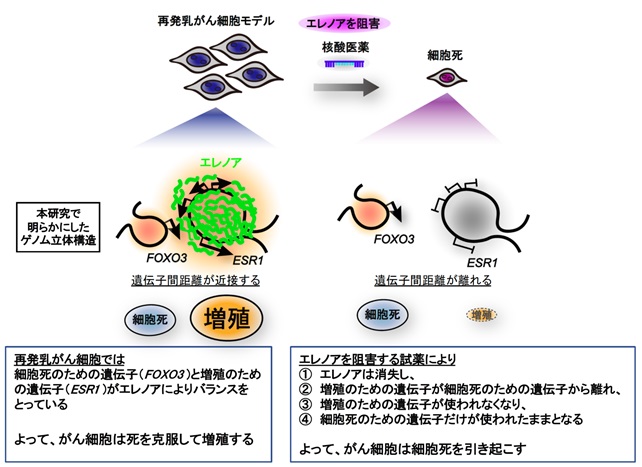
これらの結果から、再発乳がん細胞の中では、内部で進展する細胞死を克服して増殖し続けるために、細胞核内でエレノアがゲノムDNAの立体構造を操っていることが分かりました(図3)。増殖と死に関わる遺伝子の活性化のバランスが増殖に傾いた状態を崩すことが治療の鍵であり、核酸医薬などRNAを標的とした治療薬の可能性を示しました。なお、本研究は、培養細胞株における基礎研究であり、未だ再発乳がん患者を直接に調べたものではありません。
(図3)
5.本研究への支援
本研究は、下記機関より資金的支援等を受けて実施されました。
・文部科学省科学研究費補助金・新学術領域研究「遺伝子制御の基盤となるクロマチンポテンシャル」他
・科学研究費補助金基盤研究、挑戦的研究
・JST (科学技術振興機構) CREST
・AMED (革新的先端研究開発支援事業) CREST
・武田報彰医学研究助成
・内藤記念科学研究助成
・車両競技公益資金記念財団研究助成
・三菱財団研究助成金
6.用語解説
(注1)内分泌療法
乳がんの増殖に必要な女性ホルモン、エストロゲンの作用を抑制する薬剤を用いた治療。
(注2)エレノアRNA
再発乳がんで大量に生産される、タンパク質をつくらない非コードRNA分子。 細胞核内に留まり、乳がんの増殖に関わる遺伝子、ESR1遺伝子を活性化する。
(注3)核酸医薬
非コードRNA等の分子を標的とした、DNAやRNAといった核酸を利用した治療薬。 次世代の医薬品として高い期待が寄せられている。
(注4)レスベラトロール
ポリフェノールの一種でエストロゲンと類似構造を持ちエストロゲン様の働きをする。