2020-07-29 筑波大学,熊本大学,日本医療研究開発機構
研究成果のポイント
- 糖鎖の特徴的な構造を解析する新しい糖鎖プロファイリング技術を用い、皮膚の老化に伴って幹細胞の糖鎖修飾パターンが変化することを発見しました。
- 老化型の糖鎖パターンを持つ皮膚幹細胞では、細胞の増殖が顕著に低下しました。
- 糖鎖を標的にした皮膚幹細胞の老化状態の検出や老化の制御へとつながることが期待されます。
概要
国立大学法人筑波大学生存ダイナミクス研究センターの佐田亜衣子助教(研究当時、現国立大学法人熊本大学国際先端医学研究機構特任准教授)、柳沢裕美教授、国立研究開発法人産業技術総合研究所細胞分子工学研究部門の舘野浩章研究グループ長らの研究グループは、糖鎖プロファイリング技術を用いて、老化皮膚において、幹細胞表面の糖鎖構造(糖鎖修飾パターン)が変化することを見出しました。
細胞表面に存在する糖鎖は、「細胞の顔」とも呼ばれるように、細胞の種類や状態によって構造が劇的に変化することが知られています。血液型や腫瘍マーカーをはじめ、糖鎖の違いは優れたバイオマーカーとしても幅広く利用されてきました。しかし、細胞の中でも、分化細胞を生み出す組織幹細胞注1は、成体組織の全細胞の1パーセント以下に過ぎず、微量のサンプルしか得られないため、糖鎖解析を行うことは困難でした。本研究は、「レクチンアレイ法」という新しい技術を使うことで、糖鎖構造を高感度かつ迅速に検出し、加齢に伴って起こる皮膚幹細胞の糖鎖変化を捉えることに成功しました。本成果は、幹細胞の糖鎖を標的とした新たな老化対策やバイオマーカーの創出へとつながることが期待されます。
本研究の成果は、Aging Cell誌に2020年7月18日付でオンライン公開されました。
本研究は、日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(PRIME、研究期間:2018-2021年度、研究代表:佐田亜衣子)、科学技術人材育成のコンソーシアム構築事業「次世代研究者育成プログラム」Nanotech CUPAL N.R.Pコース(研究期間:2018-2019年度、研究代表:佐田亜衣子)、三菱財団自然科学研究助成(研究期間:2019年度、研究代表:佐田亜衣子)、中冨健康科学振興財団研究助成金(研究期間:2018年度、研究代表:佐田亜衣子)、住友財団基礎科学研究助成(研究期間:2019年度、研究代表:佐田亜衣子)、ホーユー科学財団助成事業(研究期間:2018年度、研究代表:佐田亜衣子)の支援を受けて実施しました。
研究の背景
組織幹細胞は、生涯にわたって増殖しながら分化細胞を生み出す能力を持った細胞です。このような細胞が、私たちの体の中のいろいろな場所に存在するので、古い細胞が失われても、日々新しい細胞を作り出すことができます。例えば、皮膚の新陳代謝や髪の毛の生え替わりは、皮膚幹細胞によって支えられています。また、最近の研究では、身体の加齢変化の一因として、分化細胞の供給源である組織幹細胞の老化(ステムセルエイジング)注2が提唱されています。しかし、その実態については未解明な部分が多くあります。皮膚においても、幹細胞老化の研究が進んでいますが、老化状態を検出するバイオマーカーが同定されておらず、老化制御のための標的因子についてもほとんど分かっていません。
一方、細胞の表面にあるタンパク質や脂質は、糖鎖注3による修飾を受けています。糖鎖は、細胞が生体内のシグナルを受け取ったり、細胞同士がコミュニケーションをしたりするときに重要であると言われています。組織幹細胞においても、この糖鎖が重要な役割を果たすと考えられますが、皮膚から少数の幹細胞を単離し、複雑な糖鎖構造(糖鎖修飾パターン)を解析するのは技術的に困難とされていました。
研究内容と成果
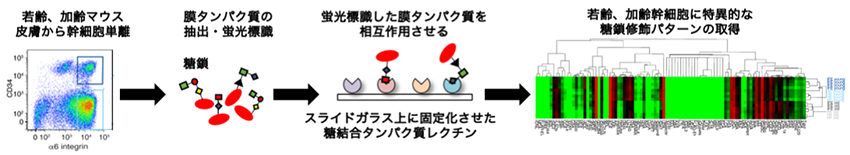
本研究では、「レクチンアレイ法」という新しい技術を用いることで、若いマウス、歳をとったマウスの皮膚から単離した幹細胞の糖鎖修飾パターンを網羅的に解析しました。具体的には、糖結合タンパク質であるレクチン注4をスライドガラス上に固定化し、幹細胞の膜タンパク質と結合させることで、幹細胞の糖鎖構造を高感度かつ迅速に検出します(図1)。
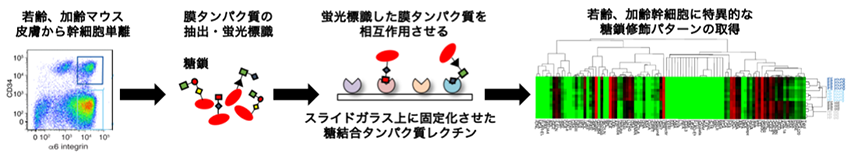 図1 レクチンアレイ法を用いた幹細胞の糖鎖プロファイリング若齢・加齢マウスよりセルソーターを用いて皮膚幹細胞を単離し、レクチンアレイ法を用いた糖鎖解析を行う。糖結合タンパク質であるレクチンをスライドガラス上に固定化し、細胞から抽出、蛍光標識した膜タンパク質をガラス上のレクチンと相互作用させることで、細胞表面に存在する糖鎖構造を高感度かつ迅速に検出することができる。この技術により加齢した皮膚幹細胞で有意に結合が変化するレクチンを同定した。
図1 レクチンアレイ法を用いた幹細胞の糖鎖プロファイリング若齢・加齢マウスよりセルソーターを用いて皮膚幹細胞を単離し、レクチンアレイ法を用いた糖鎖解析を行う。糖結合タンパク質であるレクチンをスライドガラス上に固定化し、細胞から抽出、蛍光標識した膜タンパク質をガラス上のレクチンと相互作用させることで、細胞表面に存在する糖鎖構造を高感度かつ迅速に検出することができる。この技術により加齢した皮膚幹細胞で有意に結合が変化するレクチンを同定した。
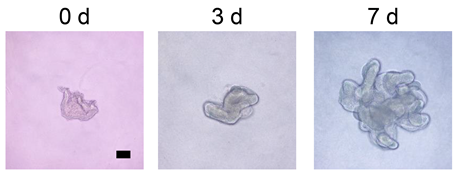
これにより、皮膚幹細胞における糖鎖のパターンをプロファイルしました。その結果、加齢に伴い、皮膚幹細胞の糖鎖修飾パターンがダイナミックに変化する「グライコームシフト」が起こることを発見しました(図2)。グライコームシフト後の老化型糖鎖パターンを持つ皮膚幹細胞では、細胞の増殖が顕著に低下することから、糖鎖の変化は機能的にも重要であることを示しました。また、加齢に伴って有意に変化する糖類(マンノース、α2-3シアル酸)をそれぞれ認識する糖結合タンパク質であるレクチン(rHeltuba、rGal8N)を同定し、これらが新たな老化バイオマーカーになり得る可能性を見出しました。
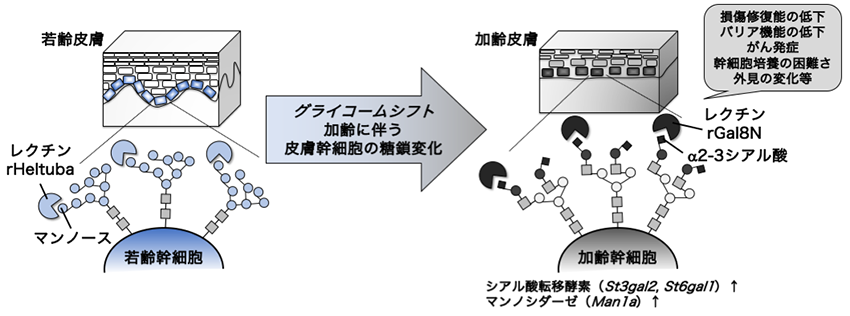 図2 皮膚幹細胞の加齢に伴う糖鎖変化に着目した老化の理解と制御皮膚幹細胞の加齢に伴い、高マンノース型(図2左)からシアル酸に富んだ複合型(図2右)へと、糖鎖修飾パターンがダイナミックに変化する「グライコームシフト」が起こる。またシアル酸の付加に働く糖転移酵素注5(St3gal2、St6gal1)、およびマンノースの分解に働く酵素(Man1a)は、加齢した皮膚幹細胞では有意に発現が上昇する。若齢幹細胞に存在するマンノース、および加齢幹細胞に存在するα2-3シアル酸をそれぞれ認識する糖結合タンパク質としてレクチン(rHeltuba、rGal8N)を同定し、新たな老化バイオマーカーとしての可能性を見出した。
図2 皮膚幹細胞の加齢に伴う糖鎖変化に着目した老化の理解と制御皮膚幹細胞の加齢に伴い、高マンノース型(図2左)からシアル酸に富んだ複合型(図2右)へと、糖鎖修飾パターンがダイナミックに変化する「グライコームシフト」が起こる。またシアル酸の付加に働く糖転移酵素注5(St3gal2、St6gal1)、およびマンノースの分解に働く酵素(Man1a)は、加齢した皮膚幹細胞では有意に発現が上昇する。若齢幹細胞に存在するマンノース、および加齢幹細胞に存在するα2-3シアル酸をそれぞれ認識する糖結合タンパク質としてレクチン(rHeltuba、rGal8N)を同定し、新たな老化バイオマーカーとしての可能性を見出した。
今後の展開
老化予防の観点から、老化状態を早い段階で予測できるようなバイオマーカーや、老化制御のための標的分子の同定が求められています。
なぜ老化した皮膚幹細胞で糖鎖が変化するのか?その生物学的意義や分子機構には未だ不明な点が多く残されています。今後、糖鎖を介した幹細胞老化の原因を究明することで、糖鎖をターゲットとした老化制御へとつながっていくことが期待されます。
用語解説
- 注1 組織幹細胞
- 成体幹細胞とも呼ばれる。成体の臓器や組織において、自己複製能(自分自身を長期的に増やす能力)と分化能(分化・成熟した細胞を産生する能力)を兼ね備えた細胞。組織の再生や損傷修復を担う。このうち、皮膚の新陳代謝や毛の生えかわり、傷の修復を担う細胞が皮膚幹細胞。
- 注2 幹細胞老化(ステムセルエイジング)
- 加齢に伴って、組織の大元の細胞である幹細胞自身が機能低下や破綻を起こし、老化の原因となっているという説。
- 注3 糖鎖
- 糖が複雑に連なった鎖状の物質。細胞表面の糖鎖は、がんや免疫、幹細胞の機能などに重要である。解析が難しいため、未知の部分も多い。
- 注4 レクチン
- 糖鎖と結合するタンパク質。複雑な糖鎖構造を検出するバイオツールとして注目されている。
- 注5 糖転移酵素
- 糖鎖の合成を行う酵素。糖の種類に特有な糖転移酵素の働きによって糖が付加され、複雑な糖鎖の構造が作られる。
掲載論文
- 題名
- Glycome profiling by lectin microarray reveals dynamic glycan alterations during epidermal stem cell aging
(糖鎖プロファイリング技術を用いた加齢に伴う皮膚幹細胞の糖鎖変化の解明) - 著者名
- Lalhaba Oinam, Gopakumar Changarathil, Erna Raja, Yen Xuan Ngo, Hiroaki Tateno, Aiko Sada, Hiromi Yanagisawa
- 掲載誌
- Aging Cell
- DOI:
- 10.1111/acel.13190
お問い合わせ先
佐田亜衣子(さだあいこ)
熊本大学 国際先端医学研究機構 特任准教授
筑波大学 生存ダイナミクス研究センター 客員准教授
柳沢裕美(やなぎさわひろみ)
筑波大学 生存ダイナミクス研究センター 教授
国立研究開発法人日本医療研究開発機構
シーズ開発・研究基盤事業部 革新的先端研究開発課