2020-09-11 理化学研究所
理化学研究所(理研)環境資源科学研究センター天然物生合成研究ユニットの高橋俊二ユニットリーダー、ケミカルバイオロジー研究グループの長田裕之グループディレクターらの共同研究グループは、放線菌[1]の二次代謝産物[2]である「リベロマイシンA(RM-A)[3]」生産が、「β-カルボリン[4]誘導体」の添加によりLuxRファミリー[5]転写因子[6]を介して増強されるメカニズムを見いだしました。
本研究成果は、類似の転写因子に制御される遺伝子群を活用した新しい天然化合物の創出につながると期待できます。
放線菌は、医薬・農薬などに用いられる有用生理活性化合物の宝庫として知られています。これまでのゲノム解析によって、30以上の二次代謝生合成遺伝子クラスターが発見されていますが、その多くは休眠遺伝子クラスターです。二次代謝生合成遺伝子クラスターの活性化機構を解明することは、創薬シーズとなり得る新しい天然化合物を創出する上で重要です。
共同研究グループはこれまでに、β-カルボリン誘導体(BR-1)を添加して放線菌Streptomyces sp. SN-593を培養すると、RM-A生産が増強されることを報告しています。今回、BR-1がLuxRファミリー転写因子(RevU)に結合することによって、revU遺伝子上流のプロモーター[7]領域への結合を促進し、RM-A生合成遺伝子クラスター全体の発現を増強することを明らかにしました。さらに、BR-1は、異種の放線菌二次代謝物の生産も増強することを発見しました。
本成果は、オンライン科学雑誌『Scientific Reports』(6月23日付)に掲載されました。
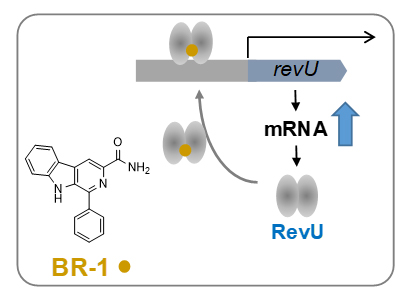
推定されるLuxRファミリー転写因子(RevU)の発現増強機構
背景
放線菌は、医薬品、農薬、抗生物質など、構造多様性を持つ有用な二次代謝産物を生産することが知られています。微生物二次代謝物の生産誘導機構を解明し、放線菌ゲノム中に存在する生合成遺伝子クラスターを活性化する手法を開発することは、新たな天然化合物の創出や、有用化合物の高生産において重要といえます。また、微生物二次代謝物は、土壌中の生物間相互作用やケミカルシグナルに応答して生産されると考えられています。化合物による二次代謝産物の生産誘導機構を解明することは、自然界の微生物応答の理解にもつながると期待されます。
放線菌Streptomyces sp. SN-593は、「リベロマイシンA(RM-A)」を生産します。これまでに共同研究グループは、理研NPDepo化合物ライブラリー[8]を用いてスクリーニングを行い、RM-A生産を増強する化合物を特定しました。また、構造活性相関研究によって、低濃度でRM-A生産を増強する「β-カルボリン誘導体(BR-1)」の作製にも成功しています(図1)注1)。
本研究では、BR-1が二次代謝物の生産を増強するメカニズムの解明を試みました。
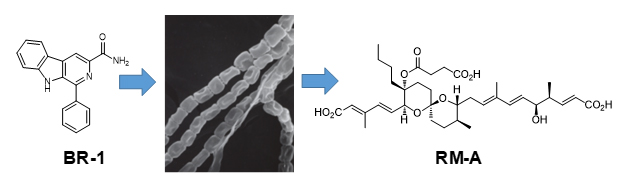
図1 BR-1添加による放線菌二次代謝物RM-Aの生産増強
放線菌Streptomyces sp. SN-593にβ-カルボリン誘導体(BR-1)を低濃度で添加すると、リベロマイシンA(RM-A)生産が増強される。
注1)Panthee S, Takahashi S, et.al. β-carboline biomediators induce reveromycin production in Streptomyces sp. SN-593 Sci. Rep. volume 9, Article number: 5802 (2019)
研究手法と成果
共同研究グループはまず、Streptomyces sp. SN-593のゲノム解読情報をもとに、BR-1存在下と非存在下で全RNA発現解析を行いました。その結果、21個の遺伝子から構成されるRM-A生合成遺伝子クラスターの発現が有意に増加し、LuxRファミリー転写因子(RevU)をコードするrevU遺伝子発現の増加も確認できました(図2)。また、RM-A生産性を失ったrevU遺伝子破壊株では、BR-1存在下でも生産性を回復できないことが分かりました。
次に、BR-1とRevUの相互作用を調べるため、放線菌内で転写因子RevUを発現させ、粗抽出液を調製した後、BR-1結合ビーズと混合しました。電気泳動により結合タンパク質分離し、得られた単一のバンドをMALDI-TOF/MS分析[9]したところ、標的はRevUであることが判明しました。
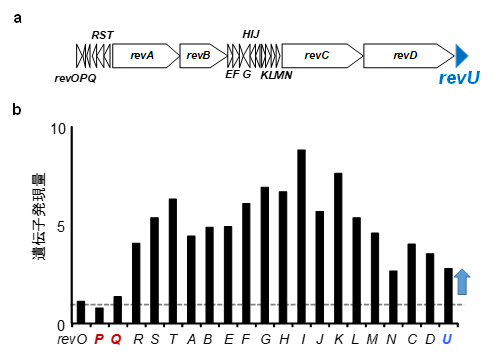
図2 BR-1によるRM-A生合成遺伝子クラスターの発現増強
a)RM-A生合成遺伝子クラスター。全長は91キロ塩基で、revA~revUの21個の遺伝子から構成される。
b)BR-1添加後に誘導されるRM-A生合成遺伝子。LuxRファミリー転写因子(RevU)の遺伝子発現が上昇していることが確認できた。破線はBR-1を添加しないときの発現量。
続いて、revU遺伝子のプロモーター領域へのRevU結合がBR-1によって強化されるかどうかを調べるために、表面プラズモン共鳴(SPR)[10]分析を行いました。ビオチン標識された二本鎖DNA断片をストレプトアビジンというタンパク質でセンサーチップに固定化し、SPRを用いてRevUプロモーター結合活性を評価しました。その結果、濃度1.25マイクロモーラー(μM、1μMは100万分の1モーラー)のBR-1の存在によって、結合活性が増強することが分かりました(図3a)。また、RevUはrevU遺伝子上流に存在するCTG-(N10)-CAG配列を含む遺伝子断片に、濃度依存的に結合することも分かりました。BR-1の最小有効濃度を調べたところ、50%効果濃度(EC50)[11]は182ナノモーラー(nM、1nMは10億分の1モーラー)であり、RM-A生産の増強に必要な濃度(350nM)に近い値でした。さらに、テトラヒドロ型BR-1はRM-A生産を増強しないが、プロモーター領域へのRevU結合も増強しないことが分かりました。
以上の結果から、revU遺伝子の活性化は、BR-1のRevUへの結合によって促進される機構を提唱しました(図3b)。
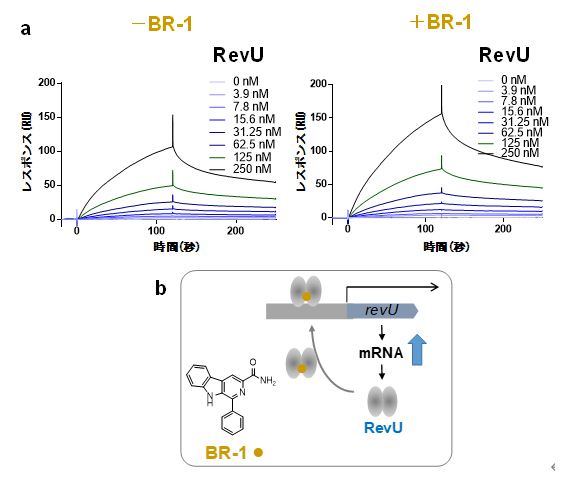
図3 表面プラズモン共鳴を用いた結合解析
a)左はBR-1非存在下、右はBR-1存在下でのRevUのプロモーター結合活性。BR-1(1.25μM)存在時に、結合が促進された。
b)推定されるLuxRファミリー転写因子(RevU)の発現増強機構。BR-1はRevUと結合することで、revU遺伝子の上流のプロモーター領域との結合を促進する。
さらに、BR-1とその誘導体が種の異なる放線菌の二次代謝産物の生産を誘発するか否かを検証しました。その結果、Streptomyces sp. RK95-74からは、ネオメディオマイシンB、Streptomyces sp. RK10-A626からは、m/z[12]が1032~1291の未知の二次代謝物の生産増加に成功しました。
今後の期待
本研究では、β-カルボリン化合物(BR-1)は、転写因子であるRevUと結合し、rev遺伝子クラスターを活性化することで、Streptomyces sp. SN-593におけるRM-A産生を選択的に増強する機構を発見しました。また、BR-1がRM-A生産菌だけでなく、他の放線菌(Streptomyces sp. RK95-74およびStreptomyces sp. RK10-A626)からの二次代謝物の産生を増強することも示しました。今後、BR-1およびその誘導体の処理により、RevUとの相同性が高いLuxRファミリー転写因子を持つ二次代謝生合成遺伝子クラスターを活用した新たな天然化合物の創出が期待できます。
本研究成果は、国際連合が2016年に定めた17項目の「持続可能な開発目標(SDGs)」のうち「3.すべての人に健康と福祉を」に大きく貢献するものです。
補足説明
1.放線菌
土壌中など自然界に広く存在するグラム陽性の真正細菌であり、複雑な構造を持つ二次代謝産物を生産する。人類は、それらの中から、医薬、農薬、動物薬などの生理活性を持つ物質を利用してきた。医薬探索源として重要視されている。
2.二次代謝産物
生物体を構成、維持する上で重要な物質を一次代謝産物、生育に必ずしも必須ではない物質を二次代謝産物と呼ぶ。微生物において、二次代謝産物の生合成に関わる酵素の遺伝子はゲノム中の特定の領域に並んで存在している。
3.リベロマイシンA(RM-A)
放線菌Streptomyces sp. SN-593から単離されたポリケチド化合物。破骨細胞に選択的に取り込まれ、標的分子のイソロイシルtRNA合成酵素の活性を阻害し、タンパク質合成を阻害することで、アポトーシスを誘導する。構造的特徴として、多くの不斉炭素中心を持つスピロアセタール環、トリカルボン酸を有している。
4.β-カルボリン
植物、動物、微生物に広く存在するインドールアルカロイド。
5.LuxRファミリー
Helix-turn-helix構造を持ち、DNAに結合して遺伝子発現を活性化する転写因子ファミリー。
6.転写因子
特定のDNA配列に結合して、遺伝子の発現を制御するタンパク質。
7.プロモーター
mRNA合成の開始に関与するDNA上の特定領域の短い塩基配列のこと。プロモーター領域にRNA合成酵素のRNAポリメラーゼが結合し、転写が始まる。
8.理研NPDepo化合物ライブラリー
天然物化学を基礎とした理研天然化合物バンク。微生物(放線菌、糸状菌など)、植物の二次代謝化合物を精製単離するとともに、天然化合物の誘導体や類縁体、人工合成化合物などを収集して、約4万化合物をライブラリー化したもの。
9.MALDI-TOF/MS分析
マトリクス支援レーザ―脱離イオン化-飛行時間型質量分析。質量分析における試料のイオン化法。MALDI-TOF/MS はmatrix-assisted laser desorption/ionization time-of-flight mass spectrometryの略。
10.表面プラズモン共鳴(SPR)
タンパク質、核酸、低分子化合物など、分子間の相互作用を測定する際に用いられる技術。SPRはsurface plasmon resonanceの略。
11.50%効果濃度(EC50)
薬物の作用が最大値の50%となる濃度。この値が小さいほど効果が強い。
12.m/z
イオンの質量を統一原子質量単位で割った値をイオンの電荷数で割って得られる無次元量を表す記号。
共同研究グループ
理化学研究所 環境資源科学研究センター
天然物生合成研究ユニット
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
基礎特別研究員(研究当時) シュレス・パンテー(Suresh Panthee)
(現 帝京大学 医真菌研究センター 博士研究員)
特別研究員(研究当時) 鬼頭 奈央子(きとう なおこ)
ケミカルバイオロジー研究グループ
研究嘱託 清水 猛(しみず たけし)
研究嘱託(研究当時) 林 輝雄(はやし てるお)
グループディレクター 長田 裕之(おさだ ひろゆき)
国立感染症研究所 真菌部第四室
室長 石川 淳(いしかわ じゅん)
帝京大学 医真菌研究センター
准教授 浜本 洋(はまもと ひろし)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金挑戦的萌芽研究「LALファミリー転写制御因子を活性化する小分子化合物による休眠遺伝子覚醒の新戦略(研究代表者:高橋俊二)」、農芸化学研究企画賞先導的生物活性物質研究と新技術開発「放線菌二次代謝物の生産を増強する小分子バイオメディエーターの開発(研究代表者:高橋俊二)」、農林水産省「農林水産業・食品産業科学技術研究推進事業」および農研機構生研支援センター「イノベーション創出強化研究推進事業」の研究課題「植物保護を目指した天然物ケミカルバイオロジー研究(研究統括:長田裕之)」の支援を受けて行われました。
原論文情報
Suresh Panthee, Naoko Kito, Teruo Hayashi, Takeshi Shimizu, Jun Ishikawa, Hiroshi Hamamoto, Hiroyuki Osada & Shunji Takahashi, “β-carboline chemical signals induce reveromycin production through a LuxR family regulator in Streptomyces sp. SN-593”, Scientific Reports, 10.1038/s41598-020-66974-y
発表者
理化学研究所
環境資源科学研究センター 天然物生合成研究ユニット
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
ケミカルバイオロジー研究グループ
グループディレクター 長田 裕之(おさだ ひろゆき)
報道担当
理化学研究所 広報室 報道担当