皮膚扁平上皮がんに対するマイクロRNA軟膏製剤の実用化へ期待
2020-11-24 東京医科歯科大学,日本医療研究開発機構
ポイント
- がん抑制型マイクロRNA(microRNA:miR)※1であるmiR-634※2を内包した軟膏製剤を開発しました。
- 皮膚扁平上皮がん担がんマウスモデルおよび皮膚化学発がんマウスモデルにおいて、miR-634軟膏製剤の経皮投与により、腫瘍細胞へのmiR-634の送達と抗腫瘍効果が確認されました。
- miR-634は、グルタミントランスポーターASCT2遺伝子※3を標的とすることにより、グルタミン代謝を抑制することを見出しました。
- miR-634軟膏製剤は、EGFR阻害剤の治療効果を増強することを見出しました。
- 上記の成果は、マイクロRNAを用いた新たな核酸抗がん薬の実用化につながることが期待されます。
概要
東京医科歯科大学・難治疾患研究所・分子細胞遺伝分野の井上純准教授、稲澤譲治教授らの研究グループは、(株)メドレックスとの共同研究により、がん抑制型miR-634を内包した“miR-634軟膏製剤”を開発し、皮膚扁平上皮がん担がんマウスモデルおよび皮膚化学発がんマウスモデルを用いて、本製剤による抗腫瘍効果およびEGFR阻害剤との併用効果を確認しました。この研究成果は、国立研究開発法人日本医療研究開発機構(AMED)「次世代がん医療創生研究事業」(P-CREATE)、文部科学省新学術領域研究(15H05908) 「がんシステムの新次元俯瞰と攻略」および文部科学省科学研究費補助金(18K06954、18H02688)の支援のもと遂行され、国際科学雑誌 Molecular Therapy – Oncolytics(モレキュラーセラピー オンコリティックス)に、2020年11月23日にオンライン版で発表されました。
研究の背景
皮膚扁平上皮がんにおいて、外科的切除が不適応な患者に対して、有効な外用剤の開発が強く求められていました。また、皮膚扁平上皮がんでは、Epidermal growth factor receptor(EGFR)遺伝子が高発現しており、EGFR阻害剤の治療適応が期待されています。しかしながら、その治療効果は限定的であるため、EGFR阻害剤による抗腫瘍効果を増強させる新たな治療戦略の開発が必要とされていました。
一方、ヒトマイクロRNA(microRNA:miR)は約22塩基からなる機能性RNAであり、複数の標的遺伝子の転写産物に直接結合することで、遺伝子発現を負に制御する働きがあります。近年、がん抑制的に機能するmiRをがん細胞へ導入する核酸補充療法(miR核酸抗がん薬)は、がん治療における新たなモダリティとして注目されています。これまでに研究グループは、miR-634のがん細胞への導入が、細胞内代謝や細胞生存に関連する複数の遺伝子を同時にかつ直接的に抑制することにより、効率的に細胞死を誘導することを明らかにしました。さらに最近、合成2本鎖miR-634をLNP(lipid nanoparticle)※4に内包したmiR-634-LNP製剤を膵臓がん担がんマウスに全身投与することにより、腫瘍増殖が抑制されることを見出しました。このように、非常に強力な抗腫瘍能力を有する“miR-634”は有用な創薬シーズとなることを示してきました。
研究成果の概要
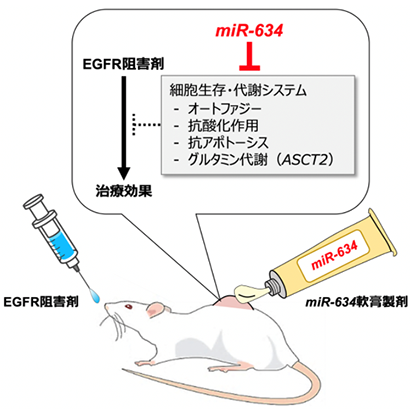
そこで本研究では、合成2本鎖miR-634を内包した“miR-634軟膏製剤”を開発し、皮膚扁平上皮がんに対する新たな外用剤としての有用性を検証することを目的として研究を行いました。初めに、皮膚扁平上皮がん担がんマウスモデルおよび皮膚化学発がんマウスモデルにおいて、miR-634軟膏製剤を経皮投与することにより、腫瘍細胞への<miR-634の効率的な送達と標的遺伝子の発現抑制とともに、顕著な腫瘍増殖の抑制が確認されました。さらに、miR-634は、グルタミントランスポーターASCT2遺伝子を標的とすることにより、グルタミン代謝を抑制することが分かりました。そして、皮膚扁平上皮がん細胞株A431担がんマウスモデルにおいて、miR-634軟膏製剤は、EGFR阻害剤の治療効果を増強することを見出しました(図参照)。
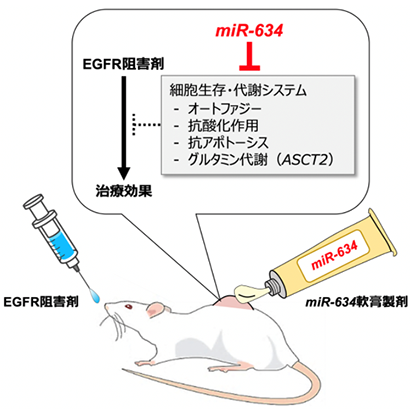
“miR-634軟膏製剤”の経皮投与によるEGFR阻害剤の治療効果の増強
研究成果の意義
がん抑制的に機能するmiRを創薬シーズとして用いたmiR核酸抗がん薬は、分子標的薬と異なり、複数のがん促進分子を同時に標的とできること、さらに、RNAに作用するため、結果的にundruggableとなった低分子化合物や抗体のターゲット分子でも標的とできることから、がん治療における新たなモダリティとして注目されています。本研究では、細胞内代謝および細胞生存システムに関連する複数の遺伝子群を同時に標的とするmiR-634を創薬シーズとして用いた“miR-634軟膏製剤”を開発し、その治療有効性を動物レベルで実証しました。このように、皮膚扁平上皮がんに対する新たな外用剤として、“miR-634軟膏製剤”の実用化が期待されます。
論文情報
- 掲載誌
- Molecular Therapy – Oncolytics
- 論文タイトル
- Improving the efficacy of EGFR inhibitors by topical treatment of cutaneous squamous cell carcinoma with miR-634 ointment
用語解説
- ※1 マイクロRNA(microRNA:miR)
- miRは、標的遺伝子の転写産物に結合することで、遺伝子発現を抑制する約22塩基からなる機能性RNAです。ヒトでは、2,500種類以上のmiRが存在しており、中でもがん抑制機能を有するがん抑制型miRは、核酸抗がん薬の創薬シーズとして期待されています。
- ※2 miR-634
- がん抑制型miRの1つであるmiR-634は、がん細胞へ導入することにより、ミトコンドリア恒常性、オートファジー、抗アポトーシス、抗酸化作用と行ったがん細胞特有の細胞生存や細胞内代謝に関連する遺伝子群の発現を抑制し、細胞死を誘導する。
- ※3 グルタミントランスポーターASCT2遺伝子
- 細胞膜上に存在するタンパク質であり、アミノ酸の1つであるグルタミンの細胞外から細胞内への取り込みに寄与する。
- ※4 LNP(lipid nanoparticle)
- LNPは、薬剤輸送システムの1つであり、イオン化脂質を用いた脂質ナノ粒子です。マイクロRNAをLNP内部に内包することにより、外部環境(血中)における核酸分解から保護され、腫瘍組織へマイクロRNAを安定に輸送することができます。
研究者プロフィール
井上純(イノウエジュン) Jun Inoue
東京医科歯科大学大学 難治疾患研究所 分子細胞遺伝分野 准教授
研究領域:腫瘍生物学
稲澤譲治(イナザワジョウジ) Johji Inazawa
東京医科歯科大学大学 難治疾患研究所 分子細胞遺伝分野 教授
研究領域:腫瘍生物学、人類遺伝学、腫瘍診断学
お問い合わせ先
研究に関すること
東京医科歯科大学大学 難治疾患研究所
分子細胞遺伝分野
稲澤譲治(イナザワジョウジ)
井上純(イノウエジュン)
報道に関すること
東京医科歯科大学 総務部総務秘書課広報係
AMEDに関すること
国立研究開発法人日本医療研究開発機構(AMED)
創薬事業部 医薬品研究開発課