痒みを根元から絶つ新たな治療の実現に期待
2021-05-19 九州大学,日本医療研究開発機構
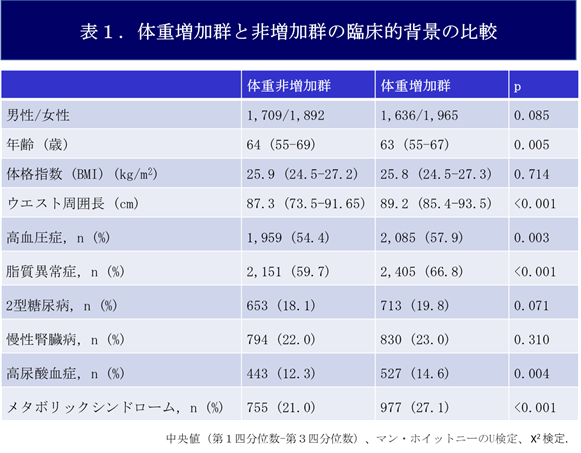
九州大学生体防御医学研究所の福井宣規 主幹教授、宇留野武人 准教授、國村和史 特任助教、同大学大学院医学系学府の上加世田泰久大学院生らの研究グループは、同大学大学院医学研究院の古江増隆 教授、東京大学大学院薬学系研究科の金井求 教授の研究グループとの共同研究により、アトピー性皮膚炎の主要な痒み惹起物質であるIL-31の産生を抑制する低分子化合物を世界に先駆けて開発しました。
アトピー性皮膚炎は国民の7~15%が罹患している国民病であり、痒みに伴い生活の質が著しく損なわれることから、その対策は急務となっています。IL-31は、アトピー性皮膚炎発症に重要な痒み物質で、主にヘルパーT細胞(※1)から産生されます。研究グループはこれまでに、DOCK8という分子がないヒトやマウスにおいてIL-31の産生が亢進し、重篤なアトピー性皮膚炎を自然発症することに着目し、そのヘルパーT細胞で発現する遺伝子を解析することで、IL-31の産生にEPAS1という転写因子(※2)が重要な役割を演じることを明らかにしました。
そこで今回、EPAS1-IL-31経路を標的とした化合物スクリーニングを実施し、DOCK8欠損マウスのヘルパーT細胞におけるIL-31産生を選択的に抑制する化合物として、IPHBAを発見しました。IPHBAは低酸素応答や他のサイトカインの産生には影響を与えませんが、IPHBAをマウスに経口投与すると、IL-31を産生するヘルパーT細胞の移入による引っ掻き行動が抑制されました。同様のIL-31選択的な抑制効果は、アトピー性皮膚炎患者さん由来のヘルパーT細胞においても認められました。そこで、約200の類縁化合物を新たに合成し、構造活性相関を検討することで、IPHBAより薬効の強い化合物の開発に成功しました。
本研究成果は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST及びLEAP)の成果で、2021年4月2日(金)に米国科学雑誌「Journal of Allergy and Clinical Immunology」に掲載されました。
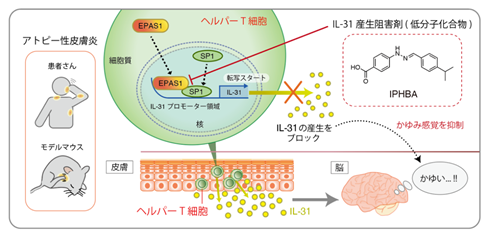
参考図
アトピー性皮膚炎の主要な痒み惹起物質であるIL-31の産生を選択的に抑制する低分子化合物を開発しました。この化合物は、痒みを根元から絶つ新たな治療の実現につながることが期待されます。
背景
痒みは「掻破したい(引っ掻きたい)という衝動を起こさせる不快な感覚」として定義され、生活の質を著しく損なうことから、その対策は重要です。特に、アトピー性皮膚炎は国民の7~15%が罹患している国民病であり、その痒みをコントロールするための創薬ニーズは極めて高いと言えます。これまで、痒み研究はヒスタミン(※3)を中心に進んできましたが、アトピー性皮膚炎の痒みの多くは抗ヒスタミン剤(H1ヒスタミン受容体遮断薬)では抑制されないことから、別の痒み物質の存在が示唆されてきました。このような中、アトピー性皮膚炎と関連した新しい痒み物質として注目されているのがIL-31です。IL-31は主にヘルパーT細胞(※1)から産生され、末梢神経と脊髄を介して脳に痒み感覚を伝えますが、IL-31の産生制御機構そのものは不明でした。
福井主幹教授らはこれまでに、DOCK8という分子がないヒトやマウスにおいてIL-31の産生が亢進し、重篤なアトピー性皮膚炎を自然発症することに着目し、そのヘルパーT細胞で発現する遺伝子を解析することで、IL-31の産生に転写因子EPAS1が重要な役割を演じることを明らかにしました。EPAS1はARNTという転写因子と会合して低酸素応答を制御することが知られていますが、EPAS1によるIL-31の産生誘導にARNTは必要なく、SP1という別の転写因子が関与していました。以上より、EPAS1はIL-31の産生を抑制するための創薬標的になると考えられました(Nature Communications 2017)。
内容
本研究では、東京大学創薬機構より提供された9,600個の化合物を対象にEPAS1-IL-31経路を標的としたスクリーニングを実施しました。その結果、4個のヒット化合物のうちIPHBAと命名した化合物では、T細胞の生存性を損なうことなく、2.5μMという比較的低用量でDOCK8欠損マウスのヘルパーT細胞におけるIL-31の遺伝子発現を抑制しました(図1A)。一方IPHBAは、低酸素応答やIL-2/IL-4といった他のサイトカインの遺伝子発現には影響しませんでした(図1A)。同様の結果は、IL-31とIL-2の産生をタンパク質レベルで測定した場合にも認められました(図1B)。以上より、IPHBAはヘルパーT細胞におけるIL-31産生を選択的に抑制する化合物であることが明らかとなりました。
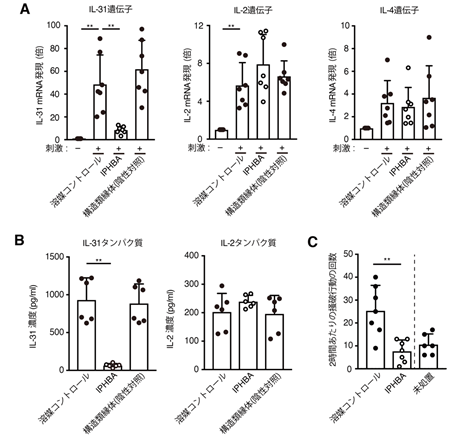
図1 IPHBAはヘルパーT細胞によるIL-31の産生を阻害し、マウスの引っ掻き行動を抑制するA:IPHBAはIL-2やIL-4の遺伝子発現に影響することなく、IL-31の発現を抑制する。
B:IPHBAはIL-2のタンパク質産生に影響することなく、IL-31タンパク質の産生を抑制する。
C:IPHBAの経口投与により、マウスの引っ掻き行動が抑制される。
さらに、IL-31タンパク質を大量に産生することができるヘルパーT細胞をマウスに移入すると、掻破行動(引っ掻き行動)が惹起されます。このマウスにIPHBAを100mg/kgで経口投与すると、ヘルパーT細胞の移入による掻破行動が抑制されました(図1C)。
次に、IPHBAの作用機序を突き止めるためクロマチン免疫沈降法(※4)を用いて解析しました。EPAS1を含む一部の転写因子は、タンパク質複合体を形成することでDNA上のプロモーター領域(※5)に結合し、転写活性を調節することが知られています。そこでEPAS1とSP1の両転写因子に着目したところ、IPHBAを添加するといずれの転写因子もIL-31プロモーター領域への結合が弱まることを見出しました(図2)。また、EPAS1とSP1は複合体を形成しますが、IPHBAはその会合を濃度依存的に抑制することも分かりました。これらのことから、IPHBAはEPAS1とSP1の会合を抑制することで、IL-31プロモーター領域への両転写因子のリクルートメント(動員)を阻害し、IL-31の遺伝子発現を抑制していることが示唆されました。
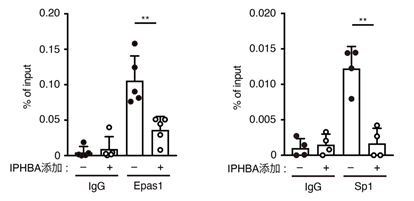
図2 IPHBA添加によりEPAS1とSP1のIL-31プロモーター領域への結合が抑制される
以上の結果はマウスモデルを使った実験であるため、ヒトにも応用できるかどうか検証する必要があります。そこで研究グループは、アトピー性皮膚炎患者さんのご協力を得て血液からヘルパーT細胞を単離し、IPHBAの評価を行いました。アトピー性皮膚炎を発症していない人に比べ、アトピー性皮膚炎患者さんのヘルパーT細胞は大量にIL-31を産生していましたが、IPHBAの添加によってその産生が抑制されることを確認しました(図3左)。IPHBAは、免疫応答全般に重要なIL-2の産生には影響を与えなかったことから(図3右)、免疫抑制作用の少ない治療薬シーズになり得ることが示唆されました。
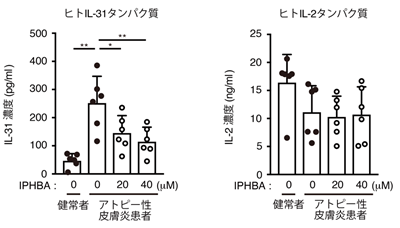
図3 IPHBAはアトピー性皮膚炎患者さん由来のヘルパーT細胞におけるIL-31産生を抑制する一方で、IL-2産生には影響しない
最後に、IPHBAの構造をベースに約200の類縁化合物を合成し、それらの構造活性相関を取得しました。その結果、IL-31の遺伝子発現をより強く抑える化合物の開発に成功しました。
今後の展開
IL-31の発見に伴い、アトピー性皮膚炎の治療の選択肢も広がりつつあります。今回、研究グループは、ヘルパーT細胞によるIL-31の産生を選択的に抑制できる低分子化合物として、IPHBAを発見しました。IPHBAをリード化合物として開発を進めることで、アトピー性皮膚炎の痒みを根元から絶つ新たな治療薬となることが期待されます。
本研究について
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業AMED-CREST「健康・医療の向上に向けた早期ライフステージにおける生命現象の解明」研究開発領域における研究課題「胎児・母体免疫クロストークによる生体恒常性維持と疾患感受性決定の分子基盤」及びLEAPにおける研究課題「DOCKファミリー分子の生体機能と動作原理の解明に基づく革新的医薬品の創出」の研究成果です。
用語解説
- (※1)ヘルパーT細胞
- リンパ球の一種であり、CD4陽性T細胞とも呼ばれる。サイトカインという液性因子を分泌し、B細胞を刺激または補助して抗体の産生を促す機能を有する。
- (※2)転写因子
- DNAに結合し、DNAの遺伝情報をmRNAへと転写する過程を調節するタンパク質。単独、あるいは他のタンパク質と複合体を形成することでこの機能が発揮される。
- (※3)ヒスタミン
- マスト細胞等から放出される化学物質で、アレルギー反応において中心的な役割を演じている。
- (※4)クロマチン免疫沈降法
- 細胞内でのタンパク質-DNA間の相互作用(結合)を解析するための実験方法。目的のタンパク質が結合したDNA断片を、抗体を使用して濃縮・単離する。
- (※5)プロモーター領域
- 転写(DNAからmRNAを合成する段階)の開始に関与する遺伝子の上流領域を指す。この領域に転写因子が結合する。
論文情報
- タイトル
- Targeted inhibition of EPAS1−driven IL-31 production by a small-molecule compound(低分子化合物によるEPAS1誘導性IL-31産生の選択的阻害)
- 雑誌名
- Journal of Allergy and Clinical Immunology
- DOI
- 10.1016/j.jaci.2021.03.029
お問い合わせ先
研究に関するお問い合わせ
九州大学生体防御医学研究所 主幹教授
福井 宣規(ふくい よしのり)
報道に関するお問い合わせ
九州大学 広報室
事業に関するお問い合わせ
(革新的先端研究開発支援事業)
国立研究開発法人日本医療研究開発機構(AMED)
シーズ開発・研究基盤事業部 革新的先端研究開発課