2021-07-16 自然科学研究機構生理学研究所,日本医療研究開発機構
パーキンソン病は手足の動かしにくさ(無動)、震え、こわばりなどの症状を示す進行性の神経難病です。60歳以上では人口100人あたり1人と多くの患者さんがいるため、超高齢社会を迎えた日本にとって大きな医療、社会問題となっています。しかしながら、どのような脳内の神経活動の異常がパーキンソン病の症状を起こすのか、詳しいメカニズムはわかっていませんでした。
今回、自然科学研究機構 生理学研究所の知見聡美助教、南部篤教授、京都大学霊長類研究所の高田昌彦教授の研究チームは、ヒトと同じ霊長類であるニホンザルにパーキンソン病様症状を発症させて、症状と神経活動の関係を詳細に調べることにより、パーキンソン病の症状を引き起こす神経メカニズムを明らかにしました。本研究成果はCerebral Cortex誌(日本時間2021年7月16日午前9時解禁)に掲載されました。
研究の背景
パーキンソン病は、動作の緩慢、手足の震えやこわばり、バランス能力の低下などの運動症状と、うつや不眠などの非運動症状を示す進行性の神経難病です。日本には15万人以上の患者さんがいますが、高齢になるほど罹患率が高くなるため、今後さらに患者数が増加すると予想されています。パーキンソン病は、脳内のドーパミンが不足することにより、大脳基底核と呼ばれる脳領域の神経活動に異常が生じて発症します。しかしながら、大脳基底核におけるどのような神経活動の異常がパーキンソン病の症状を起こすのか、詳しいメカニズムは明らかにされていませんでした。
運動を制御する神経回路
大脳基底核は、運動指令を出す役割を果たす大脳皮質運動野から指令を受け取ります。運動指令は3つの経路によって出力部である淡蒼球内節に伝えられ、運動を制御しています(図1)。大脳皮質運動野を電気的に刺激して運動指令の伝達経路を追うと、正常なサルの淡蒼球内節では、「早い興奮-抑制-遅い興奮」という3相性の神経活動として観察されます(図2左)。「早い興奮」と「遅い興奮」は、それぞれ「ハイパー直接路」と「間接路」と呼ばれる経路を通って伝えられ、運動を抑制する働きを持ちます。一方、「抑制」は「直接路」と呼ばれる経路を通って伝えられ、運動を起こす働きを持ちます。
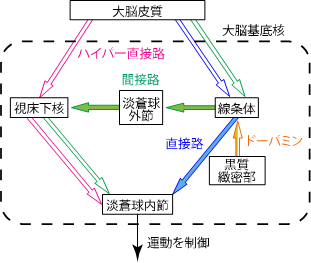
図1 大脳皮質から受け取った運動指令は、3つの経路によって大脳基底核の出力部である淡蒼球内節に伝えられる。
大脳皮質からの運動指令は、ハイパー直接路、直接路、間接路という3つの経路を通って淡蒼球内節に伝えられ、運動を調節します。黒質緻密部の神経細胞が減少してドーパミンが不足すると、パーキンソン病が発症します。白抜き矢印は興奮性、塗りつぶした矢印は抑制性入力を示します。
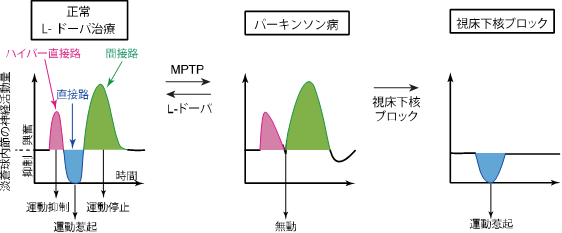
図2 パーキンソン病では、運動を起こすために必要な「直接路」を通る情報が上手く伝わらなくなっている。
大脳皮質運動野を電気的に刺激した際の淡蒼球内節の神経活動。正常では「早い興奮(ピンク)-抑制(青)-遅い興奮(緑)」という3相性の活動が観察されますが(左)、パーキンソン病では「直接路」を通って伝えられる抑制が消失していました(中)。L-ドーパ投与によって治療すると抑制が回復しました(左)。パーキンソン病では運動を起こすために必要な「直接路」を通る情報が上手く伝わらなくなっているため、手足が動かしにくくなる「無動」などの症状が引き起こされると考えられます。さらに視床下核の神経活動を薬でブロックすると、興奮が消失して抑制が回復するとともに(右)、運動症状が改善しました。
今回の研究について
本研究チームは、大脳基底核におけるどのような神経活動の異常がパーキンソン病の症状を起こすのかを明らかにするため、ドーパミン神経細胞を壊す薬剤を投与して、パーキンソン病様症状を発症させたニホンザルを用い、症状と神経活動の関係を詳細に調べました。
パーキンソン病では「直接路」の情報伝達が障害されている
パーキンソン病を発症しているサルの淡蒼球内節で調べてみると、「直接路」で伝えられる「抑制」が消失し、「ハイパー直接路」と「間接路」で伝えられる2相性の興奮が観察されることがわかりました(図2中)。また、パーキンソン病の治療に用いられるL-ドーパという薬を与えて症状が改善している間に調べてみると、抑制が回復し、正常サルと同様な3相性応答が観察されるようになりました(図2左)。これらの結果から、パーキンソン病では、運動を起こすために必要な「直接路」を通る情報が上手く伝わらなくなることにより、手足が動かしにくくなる「無動」の症状が起こると考えられます。一方で、刺激を与えず安静時に淡蒼球内節の神経活動量と活動様式を調べたところ、正常サルとパーキンソン病サルの間で大きな違いは観察されませんでした。
これまでの治療法も「直接路」の情報伝達で説明可能に
また、進行期のパーキンソン病患者さんに対して、視床下核という大脳基底核の別の部位に電極を埋め込み24時間電気刺激を与えることによって神経活動をブロックする脳深部刺激療法や、視床下核の一部を壊す手術が行われていますが、その治療メカニズムは分かっていませんでした。そこで、視床下核に薬を注入して神経活動をブロックすることでヒトの治療時と似た状態にした際、淡蒼球内節の活動がどのようになっているのかを調べました。その結果、視床下核の神経活動をブロックすると、パーキンソン病の症状が改善するとともに、淡蒼球内節の神経活動の興奮が消失して「直接路」を介する抑制が回復することが分かりました(図2右)。これらの結果は、パーキンソン病発症時には「直接路」の情報が弱くなっており、「ハイパー直接路」と「間接路」の情報に埋もれてしまっているが、視床下核をブロックすることにより「ハイパー直接路」と「間接路」の情報がなくなり、埋もれていた「直接路」の情報が見えるようになったことを示しています。つまり、「ハイパー直接路」と「間接路」をブロックすることで、弱まっている「直接路」を通る運動指令の伝達を回復させ、症状を緩和させることができていると考えられます。
南部教授は「これまでの定説では、淡蒼球内節における神経活動量の増加や活動様式の異常によってパーキンソン病の症状が説明されてきましたが、今回の結果は定説とは異なるもので、「直接路」を通る運動指令の伝達が弱まっていることが、より本質的な変化であることを示しています。「直接路」を通る情報伝達を必要なタイミングで補助したり、「ハイパー直接路」や「間接路」を通る情報伝達を弱めたりできれば、パーキンソン病の新たな治療法の開発にもつながると期待できます。」と話しています。
助成金などの必要情報
本研究は文部科学省科学研究費補助金(新学術領域研究「非線形発振現象を基盤としたヒューマンネイチャーの理解(オシロロジー)」、基盤研究)、日本医療研究開発機構(AMED)「革新的技術による脳機能ネットワークの全容解明プロジェクト(革新脳)」「戦略的国際脳科学研究推進プログラム(国際脳)」、科学技術振興機構(JST)CREST「光の特性を活用した生命機能の時空間制御技術の開発と応用(オプトバイオ)」の補助を受けて行われました。
今回の発見
- ヒトと同じ霊長類であるニホンザルにパーキンソン病様症状を発症させ、症状と神経活動との関係を詳細に調べました。
- パーキンソン病では、大脳基底核の「直接路」を通る情報が上手く伝わらなくなっていることが示唆されました。
- パーキンソン病を治療して症状が改善している際には、「直接路」を通る情報伝達が回復していることがわかりました。
- これまでの定説とは異なり、「直接路」を通る運動指令の伝達が弱まっていることが、パーキンソン病におけるより本質的な変化であることを示しました。
- 「直接路」を通る運動指令を回復させることで、パーキンソン病の治療につながる可能性があります。
この研究の社会的意義
「直接路」を通る運動指令の伝達が弱まっていることが、パーキンソン病の症状を引き起こすことがわかりました。「直接路」の情報伝達に上手く介入することにより、パーキンソン病の新たな効果的な治療法を開発できる可能性があります。
論文情報
- 題名
- Altered dynamic information flow through the cortico-basal ganglia pathways mediates Parkinson’s disease symptoms.
- 著者名
- Satomi Chiken, Masahiko Takada, Atsushi Nambu.
- 掲載誌
- Cerebral Cortex.
- 掲載日
- 日本時間2021年7月16日午前9時解禁
お問い合わせ先
研究について
自然科学研究機構 生理学研究所 生体システム研究部門
教授 南部 篤(ナンブ アツシ)
助教 知見 聡美(チケン サトミ)
広報に関すること
自然科学研究機構 生理学研究所 研究力強化戦略室
AMED事業について
日本医療研究開発機構 疾患基礎研究事業部 疾患基礎研究課