2021-07-16 理化学研究所,東京工業大学
理化学研究所(理研)開拓研究本部田中生体機能合成化学研究室の田中克典主任研究員(東京工業大学物質理工学院応用化学系教授)、山本智也基礎科学特別研究員らの研究チームは、金触媒[1]によって構造と性質を大きく変化させる「保護基[2]」を開発しました。
本研究成果は、天然物などの複雑な構造を持った有機化合物の合成に応用可能であるほか、生体内での金触媒反応によるプロドラッグ[3]の活性化やマテリアルの構築への応用が期待できます。
天然物や薬剤などを化学合成する際には、反応性の高い官能基での望まない化学反応を防ぐために保護基を導入します。保護基は特定の試薬を用いて選択的に外すことができるため、官能基を再び活性化し、それぞれの官能基に別々の化学反応を起こすことも可能です。
今回、研究チームは、金触媒によって外すことができる保護基として「2-(2-エチニルフェニル)-2-(5-メチルフラン-2-イル)-エトキシカルボニル基(Epoc基)」を開発しました。一般的な保護基は特定の試薬によって直接外されるのに対し、Epoc基は金触媒の反応により不安定な構造のHmoc基に”変身”することで、温和な条件で外れるようになるのが特徴です。このEpoc基の変身は、生体内環境に似た水中でも効率良く進行します。さらに、複雑な構造を持つ分岐ペプチドの化学合成への応用にも成功しました。
本研究は、科学雑誌『Chemical Science』オンライン版(7月9日付)に掲載されました。
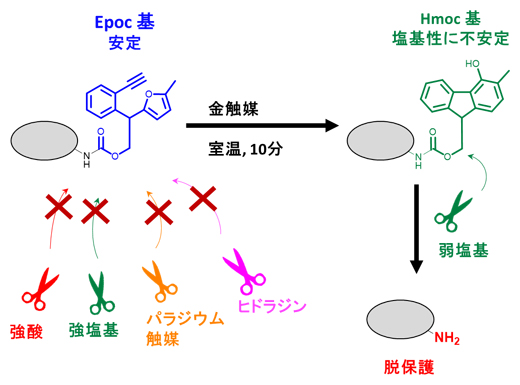
金触媒によって”変身”できるEpoc保護基の開発
背景
複雑な化学構造を持つ天然物や薬剤などの有機化合物を合成する際には、さまざまな官能基に対し、別々の化学反応を起こす必要があります。これを達成するために、これまで官能基に「保護基」を導入する戦略が取られてきました(図1A)。保護基を官能基に導入すると、その反応性を低下させることができ、また特定の試薬によって保護基を選択的に外し、官能基の反応性を復活させることができます。
保護基は官能基の反応性を抑えるだけでなく、薬剤の活性を低下させるためにも用いられています。保護基を患部で選択的に除去できれば、薬剤の活性を患部で選択的に示す「プロドラッグ」としての応用が期待できます注1)。さらに、芳香環を持つ保護基を導入した分子は、水中で会合する性質があり、バイオマテリアルに応用されています。
しかし、これまでに開発された保護基には、保護基を外す条件や保護基の安定性に問題がありました(図1B)。すなわち、温和な反応条件を用いて除去できる保護基は不安定で、別の化学反応によって外れやすく、望まない副反応が起こってしまいます。また、安定な保護基は高温や強酸などの厳しい条件を用いて外す必要があり、その場合にも望まない副反応や化合物の分解が起こってしまいます。これらの問題を解決するためには、温和な条件で外すことができ、かつ安定性を兼ね備えた保護基の開発が必要です。
そこで、研究チームは”変身”する保護基という新しい概念によって、安定でありながら温和な条件で外すことができる保護基の開発を目指しました。
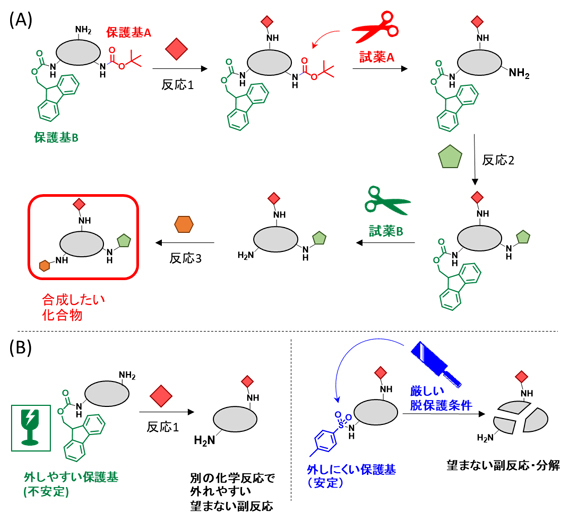
図1 有機合成における保護基の利用とこれまでに開発された保護基の問題点
A)保護基を用いる化学合成。異なる保護基を順番に外すことで、それぞれの官能基に異なる化学反応を選択的に起こすことができる。
B)これまでに開発された保護基の問題点。外しやすい保護基は不安定であり、異なる化学反応によって望まない副反応が起こる。また、安定な保護基は外しにくいため、厳しい反応条件によって望まない副反応や分解が起こる。
注1)2020年9月2日プレスリリース「生体内の金属触媒反応で薬効と物性を制御する」
研究手法と成果
研究チームは、安定な構造から不安定な構造に変身できる保護基として「2-(2-エチニルフェニル)-2-(5-メチルフラン-2-イル)-エトキシカルボニル基(Epoc基)」をデザインしました。Epoc基は、酸や塩基などに対しては安定な構造をしていますが、金(III)触媒を作用させると塩基性に不安定な「(4-ヒドロキシ-3-メチル-9H-フルオレン-9-イル)-メトキシカルボニル基(Hmoc基)」に変身します。この特徴から、Epoc基は変身する前は安定であり、変身後は外れやすい構造になることで、相反する二つの性質を両立できます。
実際に、アミノ酸や糖に導入したEpoc基を外す実験を行ったところ、Epoc基は、金(III)触媒によって室温10分という温和な条件でHmoc基へと変身し、弱塩基であるピペリジンを加えることで外すことができました(図2)。また、生体内を模した水中でもこの変換反応が効率良く進行したことから、Epoc基の変換反応を生体内へ応用できる可能性が示されました。
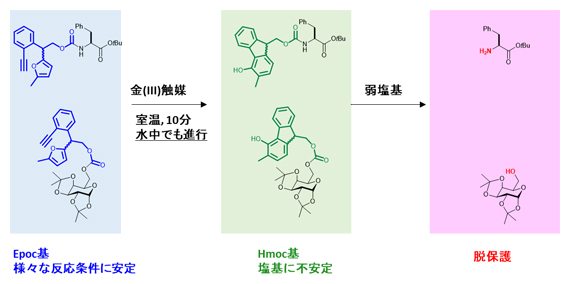
図2 Epoc基を外す反応条件
アミノ酸(上段)と糖(下段)に導入したEpoc基の反応。Epoc基は温和な金触媒反応により、塩基に不安定なHmoc基に変身する。Hmoc基は弱塩基を用いた反応によって外すこと(脱保護)ができる。
次に、Epoc基のさまざまな反応条件への安定性を調べるために、別の保護基を持つ化合物にEpoc基を導入し、保護基を選択的に外す実験を行いました。その結果、強酸や強塩基、ヒドラジン[4]やパラジウム触媒[5]といった試薬を用いた条件で外れる保護基は、Epoc基に影響を与えず、選択的に外すことができました(図3上)。このことから、Epoc基はこれらのさまざまな反応条件に安定であることが示されました。一方で、Epoc基を外す反応条件(金触媒+弱塩基)は温和であるため、同じ基質に対して他の保護基に影響を与えず、選択的にEpoc基を外すことができました(図3下)。
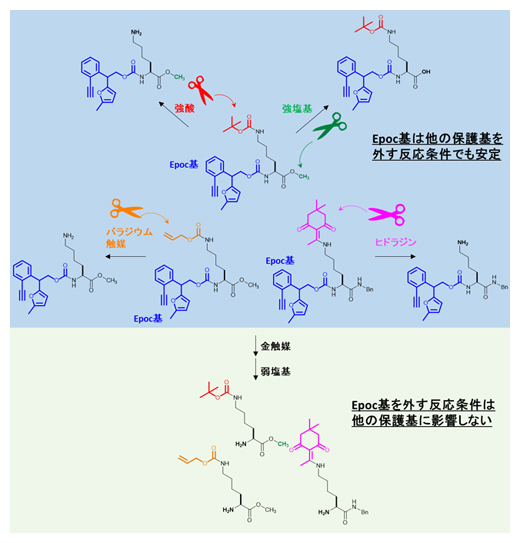
図3 Epoc基の安定性と選択的な除去
Epoc基は強酸や強塩基、ヒドラジンやパラジウム触媒など、さまざまな試薬に対して安定であった(上)。また、Epoc基を外す条件は温和であるため、同じ基質に対して、他の保護基に影響を与えなかった。
さらに、Epoc基を枝分かれしたペプチドの固相合成[6]に応用しました。ペプチド固相合成では弱塩基で外れる9-フルオレニルメチルオキシカルボニル基(Fmoc基)[7]の除去と、Fmoc基で保護したアミノ酸の縮合を樹脂上で繰り返すことでペプチド主鎖を伸ばします。枝分かれしたペプチドを合成するには、ペプチド主鎖を伸長している間は分岐点のアミノ基を保護しておき、分岐点からペプチドを伸長するときに、その保護基を選択的に外す必要があります。そのため、ペプチド主鎖を伸長する反応条件の影響を受けず、特殊な試薬を用いて選択的に外すことができる保護基を分岐点のアミノ基に導入する必要があります。
今回の実験では、ペプチドの分岐点にEpoc基を導入して、枝分かれしたペプチドの合成を行いました(図4)。Epoc基は安定であるため、Fmoc基の除去と保護アミノ酸の縮合を繰り返しても外れることなく、分岐点にEpoc基を持ったペプチドを樹脂上で合成できました。そこで、ペプチドの分岐点に導入したEpoc基を金(III)触媒によってFmoc基によく似たHmoc基に変身させることで、分岐点の保護基を外しやすくしました。Fmoc基と同様に、弱塩基を加えることでHmoc基を外し、分岐点のアミノ基を活性化しました。そして、分岐点からペプチドを伸長し、枝分かれしたペプチドを合成しました。
Epoc基はFmoc基によく似た構造に変身できるという特徴から、変身前は安定でありながら、変身後はペプチド固相合成に用いられるFmoc基を外す手法とほぼ同じ温和な条件で外すことができます。このように、その安定性と簡便で温和な外し方から、Epoc基のペプチド固相合成での有用性を示すことができました。
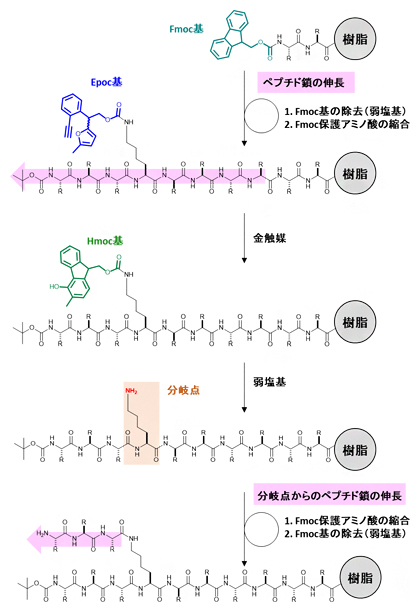
図4 Epoc基のペプチド固相合成への応用
ペプチド主鎖を伸長する反応はEpoc基に影響を与えず、分岐点にEpoc基を導入したペプチドを樹脂上で合成することができた。金触媒(III)はペプチド分岐点のEpoc基をHmoc基に変身させ、さらに弱塩基を加えることで、ペプチドの分岐点を選択的に活性化させた。これによって、分岐点からのペプチドの伸長が可能となり、枝分かれしたペプチドを合成することができた。
今後の期待
今回の研究で開発した”変身”できるEpoc基は、変身前の安定性と変身後に温和な条件で外すことができるという相反する二つの性質を両立しています。また、これまでに金(III)触媒で選択的に脱保護される保護基は開発されていないことから、有機合成での保護基の戦略について新しい選択性を示すことができました。これらの特徴から、複雑で不安定な化合物の合成にEpoc基が応用されることが期待できます。
変身によって保護基の性質を変化させるというEpoc基の特徴は、単なる保護基としての応用だけでなく、生体内で分子の性質を変化させるためのスイッチとしての可能性も秘めています。これまでに田中克典チームリーダーらは細胞培養液中やマウスの生体内で化学反応を制御できる金触媒を開発してきました注2,3)。この技術と今回開発したEpoc基を組み合わせることによって、Epoc基を導入したプロドラッグを生体内で活性化する手法を開発できるかもしれません。
さらに、Epoc基から変換されたHmoc基は大きな芳香環を含む構造をしています。Hmoc基のように大きな芳香環を持った保護基は水中で会合しやすく、バイオマテリアルにも用いられていることから、生体内金触媒によるEpoc基の変身を引き金として、生体内でバイオマテリアルを構築するような分子の開発にもつながる可能性があります。
注2)2017年2月15日プレスリリース「狙った臓器で金属触媒反応を実現」
注3)2021年3月18日プレスリリース「がん細胞上で薬剤を化学合成」
補足説明
1.金触媒
金(Au)で構成される触媒。アルキン(炭素-炭素間の三重結合)に対して強い親和性を示すため、特異な化学反応を触媒する。また、生体内での化学反応の制御にも近年は応用されている。
2.保護基
有機化合物中の反応性の高い官能基に導入することで、不活性化できる官能基。薬剤などを合成するときに、特定の官能基における望まない副反応を防ぐために導入される。特定の試薬や反応条件によって除去(脱保護)することが可能。
3.プロドラッグ
生体内の薬剤標的部位での化学反応によって、薬効を示す分子に変換されることで活性を示すようにデザインされた薬剤。標的部位選択的に活性を示すことから、副作用の軽減が期待できる。標的部位での化学反応には、生体内の酵素による触媒反応や生体内の低分子との反応が主に用いられる。また、近年は生体内に導入した遷移金属触媒によって分子の変換を行う研究も進められている。
4.ヒドラジン
分子式N2H4で表される弱塩基。引火性であることから、ロケットの燃料などに用いられている。強い還元性によってさまざまな化合物と反応するため、有機合成の試薬としても用いられる。また、ヒドラジンによって選択的に外すことができる保護基もいくつか開発されている。
5.パラジウム触媒
遷移金属の一つであるパラジウム(Pd)によって構成される触媒。炭素-炭素間の結合を形成するクロスカップリング反応など、有用な化学反応を多く触媒することから、有機合成において頻繁に用いられる。また、パラジウム触媒によって選択的に外すことができる保護基も開発されている。
6.ペプチド固相合成
ペプチド(アミノ酸によって構成されるポリマー)を樹脂上で合成する手法。樹脂に担持させたアミノ酸に対し、保護基を導入したアミノ酸の縮合と脱保護を繰り返すことで、ペプチドを伸長できる。合成したペプチドを樹脂に担持できるため、伸長に用いた試薬や副生成物を除去しやすく、簡便にペプチドを合成できる。
7.9-フルオレニルメチルオキシカルボニル基(Fmoc基)
弱塩基を用いた温和な条件によって速やかに外すことができる保護基。ペプチド固相合成では保護基を除去する反応を繰り返す必要があり、ペプチドでの望まない副反応が懸念されるが、温和な条件で外すことができるFmoc基は、副反応を抑制できる。
研究チーム
理化学研究所
開拓研究本部 田中生体機能合成化学研究室
主任研究員 田中 克典(たなか かつのり)
(東京工業大学 物質理工学院 応用化学系 教授)
基礎科学特別研究員 山本 智也(やまもと ともや)
特別研究員 チャン・ツンチェ(Chang Tsung-che)
原論文情報
Tomoya Yamamoto, Tsung-che Chang, and Katsunori Tanaka, “Epoc group: transformable protecting group with gold(III)-catalyzed fluorene formation”, Chemical Science, 10.1039/D1SC03125B
発表者
理化学研究所
開拓研究本部 田中生体機能合成化学研究室
主任研究員 田中 克典(たなか かつのり)
(東京工業大学 物質理工学院 応用化学系 教授)
基礎科学特別研究員 山本 智也(やまもと ともや)
報道担当
理化学研究所 広報室 報道担当
東京工業大学 総務部 広報課