2021-10-08 関西医科大学,日本医療研究開発機構
本研究のポイント
- がんの悪性化や炎症性疾患に関わる分子Mint3(注1)の機能を阻害する化合物を同定しました
- Mint3阻害化合物はマウスモデルで腫瘍の増殖、転移、エンドトキシンショック(注2)を抑えました
- 今後Mint3を標的としたがん治療薬、炎症性疾患治療薬の開発が期待されます
概要
関西医科大学附属生命医学研究所 がん生物学部門 坂本毅治学長特命教授らの研究グループは、がんの悪性化や炎症性疾患に関わる分子Mint3の阻害化合物を同定し、マウスモデルでMint3阻害化合物が腫瘍増殖、転移、エンドトキシンショックを抑制することを明らかにしました。
本研究成果は、オンライン雑誌「Communications Biology」に2021年10月7日付けで掲載されました。今後Mint3を標的としたがん治療薬、炎症性疾患治療薬の開発が期待されます。
研究の背景
酸素は私たちが生きていくうえで欠かすことが出来ないものです。酸素濃度を細胞がどのように感知し、それに応答していくかという仕組みを明らかにしたとして、英・米の3名の研究者が2019年にノーベル医学生理学賞を受賞しています。この、細胞の酸素濃度への応答に関わる重要な転写因子(注3)として低酸素誘導因子hypoxia inducible factor-1(HIF-1)があり、HIF-1は低酸素下で蓄積し低酸素に適応するのに必要な遺伝子の発現を促します。HIF-1は造血や幹細胞の機能維持など正常臓器の機能に重要な役割を果たす一方で、がんや炎症性疾患を悪化させていることが明らかになっています。多くの研究から、実験的にHIF-1を阻害するとがんや炎症性疾患が抑えられることが示されていますが、HIF-1が正常臓器の機能にも関わるためHIF-1自身を標的とした薬剤の開発は困難です。
研究代表者の坂本毅治学長特命教授らのグループは、これまでにがん細胞やマクロファージなど特定の細胞だけでHIF-1を活性化させる分子としてMint3を同定し、Mint3がHIF-1同様にがんや炎症性疾患に関わることを明らかにしてきました。がんの浸潤・転移に関わる膜型のプロテアーゼMT1-MMPの発現により、HIF-1の活性を抑制する分子FIH-1とMint3が結合します。その結果、FIH-1による酸素依存的なHIF-1の抑制が解かれ、酸素が存在する状態でもHIF-1は転写因子として機能することが出来ます(図1)。Mint3によるHIF-1活性化はMT1-MMPが高発現するがん細胞やマクロファージの一部の細胞に限られます。また、Mint3を欠損したマウスには明らかな異常が見られないことから、Mint3を阻害することでがん細胞やマクロファージなど特定の細胞だけでHIF-1の機能を抑制し、副作用が少なくがんや炎症性疾患が抑えられる薬剤の開発が期待されていました。しかしながら、Mint3の機能を抑える化合物は見つかっておらず、実際にMint3阻害剤ががんや炎症性疾患に有効かは不明でした。
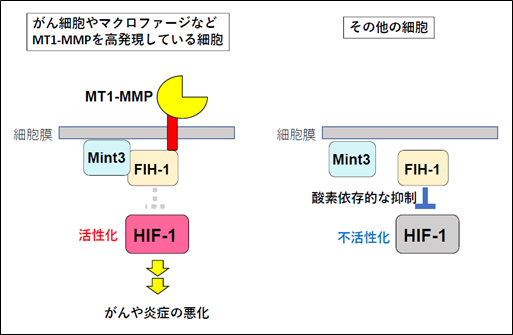
図1.Mint3によるHIF-1活性化
本研究で得られた結果・知見
坂本毅治学長特命教授らのグループは、理化学研究所環境資源科学研究センター ケミカルバイオロジー研究グループの長田裕之グループディレクター、近藤恭光専任研究員らとの共同研究で、ケミカルアレイ(注4)を用いてMint3に結合する化合物を探索し、23,275化合物の中からMint3に結合する化合物を1つ同定しました。この化合物と化学構造の似た類縁化合物の中からMint3によるHIF-1活性化を抑制する活性の高い化合物を絞り込み、初のMint3阻害化合物としてnaphthofluorescein(以下Naph)を同定いたしました(図2上)。がん細胞を用いた実験で、NaphはMint3によるHIF-1活性化を特異的に抑制しました(図2左下)。Mint3はHIF-1の活性化を介してマクロファージの解糖系(注5)によるエネルギー産生を促進することが報告されていますが(Hara T et al., JBC, 2011)、NaphはMint3特異的にマクロファージの乳酸(解糖系の最終代謝産物)産生とATPレベルを抑制しました(図2右下)。これらの結果から、Naphはがん細胞、マクロファージでMint3の機能を阻害することが分かりました。
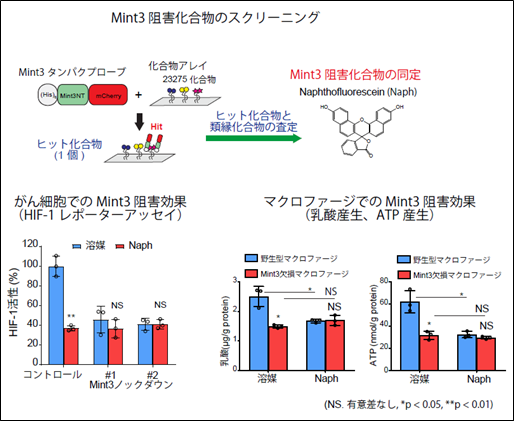
図2.Mint3阻害化合物のスクリーニングとがん細胞、マクロファージへの効果
続いて、安全性を確認するためにNaphをマウスに投与したところ、体重減少、血液生化学値の異常、肝臓や腎臓などの臓器の形態学的異常を示すことはありませんでした。次に、がん治療モデルでNaphの効果を検証しました。マウス乳がんE0771細胞の皮下腫瘍を持つマウスにNaphを投与したところ、腫瘍の増殖が顕著に抑制されました(図3左上)。また、Naphと抗がん剤を併用したところ、単剤では効果の出ない投与量・投与頻度でヒト乳がんMDA-MB-231細胞、ヒト膵がんAsPC-1細胞のマウス皮下腫瘍の増殖を抑制しました(図3右上)。これらの結果から、Naphは腫瘍増殖を抑制することが分かりました。Mint3はマクロファージの一種である炎症性モノサイトを活性化して、がんの転移を促進することが知られています(Hara T et al., PNAS, 2017)。そこでマウスメラノーマB16F10細胞の肺転移実験でNaphをマウスに投与したところ、野生型のマウスではB16F10細胞の肺転移が抑制されました(図3下)。一方で、Mint3欠損マウスではNaphはB16F10細胞の肺転移が抑制されませんでした。このことから、NaphはMint3特異的にがんの転移を抑制することが分かりました。
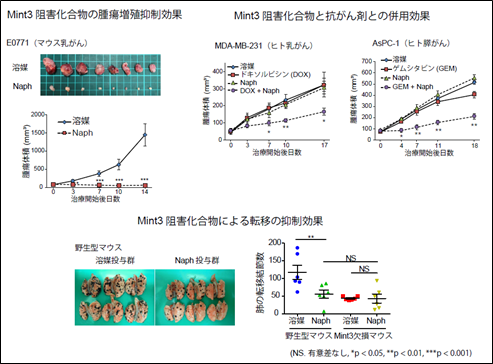
図3.Mint3阻害化合物による腫瘍増殖、肺転移の抑制効果
Mint3欠損マウスはリポポリサッカライド(LPS)に対するマクロファージの過剰活性化が抑えられることで、エンドトキシンショックに抵抗性を示すことが報告されています(Hara T et al., JBC, 2011)。そこで、エンドトキシンショックモデルでのNaphの効果を検証しました。Naphを投与した野生型マウスでは、Mint3欠損マウスと同定度にまでLPS投与後の生存率が改善しました(図4上)。血液中の炎症性サイトカインの濃度を測定したところ、Naph投与により、TNF-α、IL-6、IL-12p70の血中濃度のLPSによる上昇が抑制されました(図4下)。以上の結果から、Naphはエンドトキシンショックの予防に有効であることが分かりました。
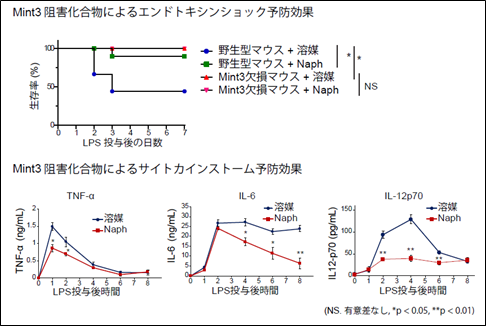
図4.Mint3阻害化合物によるエンドトキシンショックの予防効果
今後の研究展開および波及効果
本研究でMint3阻害化合物が、がんの増殖、転移、エンドトキシンショックを抑制することが明らかとなりました(図5)。本研究で同定した化合物はそのままでは可溶性に問題がありヒトには使用できませんが、今後ヒトに使用可能なMint3阻害剤の開発が進むことで、Mint3を標的とした新しいがん・炎症性疾患の治療薬の開発が期待されます。また、本研究で同定したMint3阻害化合物を使用することで、Mint3阻害剤ががんやエンドトキシンショック以外のどのような疾患の治療に有効かを調べる研究が加速することが期待されます。
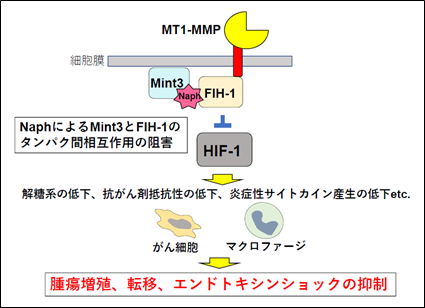
図5.Mint3阻害化合物による腫瘍増殖、転移、エンドトキシンショックの抑制
本研究への支援
本研究は、以下の支援を受けて実施されました。
- 国立研究開発法人日本医療研究開発機構(AMED)次世代がん医療創生研究事業(P-CREATE)「がん細胞・がん間質細胞特異的な酸素センシング機構を標的としたがん微小環境標的薬剤の開発(研究代表者:坂本毅治)」
- 日本学術振興会(JSPS)科学研究費補助金 基盤研究(C)「化学療法誘導性転移の新規分子機構の解明と予防法の確立(研究代表者:坂本毅治)」、基盤研究(C)「ケミカルアレイによる膜結合蛋白質発現細胞を用いたリガンド探索手法の開発(研究代表者:近藤 恭光)」
- 文部科学省(MEXT)科学研究費補助金 新学術領域研究(研究領域提案型)「ユビキチン機能制御のためのケミカルバイオロジー(研究分担者:近藤恭光)」
- 公益財団法人小林がん学術振興会 研究助成(先駆的研究)「がん組織標的薬と抗がん剤の併用によるがん特異的かつ汎用性の高い新規治療法の開発(研究代表者:坂本毅治)」
用語解説
- (注1)Mint3
- Munc18-1-interacting protein 3。分子量約60kDaの細胞内タンパク質である。別名amyloid beta A4 precursor protein-binding family A member 3(APBA3)。
- (注2)エンドトキシンショック
- エンドトキシンはグラム陰性菌の外膜を構成するリポ多糖で、リポポリサッカライド(LPS)とも呼ばれる。エンドトキシンショックとは、多量のエンドトキシンにより病的な炎症応答が誘導されサイトカインストームと呼ばれる炎症性サイトカインの血中濃度が非常に高い状態になり、血圧低下や、血管内血液凝固による多臓器不全を引き起こすショック症状。
- (注3)転写因子
- DNA上の特定の配列に結合することで標的遺伝子の発現量を変化させる分子。
- (注4)ケミカルアレイ
- 数千種類の小分子化合物を1枚のスライドガラスに固定化したもの。
- (注5)解糖系
- 細胞質内で行われる糖の代謝経路。多段階の生化学反応でグルコースをピルビン酸や乳酸に分解し、細胞のエネルギー源であるATPを産生する。解糖系に関わる多くの遺伝子がHIF-1により発現調節を受ける。
論文タイトル、著者および所属
- 掲載雑誌名
- Communications Biology(2021年10月7日オンライン版)
- 論文タイトル
- Pharmacological inhibition of Mint3 attenuates tumour growth, metastasis, and endotoxic shock
- 著者および所属
- 坂本毅治1,2,*、福井優也2,3、近藤恭光4、本田香織4、清水猛4、原敏郎5、林哲郎6、齊藤百合花7、村上善則6、井上純一郎3、金子周一2、長田裕之4、清木元治5
(*:責任著者)- 関西医科大学附属生命医学研究所 がん生物学部門
- 金沢大学医薬保健研究域医学系 システム生物学分野
- 東京大学医科学研究所 分子発癌分野
- 理化学研究所 環境資源科学研究センター ケミカルバイオロジー研究グループ
- 東京大学医科学研究所 腫瘍細胞社会学分野
- 東京大学医科学研究所 人癌病因遺伝子分野
- 帝京科学大学 医学教育センター
(所属は研究当時)
- DOI
- 10.1038/s42003-021-02701-1
お問い合わせ先
本研究に関すること
関西医科大学 附属生命医学研究所 がん生物学部門
学長特命教授 坂本毅治
プレスリリースに関すること
関西医科大学 広報戦略室
AMED事業に関すること
日本医療研究開発機構 創薬事業部 医薬品研究開発課
次世代がん医療創生研究事業(P-CREATE)


