2025-08-19 京都大学
<関連情報>
- https://www.kyoto-u.ac.jp/ja/research-news/2025-08-19-0
- https://www.kyoto-u.ac.jp/sites/default/files/2025-08/2508_BJoHaem_Jo_relj%20web-cb2d1f3e8dcbbb55fc8556b7853facdf.pdf
- https://onlinelibrary.wiley.com/doi/10.1111/bjh.70090
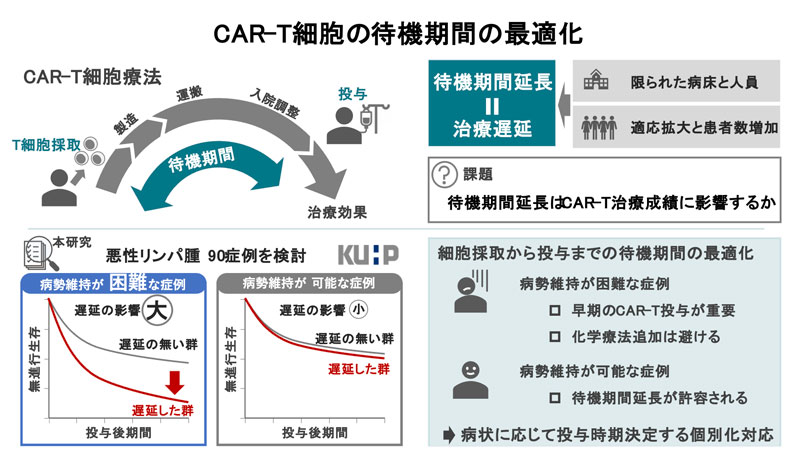
拡散性大細胞型B細胞リンパ腫において、キメラ抗原受容体T細胞の採血から輸液までの時間が延長されると、予後が悪化する Prolonged chimeric antigen receptor-T apheresis to infusion time is associated with inferior outcomes in diffuse large B-cell lymphoma
Suguru Morimoto, Tomoyasu Jo, Toshio Kitawaki, Takashi Sakamoto, Chisaki Mizumoto, Junya Kanda, Momoko Nishikori, Kouhei Yamashita, Miki Nagao, Akifumi Takaori-Kondo, Yasuyuki Arai
British Journal of Haematology Published: 11 August 2025
DOI:https://doi.org/10.1111/bjh.70090
Summary
Chimeric antigen receptor (CAR) T-cell therapy is effective for relapsed/refractory (r/r) diffuse large B-cell lymphoma (DLBCL). However, delays between apheresis and infusion frequently occur due to limited facility capacity and prolonged bridging therapy, and the clinical impact of such delays remains uncertain. We retrospectively analysed R/R DLBCL patients who underwent CAR-T-cell therapy at Kyoto University Hospital. Among 90 patients, the median apheresis to infusion interval was 66 days (range, 28–203). Patients were categorized into delayed (≥66 days) and non-delayed (<66 days) groups. Baseline characteristics at infusion were similar, whereas adverse features such as extranodal involvement and stable/progressive disease (SD/PD) were less common in the delayed group. Multivariate analysis identified delayed infusion as a significant negative prognostic factor for progression-free survival (adjusted hazard ratio [aHR] 3.13; 95% confidence interval [CI] 1.63–6.00; p = 0.001), along with extranodal involvement (aHR 2.39; p = 0.004), SD/PD (aHR 2.66; p = 0.005), bulky disease (aHR 3.08; p = 0.008) and treatment with tisa-cel (aHR 5.26; p = 0.001). Overall survival was also inferior in the delayed group (aHR 2.53, 95% CI 1.29–4.96; p = 0.007). Minimizing apheresis to infusion interval through improved workflows, institutional capacity and avoiding prolonged bridging in non-responders may enhance outcomes.


