2026-03-23 京都大学 iPS研究所
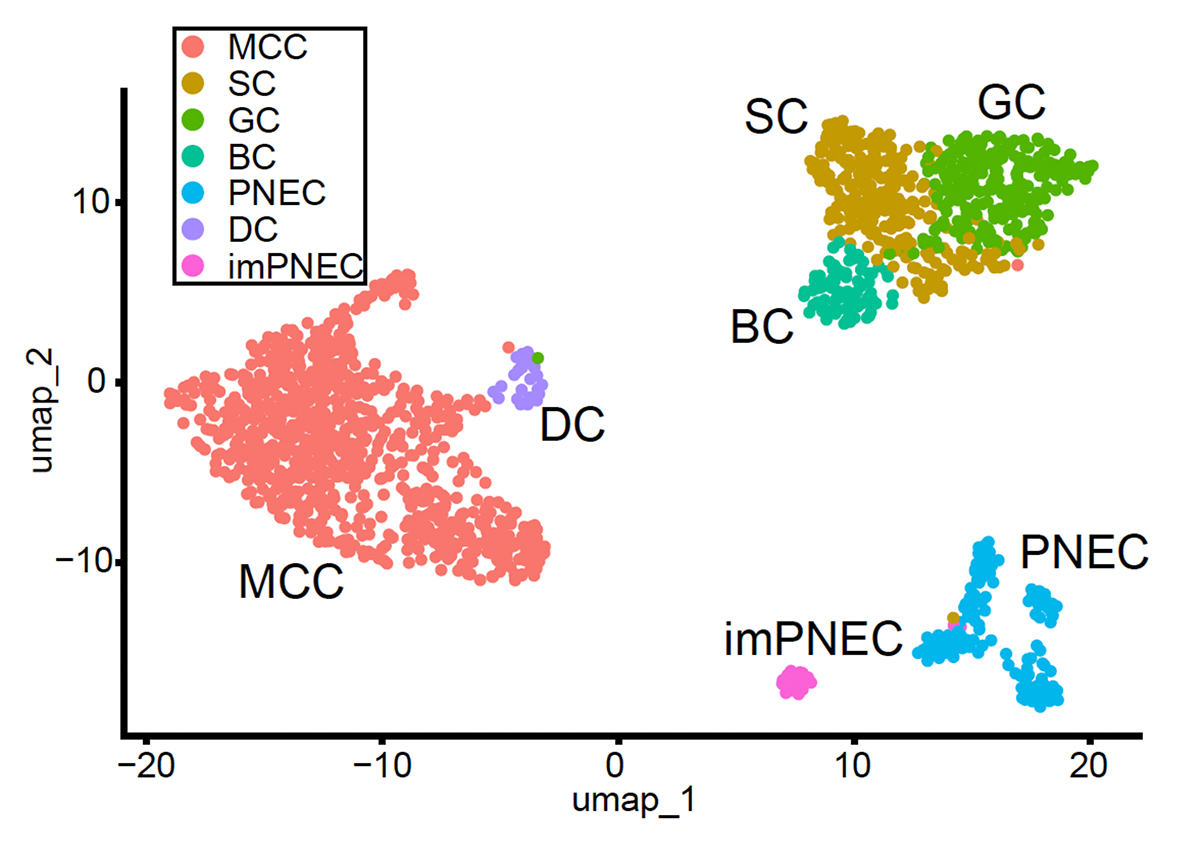
Fig. 1 ヒトiPS細胞由来気道上皮細胞のscRNA-seqに基づくUMAP解析
一つ一つの点が細胞1個を表しており、近くに表示された細胞ほど似た性質を持っている。デューテロソーマル細胞(DC)の集団が存在することが確認された。
<関連情報>
- https://www.cira.kyoto-u.ac.jp/j/pressrelease/news/260323-010000.html
- https://www.cell.com/stem-cell-reports/fulltext/S2213-6711(26)00071-8
ヒト気道分化における多繊毛形成を担うのは、後代体細胞である Deuterosomal cells are the responsible lineage for multiciliogenesis in human airway differentiation
Haruka Yamaki ∙ Satoshi Konishi s ∙ Koji Tamai ∙ … ∙ Toyohiro Hirai ∙ Kazuhiko Takeuchi ∙ Shimpei Gotoh
Stem Cell Reports Published:March 19, 2026
DOI:https://doi.org/10.1016/j.stemcr.2026.102860
Highlights
- CD36 serves as a surface marker for isolating iPSC-derived deuterosomal cells (DCs)
- Altered DC identity in CCNO variants impairs multiciliated cells (MCCs) maturation
- CCNO variants disrupt DC-MCC pathway and promote expansion of aberrant precursors
- Human iPSC-derived DCs enable study of multiciliogenesis mechanisms
Summary
Multiciliated cells (MCCs) are pivotal in airway defense via their motile cilia to eliminate inhaled pathogens and particles. Genetic variants in primary ciliary dyskinesia (PCD) disrupt ciliary function, resulting in chronic respiratory infections. The formation of MCCs requires centriole amplification mediated by non-membranous organelles called deuterosomes, whose regulatory mechanisms remain poorly characterized in humans. Single-cell transcriptomic analyses have identified “deuterosomal cells” (DCs), a transient cell population that emerges during multiciliogenesis. DCs are challenging to investigate owing to their scarcity. To elucidate the role of DCs, iPSC-derived airway epithelial cells were used to identify CD36 as a specific surface marker. Furthermore, iPSCs were established from a patient with PCD harboring Cyclin O (CCNO) variants, along with gene-corrected controls. Patient-derived iPSCs demonstrated defective MCC differentiation and aberrant DCs attributed to CCNO deficiency. This study provides a human iPSC-based platform for investigating the mechanisms underlying airway multiciliogenesis and PCD modeling.