2026-05-13 京都大学iPS細胞研究所]
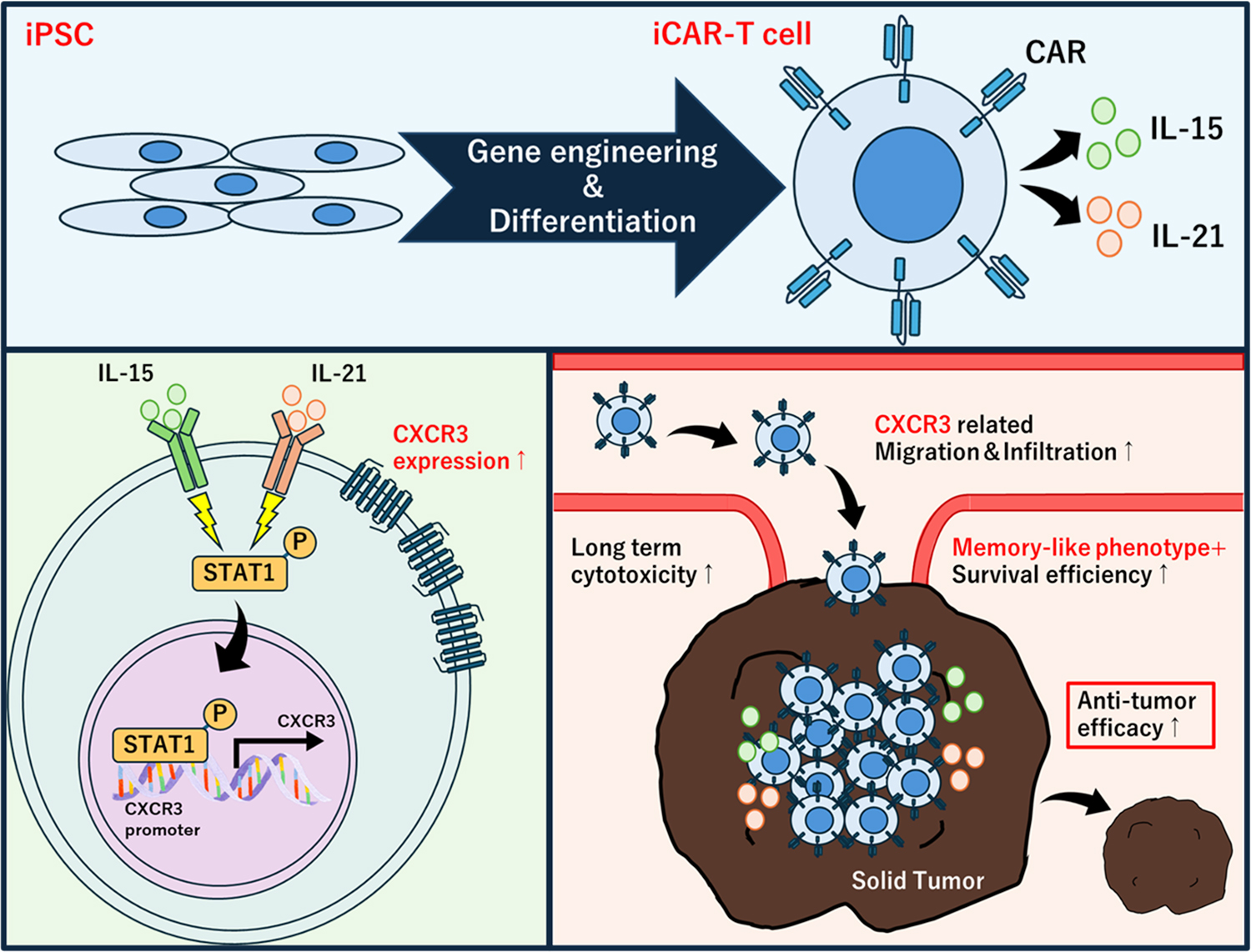
本研究の概要
<関連情報>
- https://www.cira.kyoto-u.ac.jp/j/pressrelease/news/260513-100000.html
- https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(26)00301-1
IL-15とIL-21の相乗効果により、固形腫瘍におけるiPSC由来細胞傷害性T細胞の抗腫瘍効果が向上する IL-15 and IL-21 synergy improves anti-tumor efficacy of iPSC-derived cytotoxic T cells in solid tumors
Akihiro Ishikawa ∙ Masazumi Waseda ∙ Tomoko Ishii ∙ Yohei Kawai ∙ Shin Kaneko
Molecular Therapy Published:May 12, 2026
DOI:https://doi.org/10.1016/j.ymthe.2026.04.036
Abstract
The development of effective cellular immunotherapies for solid tumors requires the presence of robust infiltration, persistence, proliferation, and antigen-specific cytotoxicity. Here, we engineered induced pluripotent stem cell (iPSC)-derived cytotoxic T cells transduced with a chimeric antigen receptor (iCAR-T cells) and identified an optimal cytokine armoring strategy. Co-expression of interleukin-15 (IL-15) and IL-21 synergistically enhanced STAT1 phosphorylation, leading to increased transcriptional activation of the chemokine receptor CXCR3 and thereby improving tumor homing capacity. Furthermore, the engineered iCAR-T cells maintained a CD45RA−CD45RO+CCR7+CD62L+ memory T cell-like phenotype in tumors, contributing to the prolonged survival of the animal model. These findings demonstrate that cytokine synergy can be engineered into iPSC-derived T cells to overcome significant barriers in solid tumor immunotherapy, offering a scalable approach to developing next-generation off-the-shelf CAR-T therapies.