2021-03-03 国立長寿医療研究センター,新潟大学,東北大学東北メディカル・メガバンク機構,日本医療研究開発機構
研究成果のポイント
- 日本人に特有および民族集団横断型の新規アルツハイマー病関連遺伝子座位群を同定
- アルツハイマー病のリスク因子群を用いた早期発症予測法の開発に貢献
- アルツハイマー病の関連分子の同定と病因解明から治療薬開発に貢献
概要
国立研究開発法人国立長寿医療研究センター(理事長:荒井秀典、愛知県大府市。以下国立長寿医療研究センター)メディカルゲノムセンターの尾崎浩一部長、重水大智ユニット長らの共同研究グループ※は、日本人および欧米人の遺伝的多型情報を基にアルツハイマー病(AD)の新規関連遺伝子座位群を発見しました。
チームは、始めに日本人のAD患者3,962人と認知機能正常者4,074人の全ゲノムにわたる一塩基多型(※1)を用いたゲノムワイド関連解析(Genome Wide Association Study;GWAS)(※2)を行い、第4染色体上FAM47E領域に日本人に特有なAD関連を示す新規遺伝子座位を同定しました。このゲノムワイド遺伝子型データの取得には、東北大学が開発したジャポニカアレイ®(※3)が使われました。
さらに国際アルツハイマー病ゲノムプロジェクト(IGAP:International Genomics of Alzheimer’s Project)のGWAS統計データを用いて民族集団横断型メタ解析(異なる民族集団のGWASデータを統計学的に統合解析すること)を実施し、第6染色体上OR2B2 領域に新規関連遺伝子座位を同定しました。この2座位に加え、統計学的にADと示唆的な有意性を示す9座位の疾患関連候補座位を同定しました。
この研究は、国立研究開発法人日本医療研究開発機構(AMED)の「臨床ゲノム情報統合データベース整備事業」による支援で実施されたもので、研究成果は科学雑誌Translational Psychiatry(トランスレーショナル・サイカイアトリー)に、2021年3月3日(JST)付で掲載されます。
- ※共同研究グループ
-
- 国立長寿医療研究センター
- 研究所/メディカルゲノムセンター(MGC)
- 所長/センター長 新飯田俊平(にいだしゅんぺい)
- 部長 尾崎浩一(おざきこういち)
- ユニット長 重水大智(しげみずだいち)
- 研究員 光森理紗(みつもりりさ)
- 研究員 秋山真太郎(あきやましんたろう)
- 研究員 森園隆(もりぞのたかし)
- 研究員 檜垣小百合(ひがきさゆり)
- 特任研究員 浅海裕也(あさのみゆうや)
- 新潟大学 脳研究所 遺伝子機能解析学分野
- 教授 池内健(いけうちたけし)
- 准教授 宮下哲典(みやしたあきのり)
- 特任助教 原範和(はらのりかず)
- 東北大学 東北メディカル・メガバンク機構
- 副機構長・教授 木下賢吾(きのしたけんご)
- 教授 田宮元(たみやげん)
背景
ADはそのほとんどが孤発性で65歳以上の高齢者に発症します。孤発性ADは、認知症の半数以上を占め環境因子や遺伝的因子が複雑に相互作用して発症することが知られています。遺伝的因子が発症に与える割合は非常に大きく、60~80%程度であると言われ、多数の遺伝的因子(ポリジェニック)がADの病因と進行に関係すると考えられています。染色体19番のApolipoprotein E遺伝子(APOE)のE4アレル(特定の遺伝子多型を持つ遺伝子座位)は、孤発性ADの最も高い遺伝的リスク因子として知られていますが、残りの大部分の遺伝的リスク因子は未だ解明されていません。
近年、欧米では大規模なゲノム解析研究が実施され、30箇所程のAD関連遺伝子座位が発見されていますが、疾患の遺伝率を考えると未だ多くの遺伝的リスク因子が存在すると考えられています。一方、日本人、欧米人など民族集団間における遺伝的構造は大きく異なることが知られており、欧米人で発見した遺伝的リスク因子のすべてが日本人にも当てはまるとは限りません。日本人の大規模サンプルを用いたADのGWASはまだまだ不十分です。
研究成果の内容
日本人のGAWSでは、国立長寿医療研究センターのバイオバンク(NCGGバイオバンク)のサンプル(AD患者2,974、認知機能正常者3,096)と新潟大学脳研究所のサンプル(AD患者988、認知機能正常者978)を統合して用いました。NCGGバイオバンクのサンプルは、東北メディカル・メガバンク機構で設計されたジャポニカアレイ®でジェノタイピングを実施し、同機構が構築した3,500人の日本人全ゲノムリファレンスパネルを用いて遺伝子型インピュテーション(※4)を施行しました。GWASは年齢と性別を考慮した統計解析により実施しました。その結果、示唆的有意性(P<5×10-6、図1)を示した9つの関連遺伝子座位を発見しました。9座位のうち2座位はAPOEと1の既知の座位でしたが、残る7座位は新規のものでした。これらについて異なる新たな日本人サンプル(AD患者:1,216例、認知機能正常者:2,446例)で再検証解析を行った結果、ゲノムワイド有意性(P<5×10-8未満)を有する遺伝子座位としてFAM47E座位(rs920608、P=5.34×10-9、odds ratio=0.65、95%CI=0.57 to 0.75、11,692例)が同定されました。この座位の特徴を調べたところ、東アジア人に特徴的な頻度を示す座位で、パーキンソン病との関連も報告されていました。GWASの結果を用いた疾患に関係する分子パスウェーイ解析ではADに関係するアミロイド前駆体タンパク関連の他にメタロペプチダーゼやメタロエンドペプチダーゼといったタンパク分解酵素の関連が新たに示唆されました。
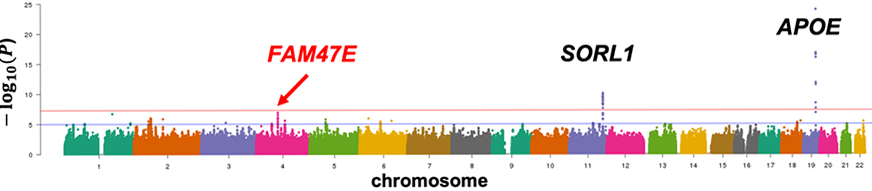
図1 日本人のGWAS解析のマンハッタンプロット
次に、GWASの検出力を増強して新たな関連遺伝子座位を同定するために欧米人データとの民族集団横断型メタ解析を実施しました。欧米人データはIGAPの統計データを利用しました。その結果26箇所の有意性(P<5×10-6)を示す遺伝子座位を同定しました。26箇所のうち18箇所はAPOEを含めた既知の座位で、残りの8箇所は新規のものでした。日本人のGWASと同様、追加サンプルによる検証解析を実施したところ、OR2B2座位(rs1497526、Meta-P=2.14×10-8)がゲノムワイド有意性を有する新規の関連遺伝子座位として同定されました。OR2B2座位は日本人および欧米人のメタ解析により同定されたことから、民族集団間共通のリスクであると考えられます。さらに、これらの解析で最終的にP<1×10-5の有意性を示すAD座位として9個の新規遺伝子領域を同定しました(表)。
表 GWASで同定した関連遺伝子座位
| GWAS有意性(P<5×10-8)を示した新規座位 | P<1×10-5の有意性を示した新規座位 | |
|---|---|---|
| 日本人のGWAS | FAM47E | BANK1、LINC00899 |
| 民族集団横断型メタ解析 | OR2B2 | MTSS1L、CLEC3B、EFL1、FAM155A、NTM、CIS、TSPAN14 |
ここで得られた網羅的な解析情報は日本医療研究開発機構(AMED)のAMEDゲノム制限共有データベース(AGD)および臨床ゲノム情報統合データベース(MGeND)に登録しますので他の研究にも役立てられます。
研究成果の意義
- 日本人の大規模なGWASと白人のGWASデータを用いた民族集団横断型メタ解析を実施し、民族集団特異的ならびに民族集団横断型AD新規関連遺伝子座位を特定しました。
- 日本人のような特定の民族集団の大規模GWASを進めることで、民族集団特異的に病因に関連する新たな遺伝的リスク因子群が特定でき、これらを用いた早期疾患発症予知法の開発に役立ちます。
- 疾患発症の遺伝的背景の特定は、ADの病因を理解するのに役立つとともに分子医科学、薬学的アプローチを組み合わせることにより、新たな治療法や予防法の開発につながる可能性が考えられます。
論文情報
- 掲載誌
- Translational Psychiatry
- 論文タイトル
- Ethnic and trans-ethnic genome-wide association studies identify new loci influencing Japanese Alzheimer’s disease risk
- 著者名
- Daichi Shigemizu, Risa Mitsumori, Shintaro Akiyama, Akinori Miyashita, Takashi Morizono, Sayuri Higaki, Yuya Asanomi, Norikazu Hara, Gen Tamiya, Kengo Kinoshita, Takeshi Ikeuchi, Shumpei Niida, Kouichi Ozaki
- DOI
- 10.1038/s41398-021-01272-3
用語解説
- (※1)一塩基多型(Single Nucleotide Polymorphism;SNP)
- 集団における塩基置換、挿入、欠失頻度がある程度多い置換を遺伝子多型と呼ぶ。一塩基多型とは一塩基(T:チミン、G:グアニン、C:シトシン、A:アデニン)のどれかが他の塩基に置換した遺伝子多型で、ゲノム配列の個人間での違いを示す代表的な多型。生活習慣病の発症には多くの一塩基多型などが関係しておりポリジェニック効果と呼ばれる。
- (※2)ゲノムワイド関連解析(Genome Wide Association Study;GWAS)
- 疾患、コントロール群間など形質の違いでの遺伝子多型の頻度の差を用いて疾患感受型遺伝子などを見つける方法の1つ。ある疾患の患者とその疾患にかかっていない被験者の間で、多型の頻度に差があるかどうかを統計的に検定して調べる。検定の結果得られたP値(偶然にそのような事が起こる確率)が低いほど、関連が強いと判定できる。2002年に日本の理化学研究所から初めて報告された。
- (※3)ジャポニカアレイ®
- 東北メディカル・メガバンク機構により設計されたジェノタイピングアレイ。日本人の全ゲノム配列を基に作成された民族特異的ジェノタイピングアレイ。
- (※4)遺伝子型インピュテーション
- ヒトゲノム上にSNPは1千万箇所以上あることが知られている。しかし、実際のアレイ上に搭載されているSNPは60万箇所程度の代表SNPであるため、数百人から数千人の全ゲノム配列解析情報を基に実際にはジェノタイピングしていない1千万箇所のSNP情報を擬似的に予測する方法。全ゲノム配列情報が多いほど正確な予測が可能になる。
お問い合わせ先
本論文に関すること
国立長寿医療研究センター メディカルゲノムセンター 臨床ゲノム解析推進部
尾崎浩一(おざきこういち)
研究プロジェクトに関すること
国立長寿医療研究センター 研究所
新飯田俊平(にいだしゅんぺい)
報道に関すること
国立長寿医療研究センター 総務部総務課
広報担当 里村亮
AMED事業に関すること
日本医療研究開発機構(AMED)
ゲノム・データ基盤事業部 ゲノム医療基盤研究開発課

