2022-04-28 北海道大学,日本医療研究開発機構
ポイント
- 慢性痛が不安を引き起こす、神経回路の可塑的変化を解明。
- 神経活動操作により、慢性痛モデル動物の不安症状を減弱させることに成功。
- 慢性痛や慢性ストレスによる、不安障害の新規治療薬開発への貢献に期待。
概要
北海道大学大学院薬学研究院の南雅文教授らの研究グループは、慢性痛が不安を引き起こす脳内メカニズムを解明しました。
慢性痛と不安障害・うつ病の併発率が高いことはこれまでにも多く報告されてきましたが、そのメカニズムはよくわかっていませんでした。研究グループは、分界条床核*1と呼ばれる脳部位に着目して研究を進め、慢性痛モデル動物において、分界条床核内の神経情報伝達に変化が生じ、この変化により分界条床核から視床下部外側野*2に情報を伝える神経細胞が抑制されることを解明しました。さらに、ケモジェネティクス*3と呼ばれる先端的な神経活動操作法により、当該神経細胞の抑制を解除することで、慢性痛モデル動物に見られる不安症状が軽減することも明らかにしました。これらの知見は、痛みが慢性化する影響で生じる分界条床核内の神経回路の機能変化が不安症状を引き起こしていることを示しています。
本研究成果は、慢性痛の治療だけでなく、慢性痛をはじめとする慢性的なストレスにより引き起こされる不安障害・うつ病などの精神疾患の治療にも役立つ、新しい治療薬やニューロモデュレーションなどの治療法の開発に貢献することが期待されます。
なお、本研究成果は、日本時間2022年4月28日(木)午前4時公開のScience Advances誌に掲載されました。
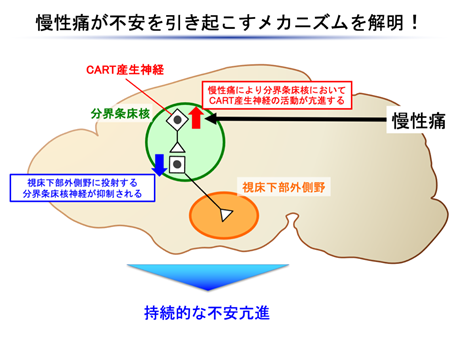
本研究の概念図
背景
ヒトは痛みにより嫌悪・不安・恐怖・抑うつを感じることで、体の危険に気づき、薬を服用したり病院に行ったりします。動物も痛みを感じることで危険を回避できます。例えば、ケガにより運動能力が低下しているときなどは、痛みの神経回路を介して不安水準を引き上げ、より慎重に行動することで危険を回避できる可能性が高まります。このように、痛みは体の危険を教えてくれる警告信号として、重要な役割を果たしています。しかし、慢性痛では、警告信号の役割を果たした後でも痛みが続き、生活の質(QOL)を大きく損なうだけでなく、不安障害やうつ病などの精神疾患の引き金ともなります(図1)。
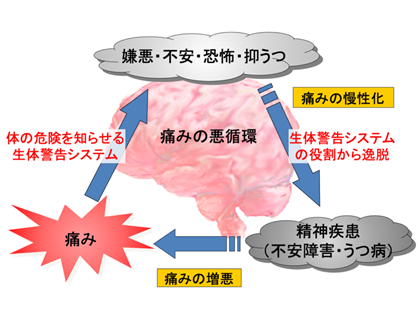
図1 慢性痛による痛みの悪循環の概念図
慢性痛と不安障害・うつ病の併発率は高いことが報告されており、慢性痛による持続的な不安・抑うつの亢進と不安障害・うつ病などの精神疾患との間には、共通の脳内メカニズムがあることが推測されます。しかし、慢性痛が持続的な不安を引き起こす脳内メカニズムについては、よくわかっていませんでした。
一方、分界条床核と呼ばれる脳部位から視床下部外側野と呼ばれる脳部位に情報を伝える神経が不安水準の調節に関与していることが、報告されていました。そこで今回、「慢性痛によって分界条床核から視床下部外側野に情報を伝える神経の働きが変化することで、持続的な不安が引き起こされる」という仮説を立て、検証しました。
研究手法・研究成果
分界条床核から視床下部外側野に情報を伝える神経の働きが、慢性痛によってどのような影響を受けるかを調べました。マウスの坐骨神経を部分的に糸で縛り、切断することにより、神経障害性疼痛モデルマウスを作製しました。
こうして4週間にわたる慢性痛を誘導したあと、単一の神経細胞の活動状態を計測できる電気生理学的手法を用いて、視床下部外側野に情報を伝える分界条床核神経の活動状態を解析しました。その結果、該当の分界条床核神経は、慢性痛時に持続的に抑制されていることがわかりました。ケモジェネティクスと呼ばれる先端的な神経活動操作法を用いて、視床下部外側野に情報を伝える分界条床核神経を人為的に活性化することで、慢性痛により亢進した不安が軽減されました。一方、ケモジェネティクスにより該当する分界条床核神経を抑制することで、慢性痛を与えていないマウスの不安水準が亢進しました。これらの結果は、当初の仮説を支持する研究成果です。
次に、慢性痛時に視床下部外側野に情報を伝える分界条床核神経が持続的に抑制される神経機構を明らかにするため、上流にある神経細胞での変化を検討しました。遺伝子改変動物とオプトジェネティクス*4と呼ばれる先端的神経活動操作法を用いて、マーカーとしてCocaine- and Amphetamine-Regulated Transcript(CART)*5と呼ばれる神経ペプチドを産生する分界条床核神経細胞を人為的に活性化させました。すると、該当の分界条床核神経への抑制性入力が増加したことから、CARTを産生する分界条床核神経細胞が、該当の分界条床核神経の上流に位置している抑制性神経であることが明らかになりました。慢性痛時におけるCART産生神経細胞の活動を電気生理学的手法により検討したところ、健常マウスと比較して、神経活動が亢進していました。さらに、ケモジェネティクスを用いてCART産生神経細胞の活動を抑制することにより、慢性痛の影響を受け亢進した不安が軽減されました。
これらの結果から、慢性痛モデルマウスでは、分界条床核内のCART産生神経細胞の活動が亢進し、視床下部外側野に情報を伝える分界条床核神経を持続的に抑制することにより、不安が亢進していると解明されました(本研究の概念図)。
今後への期待
慢性痛が不安を引き起こす脳内神経回路の機能変化を明らかにした本研究成果は、慢性痛の治療だけでなく、慢性ストレスなどにより引き起こされる不安障害・うつ病などの精神疾患の治療にも役立つ、新しい治療薬の開発や、脳内神経回路をターゲットとしたニューロモデュレーションなどの治療法の開発に貢献することが期待されます。
謝辞
本研究は、日本学術振興会科研費JP20H03389(基盤B)、JP19K22477(挑戦的研究(萌芽))、JP21K19318(挑戦的研究(萌芽))、JP20J14256(特別研究員奨励費)、日本医療研究開発機構(AMED)の、革新的先端研究開発支援事業「画期的医薬品等の創出をめざす脂質の生理活性と機能の解明」研究開発領域(21gm0910012s0105)、及び、ムーンショット型研究開発事業「目標7:2040年までに、主要な疾患を予防・克服し100歳まで健康不安なく人生を楽しむためのサステイナブルな医療・介護システムを実現」(JP21zf0127004)の助成を受けたものです。
論文情報
- 論文名
- Chronic pain-induced neuronal plasticity in the bed nucleus of the stria terminalis causes maladaptive anxiety(慢性痛による分界条床核内神経可塑的変化は不適応による不安を引き起こす)
- 著者名
- 山内直紀¹、佐藤圭一郎¹、佐藤健太¹、村川俊作¹、濱崎友美¹、野村洋¹、天野大樹¹、 南雅文¹(¹北海道大学大学院薬学研究院)
- 雑誌名
- Science Advances(アメリカ科学振興協会のオープンアクセスジャーナル)
- DOI
- 10.1126/sciadv.abj5586
- 公表日
- 日本時間2022年4月28日(木)午前4時(米国東部時間2022年4月27日(水)午後2時)(オンライン公開)
用語解説
- *1 分界条床核
- 脳の部位の名称。扁桃体とともに不安・恐怖・抑うつなどのネガティブな情動の惹起に関与することが知られている。
- *2 視床下部外側野
- 脳の部位の名称。視床下部は間脳に位置し、内分泌や自律機能の調節を担う。外側野は不安などの情動の調節に関与するほか、摂食や睡眠・覚醒の調節にも関与している。
- *3 ケモジェネティクス
- 化学遺伝学あるいは薬理遺伝学と訳される。哺乳類が有する受容体のアミノ酸配列に変異を導入することで、哺乳類が有する内在性リガンドが結合せず、外来性に投与した薬物により操作できる改変受容体を、ウイルスベクターやトランスジェニックなどの手法を用いて、特定の神経細胞集団等に発現させると、薬物投与により目的とする神経細胞の活動を上昇あるいは低下させることができる。
- *4 オプトジェネティクス
- 光遺伝学と訳される。特定の波長の光刺激によりイオン透過性が上昇する、哺乳類には本来存在しないチャネル分子などを、ウイルスベクターやトランスジェニックなどの手法を用いて、特定の神経細胞集団等に発現させると、光刺激により目的とする神経細胞の活動を上昇あるいは低下させることができる。
- *5 Cocaine- and Amphetamine-regulated transcript(CART)
- 神経ペプチドの一種。分界条床核内で特定の神経細胞集団において産生されているため、本研究では特定の神経細胞集団の活動を操作するためのマーカーとして用いた。
お問い合わせ先
北海道大学大学院薬学研究院 教授 南 雅文(みなみ まさぶみ)
配信元
北海道大学社会共創部広報課
AMED事業に関すること
日本医療研究開発機構 シーズ開発・研究基盤事業部 革新的先端研究開発課