 生物化学工学
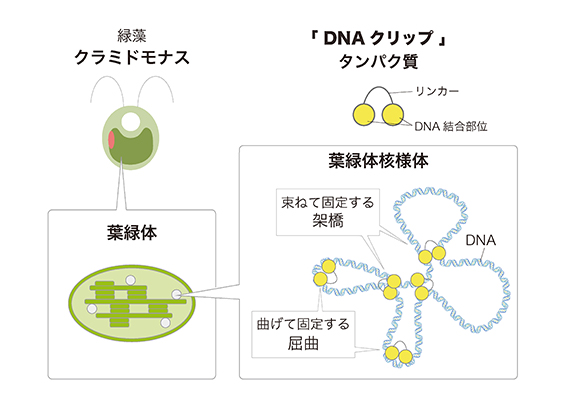
生物化学工学 葉緑体核様体をコンパクトに折りたたむ「DNAクリップ」の発見
緑藻クラミドモナスの葉緑体核様体の解析から、葉緑体DNAを折りたたむタンパク質「DNAクリップ」を発見した。
 生物化学工学
生物化学工学  生物化学工学
生物化学工学  医療・健康
医療・健康  医療・健康
医療・健康  生物化学工学
生物化学工学  医療・健康
医療・健康  生物化学工学
生物化学工学  細胞遺伝子工学
細胞遺伝子工学 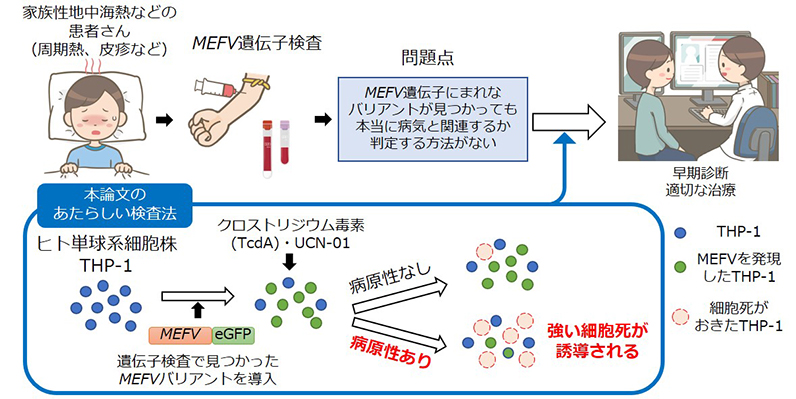 医療・健康
医療・健康 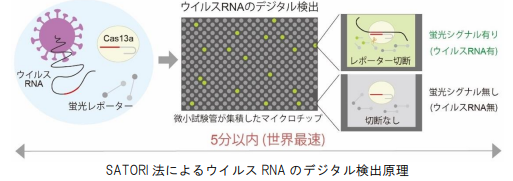 有機化学・薬学
有機化学・薬学  医療・健康
医療・健康 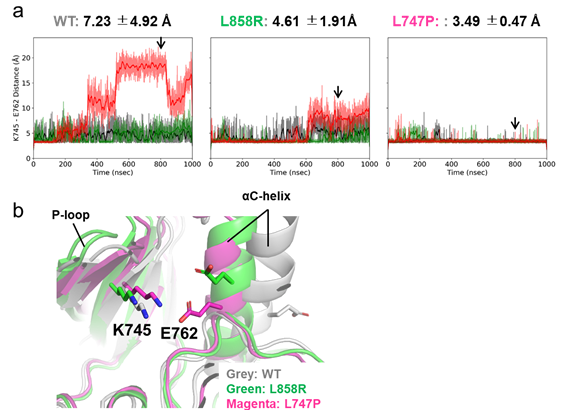 有機化学・薬学
有機化学・薬学