2022-10-28日本電子株式会社,日本医療研究開発機構
日本電子株式会社(本社:東京都昭島市、代表取締役社長兼CEO:大井泉、以下「日本電子」)が代表機関となり、2018年3月に国立研究開発法人日本医療研究開発機構(以下「AMED」)と委託研究開発契約を締結した医療研究開発革新基盤創成事業(以下「CiCLE」)における課題「タンパク質構造解析のハイスループット化へ向けた装置開発」において、計画通りに高速撮影可能なクライオ電子顕微鏡(以下「クライオ電顕」)を開発し、当初目的を達成しました。
課題の背景と目標
クライオ電顕※1を用いて単粒子像解析※2によるタンパク質分子の構造解析を高分解能で行うためには、タンパク質分子を氷薄膜に包埋した凍結試料グリッド※3のクライオ電顕像を数千枚取得する必要があります。プロジェクト開始当初はクライオ電顕による画像取得スループットは1時間あたり40~50枚であり、データ取得に数日を必要としました。創薬の加速化を視野に入れ、クライオ電顕によるタンパク質構造解析のスループット改善を目的として以下を実施しました。
- AIを用いた試料選別ソフトの開発
- 試料移動後のドリフト※4が収まるまでの待機時間を減らすクライオステージ※5の開発
- データ取得の新しいワークフロー開発
課題の成果
本プロジェクトは大阪大学(以下「阪大」)、理化学研究所SPring-8センター、および阪大蛋白質研究所を分担機関として実施されました。
AIを用いた試料選別ソフトの開発は阪大が中心となり、理化学研究所SPring-8センターおよび阪大において様々なタンパク質の電顕像を学習データとして取得し、凍結試料グリッドの良否を自動選別できるソフトウェアを開発しました。
試料移動後のドリフトが収まるまでの待機時間を減らすゴニオメータの開発は日本電子が担当し、試料移動後のドリフト量を低減(従来比約半分)させる新クライオステージを開発しました。
データ取得の新しいワークフロー開発は阪大を中心として行われ、電子ビームの高速制御による多数像の高速撮影によりクライオステージの移動頻度を低く抑える方法を見出しました。
以上により、1時間あたりの画像取得スピードとして毎時約1200枚を達成し、プロジェクト開始時に比べて約20~30倍の高速化に成功したことになります。
課題の意義
毎時約1200枚の画像取得能力は、先行する海外メーカーのスループットを大幅に(2倍以上)超えるものです。本プロジェクトにより国産電子顕微鏡の競争力が大きく向上したと言えます。また、本プロジェクトを通して単粒子像解析の講習会を阪大蛋白質研究所が中心となって実施しました。これらによりクライオ電子顕微鏡装置の性能向上だけでなく、ユーザーコミュニティー全体のボトムアップに繋がったと考えています。

図1 クライオ電顕(CRYO ARM™300)の外観
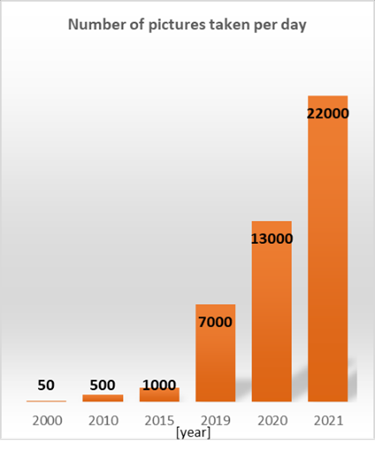
図2 スループットの変遷(1日に取得できる画像枚数)
今後の展望
今後、製薬企業およびアカデミアを含む研究組織にクライオ電顕を使用していただき、改善点についてフィードバックを得ながら装置およびワークフローのブラッシュアップを継続していきます。これにより将来的に創薬に要する期間の短縮を目指します。
用語解説
- ※1 クライオ電顕
- 試料を液体窒素温度に冷却しながら観察が行える透過電子顕微鏡。
- ※2 単粒子像解析
- 凍結試料グリッドの氷薄膜中に分散した分子(単粒子)像を液体窒素温度にて撮影した電子顕微鏡画像から、画像解析によってその三次元構造を解析する手法。
- ※3 凍結試料グリッド
- 微小孔カーボン薄膜搭載グリッド上で、微小孔カーボン薄膜中にタンパク質分子などの水溶液薄膜を形成させ急速凍結して、タンパク質分子等を非晶質の氷薄膜に包埋した透過電子顕微鏡用の試料。
- ※4 ドリフト
- クライオステージ上の凍結試料グリッドの観察位置を変更させるためにグリッドを移動した後、完全に停止するまでの間に試料がゆっくりと動く現象。
- ※5 クライオステージ
- 透過電子顕微鏡の試料を保持し、液体窒素により試料を冷却する機構を持ち、さらに観察位置を変更させるための駆動機構を備えたもの。
本件に関するお問い合わせ先
課題内容に関するお問い合わせ
日本電子株式会社
経営戦略室
コーポレートコミュニケーション室
広報・ブランドグループ
AMED事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
革新基盤創成事業部 計画調整課