2022-11-30 東京大学
発表者
平野 里奈(東京大学定量生命科学研究所クロマチン構造機能研究分野・特任研究員)
胡桃坂 仁志(東京大学定量生命科学研究所クロマチン構造機能研究分野・教授)
江原 晴彦(理化学研究所生命機能科学研究センター転写制御構造生物学研究チーム・研究員)
関根 俊一(理化学研究所生命機能科学研究センター転写制御構造生物学研究チーム・チームリーダー)
発表のポイント
- 染色体の中でDNAの折りたたみを担うリンカーヒストン(H1)が、遺伝子の読み取り装置であるRNAポリメラーゼIIにどのような作用を及ぼすのかについては、ほとんど明らかにされていませんでした。
- RNAポリメラーゼIIが、H1により折りたたまれたDNAを読み取る様子(立体構造)を、クライオ電子顕微鏡を用いて解析しました。その結果、H1がRNAポリメラーゼIIの反応を一時停止させることを明らかにしました。
- H1の存在量の異常やH1のアミノ酸配列の変異は、細胞のがん化に関与していると考えられています。そのため本研究は、H1の関わるがん化のメカニズムの解明につながることが期待されます。
発表概要
東京大学定量生命科学研究所クロマチン構造機能研究分野の平野里奈 特任研究員、胡桃坂仁志 教授らの研究チームは、理化学研究所生命機能科学研究センターの江原晴彦 研究員、関根俊一 チームリーダーとの共同研究で、RNAポリメラーゼIIが、リンカーヒストン(H1)により折りたたまれたDNAの遺伝情報を読み取る仕組みを解明しました。
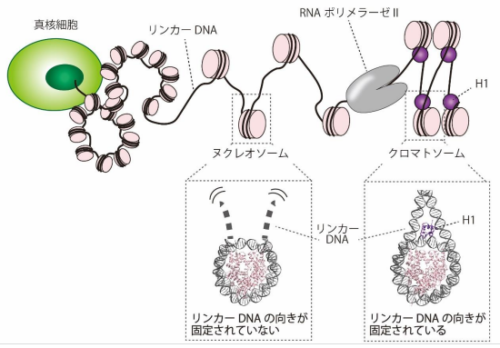
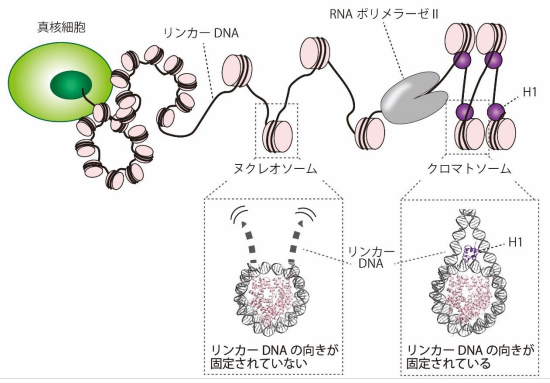
ヒトを含む高等真核生物のDNAは、コアヒストンに巻き付いたヌクレオソームを形成しています。ヌクレオソームはH1が結合することによって、DNAがさらに折りたたまれた構造体であるクロマトソームを形成します。DNAの遺伝情報が機能するには、H1によるクロマトソーム形成によって折りたたまれたDNAを、その読み取り装置であるRNAポリメラーゼIIによりメッセンジャーRNAへと写し取る(転写する)必要があります。しかし、クロマトソームに折りたたまれたDNAの転写の際に、H1がRNAポリメラーゼIIにどのような作用を及ぼすのかについては、未だに明らかにされていませんでした。
そこで本研究チームは、RNAポリメラーゼIIがクロマトソームのDNAを転写する反応を試験管内で再現し、その転写反応過程の様子を、クライオ電子顕微鏡を用いた立体構造解析により解明しました。今回明らかになった立体構造から、RNAポリメラーゼIIがクロマトソームを転写する際に、H1がRNAポリメラーゼIIの進行を一時停止させる様子が明らかとなりました。
H1存在量の異常やH1のアミノ酸配列の変異は、がん化と密接に関連していることが知られています。H1は転写量を制御する因子であるため、これらのH1の異常による転写制御の不具合は、がん化に関わると考えられます。そのため、本成果は、H1の異常によって引き起こされるタイプの細胞がん化のメカニズムの理解につながる事が期待されます。
本研究は主に、国立研究開発法人日本医療研究開発機構(AMED)の創薬等ライフサイエンス研究支援基盤事業(BINDS)「エピジェネティクス研究と創薬のための再構成クロマチンの生産と性状解析」(代表:胡桃坂仁志、JP21am0101076)と「クライオ電子顕微鏡による分子・細胞構造解析の支援と高度化」(代表:吉川雅英、JP22ama121002j001)、日本学術振興会(JSPS)の新学術領域研究「遺伝子制御の基盤となるクロマチンポテンシャル」(代表:胡桃坂仁志、JP18H05534)、基盤研究(B)「転写と共役したヌクレオソーム再構築の分子メカニズムの解明」(代表:江原晴彦、JP20H03201)、基盤研究(A)「クロマチン上で起こる転写と共役した二重鎖切断修復の分子機構の解明」(代表:胡桃坂仁志、JP20H00449)、基盤研究(S)「転写と中核的な生命機能を結びつける高次複合体の構造基盤」(代表:関根俊一、JP20H05690)、「クライオ電子顕微鏡によるネイティブなセントロメアクロマチンの立体構造解析」(代表:滝沢由政、JP22K06098)、および国立研究開発法人科学技術振興機構(JST)の戦略的創造研究推進事業(ERATO)「胡桃坂クロマチンアトラスプロジェクト」(研究総括:胡桃坂仁志、JPMJER1901)の支援を受けて実施されました。