2025-06-20 コペンハーゲン大学(UCPH)
<関連情報>
- https://news.ku.dk/all_news/2025/06/vaccine-disguised-as-a-virus-tricks-the-body-into-stronger-immunity/
- https://www.nature.com/articles/s41565-025-01889-1
抗原提示カプシドウイルス様粒子をコードするモジュール型mRNAワクチンプラットフォームがマラリア抗原Pfs25の免疫原性を高める A modular mRNA vaccine platform encoding antigen-presenting capsid virus-like particles enhances the immunogenicity of the malaria antigen Pfs25
Cyrielle Fougeroux,Sven Hendrik Hagen,Louise Goksøyr,Kara-Lee Aves,Anna Kathrine Okholm,Candice Morin,Abhijeet Girish Lokras,Saahil Sandeep Baghel,Camilla Foged,Marga van de Vegte-Bolmer,Geert-Jan van Gemert,Matthijs M. Jore,Elena Ethel Vidal-Calvo,Tobias Gustavsson,Ali Salanti,Thor Grundtvig Theander,Morten Agertoug Nielsen,Willem Adriaan de Jongh & Adam Frederik Sander Bertelsen
Nature Nanotechnology Published:14 May 2025
DOI:https://doi.org/10.1038/s41565-025-01889-1
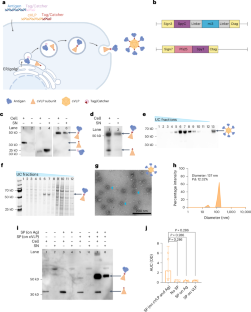
Abstract
The COVID-19 pandemic has emphasized the potential of mRNA vaccines in fighting pandemics, owing to their rapid development, strong immunogenicity and adaptability. However, a drawback is their dose-limiting reactogenicity and inability to generate durable humoral immunity. Here we introduce a modular nucleotide vaccine platform combining the advantages of genetic and capsid virus-like-particle-based vaccines. This platform allows for the display of various antigens on different capsid virus-like particles, improving the magnitude, quality and longevity of the vaccine-induced immune responses. We applied this technology to enhance the immunogenicity of the Pfs25 antigen. Immunization with lipid-nanoparticle-formulated mRNA encoding Pfs25 capsid virus-like particles resulted in higher and potentially more durable anti-Pfs25 antibody responses, along with enhanced functional activity, compared with an mRNA vaccine encoding soluble Pfs25. By improving both humoral and cellular immune responses, this approach may reduce the dose and number of administrations required for effective protection. As a result, it can improve the feasibility of both DNA- and mRNA-based vaccines targeting pandemic and endemic infectious diseases.