2026-03-13 北海道大学,微生物化学研究所
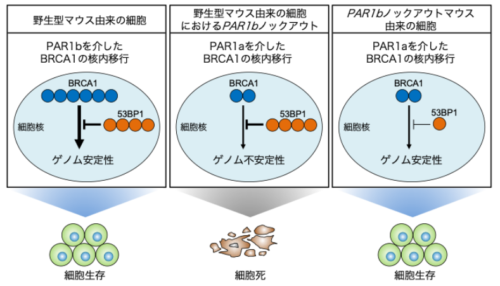
図 1. 本研究の概要図
<関連情報>
- https://www.hokudai.ac.jp/news/2026/03/post-2221.html
- https://www.hokudai.ac.jp/news/pdf/260313_pr2.pdf
- https://www.nature.com/articles/s41598-026-39737-4
PAR1bノックアウトマウスの生存における、PAR1キナーゼファミリーの二つのメンバーであるPAR1bとPAR1aの間の潜在的な冗長性 Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice
Naoko Murata-Kamiya,Adriana Alejandra Del Valle Lazarte,Ippei Kikuchi & Masanori Hatakeyama
Scientific Reports Published:12 March 2026
DOI:https://doi.org/10.1038/s41598-026-39737-4
Abstract
The PAR1/MARK family of serine/threonine kinases (PAR1a-d) redundantly controls the cell polarity. PAR1b also mediates the phosphorylation of BRCA1, which promotes its nuclear translocation. In the nucleus, BRCA1 protects stalled replication forks and repairs double-strand DNA breaks via homologous recombination. Consequently, conventional BRCA1-knockout mice are embryonically lethal. In contrast, conventional PAR1b-knockout mice reach adulthood, suggesting a compensatory mechanism for PAR1b in regulating BRCA1 in these knockout mice. Here we find that, while PAR1b knockout in embryonic fibroblasts (MEFs) derived from wild-type mice elicits growth inhibition/death, MEFs lacking PAR1b can be readily established from conventional PAR1b-knockout mice. In PAR1b-null MEFs from PAR1b-knockout mice, PAR1a, but not PAR1c and PAR1d, becomes essential for survival and expansion. Thus, PAR1a-mediated cryptic redundancy, most likely due to BRCA1 phosphorylation by PAR1a, is unleashed only when functional PAR1b is absent from the earliest stages of embryogenesis, which induces significant epigenetic changes in gene regulation, including 53BP1 silencing. Reduced 53BP1 diminishes the role of BRCA1 in genome protection, thereby contributing to the survival of conventional PAR1b-knockout mice, in which PAR1a only partially compensates for the function of PAR1b in BRCA1 regulation. This study presents the first evidence of epigenetic modification-driven cryptic redundancy during early embryogenesis.