2019-07-03 国立国際医療研究センター
発表のポイント
- マウスの造血幹細胞の細胞周期を生体内と同様に静止期に維持したまま1ヶ月にわたり機能を保つ培養ができるようになった。
- 十分な脂質の供給、低サイトカイン、低酸素が必要最小限の要素であることを明らかにした。
- 本発見により、生体外でより体内の状況に近い環境で造血幹細胞の研究を行うことが可能となり、増幅させた造血幹細胞を静止期に戻す方法の開発や白血病発症の初期過程の研究への応用が期待される。
発表の概要
国立国際医療研究センター研究所の田久保 圭誉 プロジェクト長・小林 央 上級研究員(生体恒常性プロジェクト)を中心とした研究チーム(慶應義塾大学と九州大学との共同研究チーム)は、マウスおよびヒト骨髄(注1)検体を用いた研究から、造血幹細胞(注2)を体内の環境に近い培養条件で培養することで、細胞周期を静止期(注3)に維持したまま1ヶ月にわたり機能を保つことができるようになりました。
研究の背景
造血幹細胞は、全ての血液細胞を一生涯にわたり供給することができる細胞です。造血幹細胞自身は、生体内では細胞分裂をほとんどせずに(細胞周期の静止期にあります)、骨髄の中で生存しています。造血幹細胞は血液疾患を根治する際の骨髄移植(造血幹細胞移植)に必須の細胞で、これまで造血幹細胞を体外で培養して増やす試みが数多く行われてきて、近年の研究の進展から造血幹細胞を増幅することにはある程度可能となってきました。一方で、造血幹細胞を培養下において生体内と同様に静止期に維持する技術を開発することは、造血幹細胞の性質をより生理的な条件で明らかにする上で重要なものの、増幅させる方法に比べて多くは研究されてきませんでした。本研究チームは造血幹細胞の培養条件を様々に検討し、より生体の骨髄内に近い環境条件で培養することで造血幹細胞を静止期に維持する方法の開発を試みました。
本研究の概要・意義
1)従来の造血幹細胞培養法では脂肪酸の供給が不足している(図1)
マウスの造血幹細胞の培養は無血清、少量のアルブミン、十分なサイトカイン(SCFとTPO、(注4))によって従来培養されていましたが、この条件下では長期に造血幹細胞を維持できませんでした。そこで本研究グループでは、培養した造血幹細胞が骨髄から取り出したばかりの造血幹細胞と何が異なるかをcDNAマイクロアレイ解析によって探索しました。その結果、培養した後の造血幹細胞では脂肪酸を合成する酵素の遺伝子発現が上昇しており、現在の培養条件では脂肪酸が不足していることがわかりました(図1)。
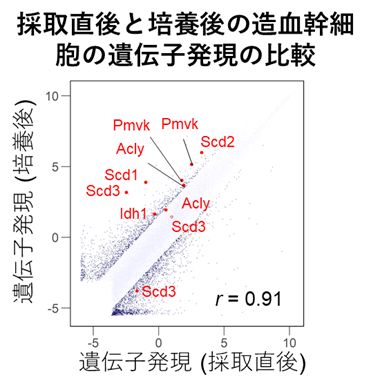
図1:培養後の造血幹細胞では脂肪酸合成関連遺伝子の発現が上昇している。
2)アルブミンは骨髄の中に浸透し脂肪酸の供給源となり得る
アルブミンは血液の中で最も豊富に含まれるタンパク質で、脂肪酸を体全体の細胞に届ける役割があることは古くから知られていましたが、骨髄組織の中にまでアルブミンが到達しうるかを、生体イメージング技術を用いて改めて検討しました。その結果蛍光色素を結合させたアルブミンをマウスに注射すると時間とともに骨髄の中に浸透し、アルブミンが生理的な環境で骨髄に分布することを示しました(図2)。アルブミンが少ない培地で培養した造血幹細胞は脂肪酸の合成を阻害する薬剤を添加するとほとんど生存できませんでしたが、アルブミンを十分に加えた環境では、脂肪酸の合成を阻害してもほとんど生存に影響がありませんでした(図3)以上の結果から、培養液の中に脂肪酸の供給源として十分なアルブミンを加えることは造血幹細胞の生理的な環境を再現するために必要と考えられました。
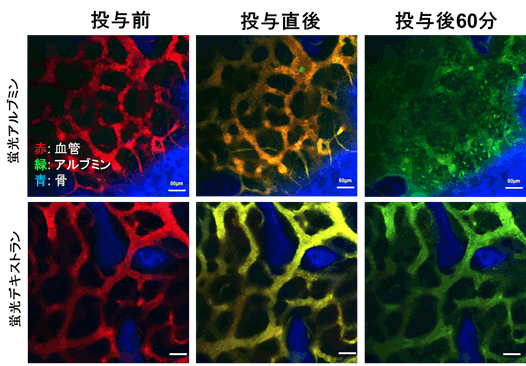
図2:マウスの頭蓋骨の骨髄を生きたまま多光子レーザー顕微鏡で観察しながら、蛍光標識したアルブミンを投与して骨髄の中への分布を見た。蛍光アルブミンは骨髄の血管の外に分布したのに対して分子量がより大きいデキストランは血管内に留まった。
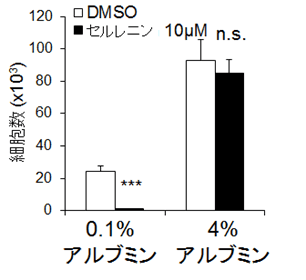
図3:造血幹細胞をセルレニン(脂肪酸合成阻害薬)の存在下で7日間培養した際の、低いアルブミン濃度(0.1%)と高いアルブミン濃度(4%)の細胞数の比較。0.1%のアルブミン濃度ではセルレニンにより造血幹細胞はほとんど増殖できなかったのに対して、高いアルブミンの存在下ではセルレニンの影響は見られなかった。***, P値<0.001、n.s. 統計的有意差なし。
3)造血幹細胞を静止期に維持するためには低いサイトカイン濃度が必要
造血幹細胞の生存にはSCFとTPOのサイトカインが重要であることは以前から知られており、これまでの培養においてもこの二種のサイトカインが中心的に用いられてきましたが、体内で静止期を維持している濃度はわかっていませんでした。また骨髄の中は酸素濃度が低いことが知られていたので、低酸素と高酸素のそれぞれの環境で、かつ十分に脂質の供給があるアルブミン濃度において、造血幹細胞が静止期に維持されるSCFとTPOの濃度を決定しました(図4)。その結果、SCF、TPOが従来用いられている濃度よりも遥かに低い濃度において造血幹細胞が分化・増殖せずに維持されることがわかりました。
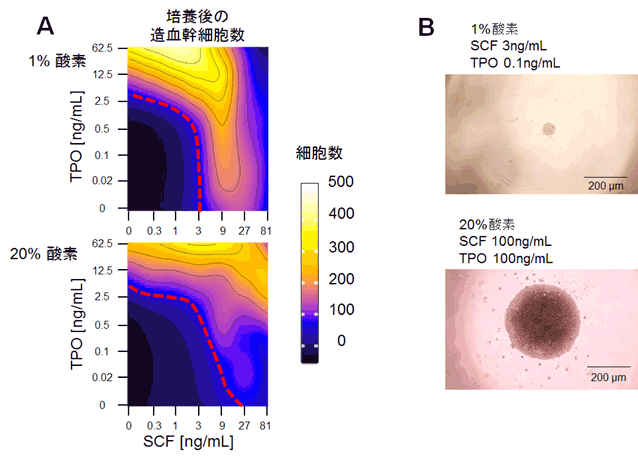
図4
(A)マウス造血幹細胞300個を7日間、さまざまなサイトカイン濃度で培養した後の造血幹細胞数。上段は骨髄と同様の低酸素、下段は高酸素条件。造血幹細胞が静止期を維持したまま数が保たれるのは赤い点線で示している。
(B)低酸素、低サイトカイン濃度(上段)および高酸素、高サイトカイン濃度(下段)で培養した後の造血幹細胞のコロニー。上段ではほとんど細胞が増殖していない(=静止期にある)。
このようにして決定した、高いアルブミン濃度、低い酸素濃度、低いサイトカイン濃度において造血幹細胞の機能が保たれているかを確認するために、造血幹細胞を別のマウスに移植する骨髄移植の実験を行ったところ、確かに低いサイトカイン濃度で1ヶ月にわたり培養した造血幹細胞は採取直後の造血幹細胞に匹敵する能力を維持していました(図5)。ヒトの骨髄由来の造血幹細胞においても類似の高アルブミン、低酸素、低サイトカイン濃度において静止期を維持したままある程度機能を維持することも確認できました。
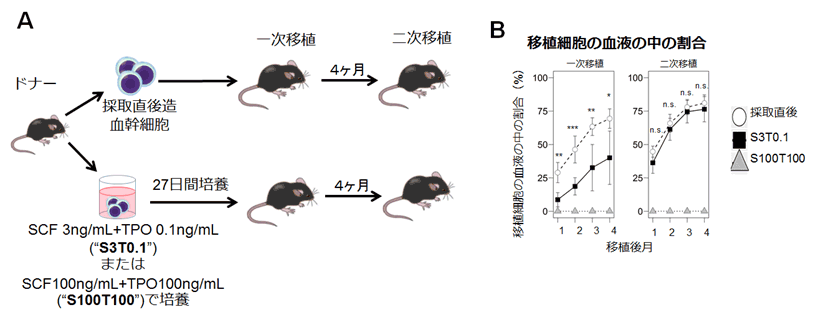
図5
(A)マウス造血幹細胞を一匹あたり500個ずつ放射線照射したマウスに移植して、造血幹細胞が血液細胞を作る能力を評価した。採取直後の造血幹細胞および、低サイトカイン(SCF 3ng/mL, TPO 0.1ng/mL)もしくは高サイトカイン(SCF 100ng/mL TPO 100ng/mL)で27日間培養した後に移植した。
(B)一次移植および二次移植(一次移植したマウスの骨髄から細胞を分取し別の放射線照射したマウスに移植)した後の、移植細胞由来の白血球の割合を測定した。低サイトカイン条件で培養した造血幹細胞は採取直後の細胞に近いレベルで血液が造られているのに対し、従来の高サイトカイン条件ではほとんど血液を作る能力は失われていた。
今後の展望
本研究チームは、生体内の造血幹細胞の振る舞いを模倣するためにさまざまな培養条件を検討した結果、高アルブミン濃度、低サイトカイン濃度、低酸素環境において生体内と同様に静止期を維持した造血幹細胞の培養が可能であることを見出しました。これにより、生体外でより体内の状況に近い環境で造血幹細胞の研究を行うことが可能となり、増幅させた造血幹細胞を静止期に戻す方法の開発や、造血幹細胞に由来するタイプの白血病が発症する過程の研究への応用が期待されます。
用語解説
- (注1)骨髄:
- 全身の骨の硬い部分の内側を骨髄と呼び、血液は骨髄で作られる。若いときは手足の骨を含む全身の骨髄で血液を作るが、年をとるにつれて、背骨、骨盤、胸骨などの一部の骨だけで血液を作るようになる。
- (注2)造血幹細胞:
- 哺乳動物の成体では骨髄に存在している数少ない細胞で、細胞分裂することで生涯に渡り血液を供給している。骨髄の血液細胞10万個に1個程度の割合で存在する。
- (注3)静止期:
- 細胞は分裂することによって数を増やしていく。細胞分裂する周期のことを細胞周期と呼び、G1期、S期、G2期、M期に分かれているが、細胞が分裂しない状態のことを細胞周期の静止期(G0期)と呼び他の細胞周期と区別する。
- (注4)サイトカイン:
- 細胞表面の受容体に結合することで、細胞に増殖や分化等の信号を伝える。通常は標的となる細胞とは異なる細胞から分泌される。本研究で用いたSCF(ステムセルファクター)、TPO(トロンボポエチン)もサイトカインの一種。
本研究への支援
本研究は、下記機関・研究費より主に支援を受けて実施されました:
- 日本医療研究開発機構(AMED)
- 再生医療実現化拠点ネットワークプログラム「造血幹細胞の代謝制御メカニズム解明と機能増強法の探索」(18bm0704011)
遺伝子・細胞治療研究開発基盤事業「革新的幹細胞培養技術に基づいた造血幹細胞遺伝子編集の開発研究」(18ae0201014)
- 文部科学省
- 科学研究費補助金 新学術領域研究・ステムセルエイジングから解明する疾患原理「ニッチ-幹細胞相互作用による造血系抗老化システムの解明」(26115005)
- 日本学術振興会
- 科学研究費補助金基盤研究(B)「造血幹細胞ニッチ因子としての代謝物の時空間構成と機能解明」(18H02845)
- 国立国際医療研究センター
- 国際医療研究開発費 (26-001, 29-2007)
発表雑誌
- 雑誌名:
- Cell Reports
- 論文名:
- Environmental Optimization Enables Maintenance of Quiescent Hematopoietic Stem Cells Ex Vivo
- 著者:
- Hiroshi Kobayashi, Takayuki Morikawa, Ayumi Okinaga, Fumie Hamano, Tomomi Hashidate-Yoshida, Shintaro Watanuki, Daisuke Hishikawa, Hideo Shindou, Fumio Arai, Yasuaki Kabe, Makoto Suematsu, Takao Shimizu, and Keiyo Takubo
- 掲載日:
- 米国東部標準時間7月2日午前11時(日本時間7月3日午前1時)に、オンライン掲載予定。
- 参照URL:
- Cell Reportsホームページ (http://cellreports.cell.com)
お問い合わせ先
本件に関するお問い合わせ先
国立国際医療研究センター研究所 生体恒常性プロジェクト
責任著者役職名 田久保 圭誉(たくぼ けいよ)プロジェクト長
取材に関するお問い合わせ先
国立国際医療研究センター 広報企画室
担当:三山 剛史
AMED事業に関するお問い合わせ先
日本医療研究開発機構(AMED)
戦略推進部 再生医療研究課