難治性がん治療薬の開発に期待
2020-03-16 京都大学
金井雅史 医学研究科特定准教授、掛谷秀昭 薬学研究科教授、株式会社セラバイオファーマらの研究グループは、大腸がんの標準治療薬オキサリプラチンが効かなくなった治療抵抗性大腸がんの動物モデルにおいて、水溶性プロドラッグ型クルクミン(CMG)が顕著な抗腫瘍効果を示すことを明らかにしました。
ショウガ科のウコンに含まれるポリフェノール化合物クルクミンは、がん、心臓病、アルツハイマー等に対する治療薬としての開発が期待されています。本研究グループはすでに、生体内において、CMGがクルクミンのプロドラッグとして利用できることを証明しています。
一方、大腸がんの約40%に認められているKRAS遺伝子変異は、オキサリプラチンに対する治療抵抗性の要因であると考えられており、この治療抵抗性のメカニズムとしてKRAS遺伝子の変異によるNF-κB経路の活性化が挙げられます。クルクミンは、このNF-κB経路及びプロテアソームなどを阻害することが報告されています。そこで本研究グループは、オキサリプラチンに抵抗性を持つヒト結腸腺がんHCT116細胞を移植したマウスゼノグラフトモデルにおいて、CMGの抗腫瘍効果を検討しました。その結果、CMGはオキサリプラチン投与により認められる体重減少、骨髄抑制、肝障害などを伴うことなく、顕著な抗がん活性を示すことが明らかになりました。また、CMGはオキサリプラチンと併用することで、相加的な抗がん効果を示し、オキサリプラチンの副作用を増強しないことも明らかになりました。
CMGは、NF-κB経路及びプロテアソームなどが異常に活性化された難治性がんなどに対して、安全性の高い治療薬としての実用化が期待されます。
本研究成果は、2020年3月12日に、国際学術誌「Cancer Science」のオンライン版に掲載されました。
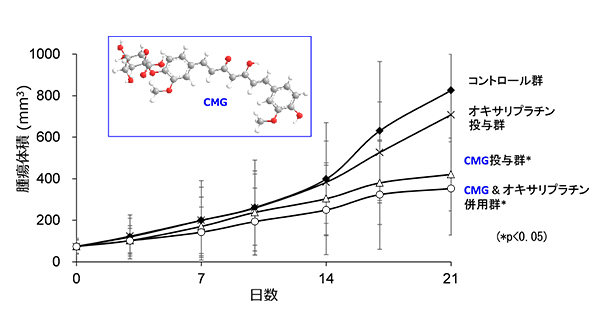
図:CMGは治療抵抗性ヒト結腸がんマウスモデルにおいて抗腫瘍効果を示す
詳しい研究内容について
水溶性プロドラッグ型抗がん剤 CMG の治療抵抗性大腸がんに対する抗腫瘍効果を解明
―難治性がん治療薬の開発に期待―
概要
京都大学医学研究科 金井雅史 特定准教授、京都大学大学院薬学研究科 掛谷秀昭 教授、株式会社セラバイオファーマらの研究グループは、大腸がんの標準治療薬オキサリプラチンが効かなくなった治療抵抗性大腸がんの動物モデルにおいて、水溶性プロドラッグ型クルクミン(CMG)が顕著な抗腫瘍効果を示すことを明らかにしました。
ショウガ科のウコンに含まれるポリフェノール化合物クルクミンは、がん、心臓病、アルツハイマー等に対する治療薬としての開発が期待されています。本研究グループはすでに、生体内において、クルクミンモノグルクロニド( CMG)がクルクミンのプロドラッグとして利用できることを証明しています。
一方、大腸がんの約 40%に認められている KRAS 遺伝子変異は、オキサリプラチンに対する治療抵抗性の要因であると考えられており、この治療抵抗性のメカニズムとして KRAS 遺伝子の変異による NF-κB 経路の活性化が挙げられます。クルクミンは、この NF-κB 経路及びプロテアソームなどを阻害することが報告されています。そこで研究グループは、オキサリプラチンに抵抗性を持つヒト結腸腺がん HCT116 細胞を移植したマウスゼノグラフトモデルにおいて、CMG の抗腫瘍効果を検討しました。その結果、CMG はオキサリプラチン投与により認められる体重減少、骨髄抑制、肝障害などを伴うことなく、顕著な抗がん活性を示すことが明らかになりました。また、CMG はオキサリプラチンと併用することで、相加的な抗がん効果を示し、オキサリプラチンの副作用を増強しないことも明らかになりました。
したがって、CMG は、NF-κB 経路及びプロテアソームなどが異常に活性化された難治性がんなどに対して、安全性の高い治療薬としての実用化が期待されます。
本研究成果は、2020 年 3 月 12 日に日本癌学会オープンアクセスジャーナル「Cancer Science」のオンライン版に掲載されました。
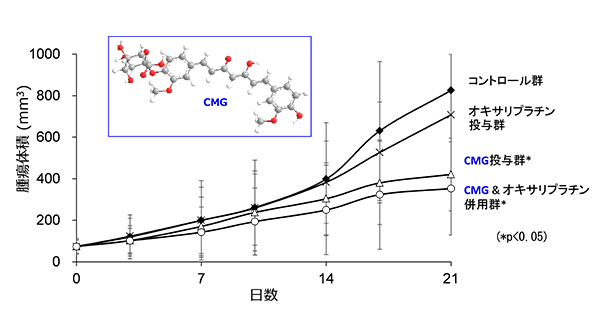
図:CMG は治療抵抗性ヒト結腸がんマウスモデルにおいて抗腫瘍効果を示す
1.背景
ショウガ科のウコンに含まれるポリフェノール化合物クルクミンは、さまざまな生理作用が報告されており、がん、心臓病、アルツハイマー等に関する基礎研究及び臨床研究が行われています。しかし、クルクミン原末をそのまま摂取しても多くは腸管で吸収されないために、血液には移行せず肝臓を含む各種臓器での顕著な効果を期待できません。そこで研究グループは、クルクミンのバイオアベイラビリティー(生物学的利用能)の向上のために精力的な研究を行った結果、生体内において、クルクミンモノグルクロニド(CMG)がクルクミンのプロドラッグとして利用できることを証明しています(図 1、参考文献)。さらに、ヒト結腸腺癌 HCT116 細胞を移植したマウスゼノグラフトモデルにおいて、CMG は体重減少、骨髄抑制、肝障害などの副作用を伴うことなく、顕著な抗がん活性を発揮することも明らかにしています。
2.研究手法・成果
大腸がんの約 40%に認められている KRAS 変異は、抗がん剤オキサリプラチン療法に対する治療抵抗性の要因であると考えられており、この治療抵抗性メカニズムとして KRAS 変異による NF-κB 経路の活性化が挙げられます。一方、クルクミンはこの NF-κB 経路及びプロテアソームなどを阻害することが報告されています。そこで本研究では、オキサリプラチンに抵抗性を持つヒト結腸腺がん HCT116 細胞 (KRAS変異, がん抑制遺伝子p53欠損)を移植したマウスゼノグラフトモデルにおけるCMGの抗腫瘍効果を検討しました。
その結果、CMG は生体内においてクルクミンに変換され、KRAS 変異によって活性化された NF-κB 経路を抑制し、オキサリプラチン投与により認められる体重減少、骨髄抑制、肝障害などを伴うことなく、顕著な抗がん活性を示すことが明らかになりました。また、CMG はオキサリプラチンと併用することで、相加的な抗がん効果を示し、オキサリプラチンの副作用を増強しないことも明らかになりました。
(図 2)
3.波及効果、今後の予定
研究グループはこれまでに、CMG を静脈投与することで、従来のクルクミン原末の経口投与と比較して、クルクミンが極めて高い血中濃度( 約 1,000 倍以上)を示すことを明らかにしています( 参考文献)。さらに、今回、CMG がオキサリプラチン抵抗性大腸がんに顕著な抗腫瘍効果を発揮することを明らかにしました。クルクミンは NF-κB 経路及びプロテアソームなどを阻害することが報告されていますので、 CMG は両経路が異常に活性化された難治性がんなどに対して、安全性の高い治療薬としての実用化が期待されます。
<参考文献>
Ozawa, H. et al. Curcumin β-D-glucuronide plays an important role to keep high levels of free-form curcumin in the blood. Biol. Pharm. Bull. 2017, 40, 1515-1524.
(参考:京都大学プレスリリース「安全性の高い水溶性プロドラッグ型クルクミン(CMG)の開発に成功~抗がん剤などとしての実用化に期待」
URL:http://www.kyotou.ac.jp/ja/research/research_results/2017/ 170901_1.html)
4.研究プロジェクトについて
本研究は、京都大学大学院医学研究科、京都大学大学院薬学研究科、株式会社セラバイオファーマ、東京慈恵会医科大学との共同研究であり、日本学術振興会(JSPS)の支援のもとに行なわれました。
<用語解説>
プロドラッグ:生体内で代謝され活性代謝物となる薬剤。
KRAS 変異:KRAS 遺伝子はがん遺伝子の1つで、KRAS 変異は多くのがんの発生における必須段階である。
オキサリプラチン:白金製剤に分類される抗がん剤。
NF-κB 経路:ストレス、サイトカイン、紫外線などにより活性化される転写因子 NF-κB によって制御されている細胞内シグナル伝達経路。
プロテアソーム:細胞内でタンパク質の分解を行う巨大な酵素複合体。
マウスゼノグラフトモデル:ヒト由来のがん細胞を免疫不全マウスに移植した異種移植動物実験モデル。
<論文タイトルと著者>
タイトル:Curcumin β-D-glucuronide exhibits anti-tumor effects on oxaliplatin-resistant colon cancer with less toxicity in vivo( CMG (Curcumin β-D-glucuronide)は、オキサリプラチン抵抗性大腸がんにおいて、低毒性で抗腫瘍効果を発揮する)
著 者:Hitomi Ozawa-Umeta, Atsuhiro Kishimoto, Atsushi Imaizumi, Tadashi Hashimoto, Tadashi Asakura, Hideaki Kakeya, Masashi Kanai
掲 載 誌:Cancer Science. doi: 10.111/cas.14383
<参考図表>
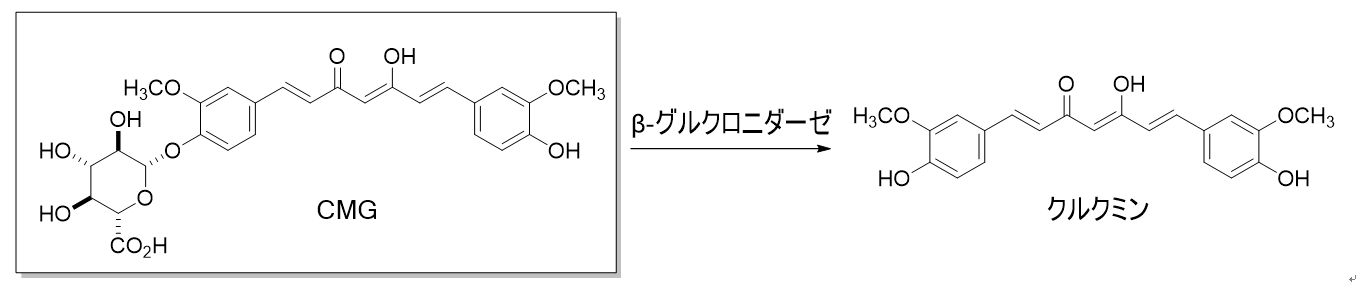
図 1. CMG は生体内においてクルクミンに変換される。
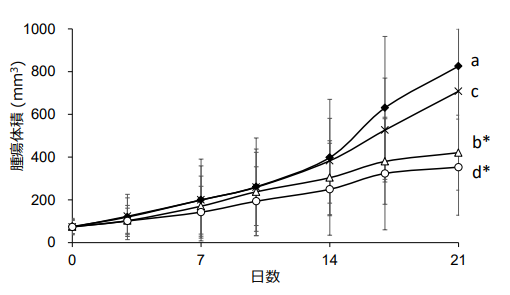
図 2. CMG はオキサリプラチン抵抗性大腸がん( ヒト結腸腺がん HCT116[KRAS 変異, p53 欠損])において抗腫瘍効果を示す。
a. コントロール群, b. CMG 投与群, c. オキサリプラチン投与群, d. CMG・オキサリプラチン併用群 (*p<0.05)