2020-04-21 分子科学研究所
発表のポイント
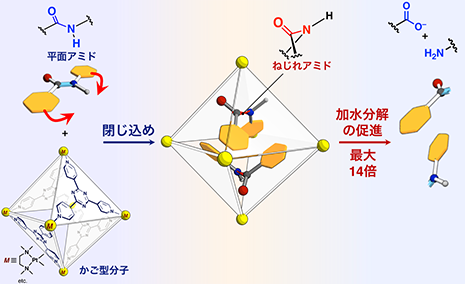
◆アミド分子をかご型分子に閉じ込めてねじることで、加水分解反応の促進に成功。
◆分子の新しい活性化手法として分子変換技術や触媒の開発につながる成果。
◆新しい仕組みの人工酵素やプロドラッグの活性化手法として応用が期待される。
発表概要
東京大学大学院工学系研究科応用化学専攻の竹澤浩気助教、藤田誠教授(東京大学卓越教授/分子科学研究所卓越教授兼任)らは、自己組織化の原理を利用して合成された中空のかご型分子にアミド分子(注1)を閉じ込めることで、アミド結合をねじって(歪ませて)反応を促進させることに成功しました。分子の反応性を高める方法として歪みを利用する方法が注目を集めていますが、これまでは煩雑な化学修飾によって分子に歪みを生み出すことが一般的でした。本手法では、化学修飾をせず、かご型分子に閉じ込めるだけで歪みを生み出すという、これまでにない簡便な方法でアミド結合を活性化する(切れやすくする)ことができました。
アミド結合は、生体内では、アミノ酸同士を連結させてタンパク質をつくりだす重要な結合で、似たようなアミド活性化の仕組みは、生体内において、一部のタンパク質の自己分解などで用いられています。本研究結果は、これらの生体内反応の機構に迫る成果であるといえます。また、本手法を一般化することで、新しい仕組みの人工酵素やプロドラッグ活性化手法としての応用が期待されます。
本研究成果は4月20日(英国夏時間)に英国科学誌「Nature Chemistry」のオンライン版で公開されました。
発表内容
1. 研究の背景と経緯
タンパク質などの生体分子や高分子材料に広く用いられるアミド化合物は、アミド結合周りに平面構造を有し、高い化学安定性を示します。この性質はアミド化合物の有用性の元となっていますが、アミド部位を選択的に反応させて別の分子種に変換することを困難にしています。一方で、アミド結合にねじれを生じさせると、その性質が一変し、加水分解(注2)を起こしやすくなるとされていました。これまで実際に、ねじれたアミド結合をもつモデル化合物が多段階の有機合成によって作られ、その高い反応性が明らかにされてきました。生体内でも、このようなねじれたアミド結合の高い反応性が利用されていると推定されています。一部のタンパク質は、自己分解やスプライシング(注3)において、自身の構造中に含まれる特定のアミド結合をねじることによって選択的に切断していると提唱されています。これらのタンパク質は、人工的に作られたモデル化合物とは異なり、非共有結合性相互作用(注4)を使ってアミドをねじっているとされています。この生体内でアミド結合をねじって活性化する手法に着目し、同様の非共有結合性相互作用に基づいたアミドの活性化を、本研究グループで長年開発・応用してきたかご型分子を用いて行うことを着想しました。すなわち、狭い内部空間を持つかご型分子に閉じ込めることで、アミドをねじれた構造に制限する手法です。
2.研究の内容
通常の溶液中では平面構造をもち不活性なアミド化合物を自己組織化(注5)によって組み上げたかご型分子に閉じ込めることで、アミド結合をねじり、活性化できることを実証しました(図1)。アミド化合物をかご型分子の水溶液と加熱混合すると、かご型分子内に閉じ込められます。これを単結晶X線構造解析(注6)によって解析したところ、アミド化合物が2分子、ねじれた構造でかご型分子の内部に閉じ込められていることがわかりました(図2)。アミド結合周りのねじれは、34°にまで達していました。このようにしてねじられたアミド化合物に対し、加水分解反応を行うと、通常の溶液中(かご型分子なし)に比べて反応速度が約5倍に加速されました。このように、標的の分子をかご型分子に閉じ込めるだけで、分子にねじれを生じさせ、特定の結合を活性化させるという手法はこれまでになく、新しい仕組みでの人工酵素の創出に成功したと言えます。
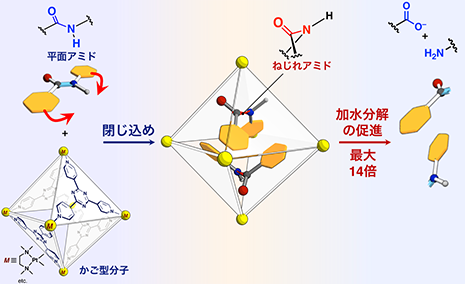
図1 かご型分子へアミドを閉じ込めてねじれを生み出し、加水分解に対する反応性を向上させるイメージ図
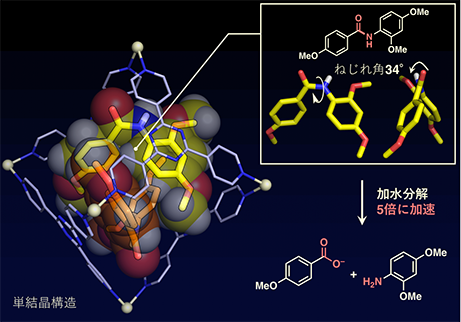
図2 平面アミドをかご型分子に閉じ込めるとアミド結合が 34° までねじられることが、単結晶構造から明らかになった。こうしてねじられたアミドに対し塩基を作用させ加水分解すると、反応速度が約5倍に加速された。
また、特定のアミド分子については、反応に関与しない「詰め物分子」をかご型分子内に同時に閉じ込めることにより、アミド結合のねじれ度合いを精密に制御し、反応性を制御することにも成功しました(図3)。アミド化合物単独ではねじれた構造とねじれていない構造それぞれをとっている2分子がかご型分子に閉じ込められます。これに対し、円錐形の分子を同時に閉じ込めるとアミドは平面構造を、平面状の分子を同時に閉じ込めるとアミドはねじれた構造をとるようになりました。これらについて加水分解の反応速度を調べると、かご型分子なしでの反応に比べ、平面構造のアミドは約3倍の加速にとどまったのに対し、ねじれたアミドは14倍にも加速されました。このように分子の活性化度合いを変化させることができるのは、これまでの手法にない独自の成果であると言えます。本研究は不活性分子の活性化手法として新しいものであり、さまざまな有機反応への応用が期待できます。
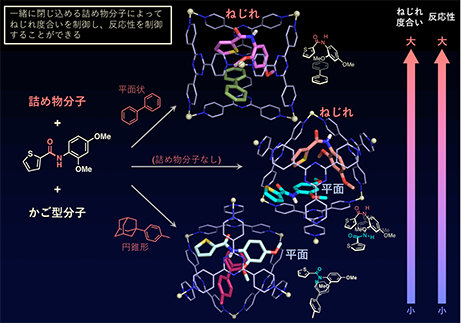
図3 アミドと一緒に詰め物分子をかご型分子に閉じ込めることで、アミドのねじれ度合いを制御し、反応性を制御できる。
3.今後の期待
れまで分子を歪ませて活性化するには、化学結合の力を借りて無理やり歪ませる手法が一般的でした。本研究で示された手法では、アミド分子に対し特別な化学修飾をすることなしに、かご型分子に閉じ込めるという簡便な手法でアミド分子を歪ませ、活性化することができました。今後は、さらなる効率で活性化ができるようなかご型分子を開発したり、他種類の分子へ応用したりすることで、より有用な分子活性化手法として開発をすすめることができます。将来的には、特定の分子の特定の箇所を選択的に切断する、新しい仕組みの触媒としての応用や、生体内でのプロドラッグ(注7)活性化への応用などが期待されます。
発表雑誌
雑誌名: Nature Chemistry (4月20日)
論文タイトル: Enhanced reactivity of twisted amides inside a molecular cage
著者: Hiroki Takezawa*, Kosuke Shitozawa, Makoto Fujita*
DOI番号:10.1038/s41557-020-0455-y
問い合わせ先
東京大学大学院工学系研究科 応用化学専攻
助教 竹澤 浩気
東京大学大学院工学系研究科 応用化学専攻
(分子科学研究所 卓越教授)
教授 藤田 誠
【機関窓口】
東京大学 大学院工学系研究科 広報室
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
用語解説
注1)アミド(結合、化合物)
ここでは、カルボン酸とアミンが縮合してできた結合・化合物を指す。生体分子として代表的なタンパク質は、無数のアミノ酸がアミド結合(ペプチド結合)でつながって形成される。
注2)加水分解
化合物の水による分解反応。ここでは、アミドが水によってアミンとカルボン酸に分解する反応のこと。
注3)スプライシング
直鎖状のポリマーから特定の部分を取り除き、残りの部分を再結合させて組み替える反応。タンパク質は一般に、アミノ酸がアミド(ペプチド)結合によって一本鎖に連なった構造をとっている。タンパク質においても途中に位置する部位が切り離され、その両端部分が再連結するスプライシング反応が知られている。一部のタンパク質では、このスプライシング反応に歪んだアミド結合が重要な役割を果たしていることが提唱されている。
注4)非共有結合性相互作用
共有結合以外の比較的弱い相互作用。生体分子の高次構造の形成や分子認識に用いられる可逆的な相互作用。
注5)自己組織化
複数の分子が分子間での比較的弱い相互作用により自発的に組織や高次構造を作り出すこと。
注6)単結晶X線構造解析
均質な単結晶にX線を照射し、その回折像から分子の三次元的な構造を明らかにする分析手法。分子の形を知ることができる最も強力な分析手法として知られる。
注7)プロドラッグ
体内で代謝されて初めて作用を及ぼす薬。そのままでは薬効を発揮せず、意図した場で分解反応等により薬効を示す形に変化してはたらく。