理化学研究所(理研)環境資源科学研究センター天然物生合成研究ユニットの加藤直樹研究員、ケミカルバイオロジー研究グループの長田裕之グループディレクター、近畿大学農学部の松田一彦教授、大阪府立大学生命環境科学研究科の甲斐建次講師らの共同研究グループ※は、糸状菌の生産する殺虫活性物質オカラミンの殺虫活性に必須な部分構造の特定に成功しました。
本研究成果は、オカラミンの構造をもとにした人や動物に優しい新たな殺虫剤開発に貢献すると期待できます。
オカラミンはペニシリウム属糸状菌の生産する殺虫活性物質であり、無脊椎動物にのみ存在する抑制性グルタミン酸受容体(GluCl)[1]に作用することで、殺虫活性を示します。今回、共同研究グループは、オカラミン生産糸状菌の遺伝子を改変することで、通常の培養では取得困難な生合成中間体などの関連化合物を収集し、それらのグルタミン酸受容体に対する作用を調べました。その結果、「8員環の1,4-ジヒドロアゾシン構造」と「インドール環窒素にプレニル基」を持つことがオカラミンの活性に必須であることが明らかになりました。
本研究成果は、米国の科学雑誌『ACS Chemical Biology』(3月16日号)に掲載されました。
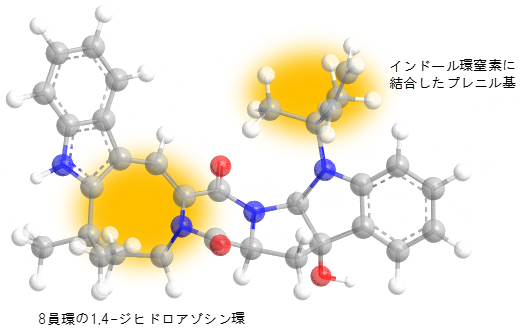
図 オカラミンAの殺虫活性に必須な部分(黄色)
※共同研究グループ
理化学研究所 環境資源科学研究センター
天然物生合成研究ユニット
研究員 加藤 直樹(かとう なおき)
特別研究員 古谷 章悟(ふるたに しょうご)
テクニカルスタッフⅠ 衣笠 清美(きぬがさ きよみ)
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
ケミカルバイオロジー研究グループ
基礎科学特別研究員 大高 潤之介(おおたか じゅんのすけ)
グループディレクター 長田 裕之(おさだ ひろゆき)
近畿大学農学部
大学院生 野口 晃(のぐち あきら)
准教授 伊原 誠(いはら まこと)
教授 松田 一彦(まつだ かずひこ)
大阪府立大学 生命環境科学研究科
講師 甲斐 建次(かい けんじ)
名誉教授 林 英雄(はやし ひでお)
※研究支援
本研究は、科学技術振興会(JSPS)科学研究費補助金・基盤研究A「微生物を介した植物の間接誘導防衛機構の解明にもとづく次世代昆虫制御物質の創出(領域代表者:松田一彦)」、同基盤研究A「微生物二次代謝遺伝子の改変、覚醒による新規生物活性物質の創出(領域代表者:長田裕之)」などによる支援を受けて行われました。
背景
抑制性グルタミン酸受容体(GluCl)は、神経伝達を仲介するリガンド[2]作動性イオンチャネルの一つであり、無脊椎動物にのみ存在します。この受容体は、抗寄生虫薬イベルメクチン[3]の分子標的であることからも注目を集めています。
オカラミンは、糸状菌Penicillium simplicissimum AK40株から発見された殺虫活性物質です。これまでに発見されたオカラミン類の中で、高い殺虫活性を示すオカラミンAとBは8員環のアゾシンを共通して持っており、最も強力な殺虫活性を示すオカラミンBは4員環のアゼチジンを含んだ八環性骨格という非常に珍しい化学構造を持っています(図1)。近年、オカラミンの分子標的がGluClであること、イベルメクチンとは異なり、ヒトのグリシン受容体(GlyR)やγ-アミノ酪酸受容体(GABAAR)に対してほとんど作用を示さないことが分かり、オカラミンが選択性の高い殺虫剤開発のシード化合物となる可能性が示されました。
これまでに国内外の複数の研究グループによって、オカラミンの化学合成が試みられてきましたが、オカラミンAやBといった高い殺虫活性を持つ化合物の全合成の報告はまだありません。その一方で、最近、生産菌であるPenicillium属糸状菌からオカラミンの生合成に関わる遺伝子が同定されました。これにより、十分量の化合物供給、ならびにさまざまな構造の類縁化合物取得への道が開かれました。
研究手法と成果
共同研究グループは、これまで生産菌から取得されていないオカラミン類縁化合物を探索するため、オカラミンの生合成に関わる遺伝子のうち、環化や修飾を担う四つのオキシゲナーゼ遺伝子okaB、okaD、okaE、okaGを選び、これらの遺伝子欠失株を作製しました。得られた欠失株では、生合成経路の最終産物の一つであるオカラミンBの生産が消失し、各遺伝子が担う生合成反応の基質となる化合物(あるいはその類縁化合物)の蓄積が認められました。その中には、これまでに糸状菌P. simplicissimum AK40株の培養物からは取得できなかった化合物(2-デヒドロキシ-3-デメトキシオカラミンBとオカラミンH)が含まれていました。
次に、オカラミンの化学構造のどの部分が殺虫活性に重要かを調べるため、各欠損株から収集したオカラミン類のGluClに対する作用を、カイコガ由来GluClを発現させたアフリカツメガエル卵母細胞を用いた二電極膜電位固定法[4]により評価しました(図2)。その結果、8員環のアゾシンを持たない類縁化合物(オカラミンG)や、アゾシン環を構成する二重結合の一方が飽和した環を持つ類縁化合物(オカラミンN)では、GluClに対する作用がほとんど失われることが分かりました。このことから、ある特定の立体配座を持つ8員環構造(1,4-ジヒドロアゾシン構造)がオカラミンの殺虫活性に必須であることが分かりました。また、オカラミンHも活性を示さないことから、インドール環窒素へのプレニル基の付加も重要であることが明らかになりました。
今後の期待
本研究により、オカラミン生産菌の遺伝子欠失株を利用することで、本来の生合成プロセスでは取得が難しい生合成中間体などの類縁化合物を効率的に収集し、それらのGluClに対する作用の評価により、オカラミンの殺虫活性に重要な部分構造を突き止めました。
本研究は、構造が複雑で化学合成困難な天然物の生物活性評価における生合成研究の利点を示したのと同時に、今後の誘導体展開に有益なオカラミンの構造活性相関[5]情報を提示しており、新たな殺虫剤開発への貢献が期待できます。
原論文情報
Naoki Kato, Shogo Furutani, Junnosuke Otaka, Akira Noguchi, Kiyomi Kinugasa, Kenji Kai, Hideo Hayashi, Makoto Ihara, Shunji Takahashi, Kazuhiko Matsuda, and Hiroyuki Osada, “Biosynthesis and structure-activity relationship studies of okaramines that target insect glutamate-gated chloride channels”, ACS Chemical Biology, 10.1021/acschembio.7b00878
発表者
理化学研究所
環境資源科学研究センター 天然物生合成研究ユニット
研究員 加藤 直樹(かとう なおき)
環境資源科学研究センター ケミカルバイオロジー研究グループ
グループディレクター 長田 裕之(おさだ ひろゆき)
近畿大学 農学部
教授 松田 一彦(まつだ かずひこ)
大阪府立大学 生命環境科学研究科
講師 甲斐 建次(かい けんじ)
報道担当
理化学研究所 広報室 報道担当
近畿大学 農学部事務部
大阪府立大学 広報課 広報グループ
補足説明
-
- 抑制性グルタミン酸受容体(GluCl)
- システインループ受容体ファミリーに属するイオンチャネルの一種であり、無脊椎動物の神経細胞にのみ存在する。グルタミン酸が受容体に結合することで、Cl–イオンの細胞内への流入が起こり、それにより神経伝達の抑制が引き起こされる。
-
- リガンド
- 受容体と相互作用する物質のこと。
-
- イベルメクチン
- 放線菌の生産する抗寄生虫薬アベルメクチン(エバーメクチン)の化学誘導体のひとつ。WHOの指導の下、オンコセルカ症(河川盲目症)やリンパ性フィラリア症の制圧に用いられている。大村智(北里大特別栄誉教授)は、本化合物による寄生虫感染症治療法の発見の功績によりウィリアム・キャンベルとともに2015年ノーベル生理学・医学賞を受賞した。
-
- 二電極膜電位固定法
- 膜電位を測定する電気生理学的実験手法のひとつ。膜電位を一定値に保ちながら膜電流を測定する方法で、チャネルや起電性のトランスポーターを流れる抵抗性のイオン電流のみを測定することができる。
-
- 構造活性相関
- 化合物の化学構造と生物活性の関係のこと。医薬、農薬開発において、より強い活性を持つ化合物を創出や、大量供給のための化学合成を行う上で重要な情報となる。
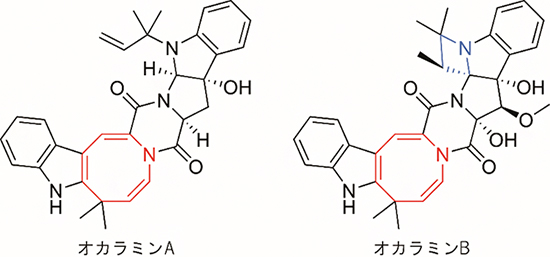
図1 オカラミンの化学構造
殺虫活性に必須である8員環の1,4-ジヒドロアゾシン(赤色)はオカラミンA(左)とオカラミンB(右)に共通する部分構造である。オカラミンBはさらに4員環のアゼチジン(青色)を含んだ八環性骨格(8個の環状構造を持つ)という天然物でも非常に珍しい化学構造をしている。
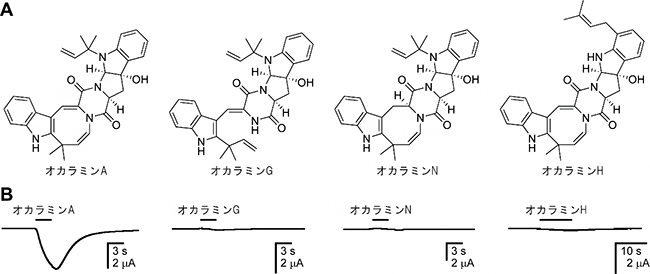
図2 カイコガ由来抑制性グルタミン酸受容体(GluCl)に対するオカラミンの作用
(A)GluClに対する作用を評価したオカラミン類(の一部)の化学構造。
(B)GluClを発現させたアフリカツメガエル卵母細胞を用いて、二電極膜電位固定法により測定したオカラミン処理の電流応答。オカラミンAはGluClに対して作用を示すが、1,4-ジヒドロアゾシン構造を持たないGやN、プレニル基がインドール環の別の場所に付加したHは示さないことが分かった。