2020-09-18 筑波大学,東北大学,日本医療研究開発機構
研究成果のポイント
- 動物細胞用に開発されたRAPタグ注1)が、植物細胞においても有効なペプチドタグとしてはたらくことが明らかになりました。
- RAPタグを認識する抗体注2)PMab-2を、植物細胞内で大量に作製することに成功しました。
- 植物において低コストで抗体を作製することができることから、植物細胞における抗体作製の基盤技術となり得ます。
概要
筑波大学生命環境系/つくば機能植物イノベーション研究センター三浦謙治教授、東北大学未来科学技術共同研究センター/大学院医学系研究科加藤幸成教授らの研究グループは、動物細胞で作られる目的タンパク質に目印をつけるために開発されたRAPタグが、植物細胞の作るタンパク質の検出にも有効であること、さらにRAPタグを認識する抗体であるPMab-2を植物で効率的に生産することを可能とし、タグを付けたタンパク質の精製に有用であることを明らかにしました。
生体内にある多種類のタンパク質の中から、目的タンパク質の機能・局在などを調べるためには、目的タンパク質に特異的な抗体が必要です。しかし、それが容易に入手できるとは限りません。そこで、遺伝子工学的手法によって、目的タンパク質に目印となるタグをつけて、生体内で発現させることで、他のタンパク質と区別することができます。しかしながら、植物で発現させた場合、タグ抗体が特異的に働かないなどの困難もあり、これまで実際に利用されているのは数種にとどまっていました。
本研究では、RAPタグを付与したタンパク質を植物体内にて発現させた場合、PMab-2抗体を用いて、特異的に目的のタンパク質を検出することが可能であるとともに、PMab-2抗体によるアフィニティークロマトグラフィー注3)により、目的タンパク質を精製できることを明らかにしました。また、本研究グループが開発した「つくばシステム参1)」を用いて、植物細胞にてRAPタグを認識するPMab-2抗体を大量に産出させることに成功しました。この植物由来PMab-2抗体は、簡便に高純度で精製することが可能で、CHO細胞注4)由来PMab-2抗体と同様の抗体活性をもつことを示しました。
これらのことから、植物においてRAPタグが有効に機能すること、および、「つくばシステム」によりRAPタグを認識するPMab-2抗体を生産・精製することができることが分かり、植物におけるタグシステムの新たなレパートリーが追加されました。これにより、低価格で抗体を作製・精製するための基盤技術の構築、さらには植物バイオテクノロジー分野の発展にも寄与することが期待されます。
本研究の成果は、2020年9月10日付「Frontiers in Plant Science」で公開されました。
*本研究は、科学研究費補助金(19H04637)、日本医療研究開発機構(AMED)・先端的バイオ創薬等基盤技術開発事業(JP19am0401013)、AMED・創薬等ライフサイエンス研究支援基盤事業(BINDS;JP19am0101078)、AMED・次世代治療・診断実現のための創薬基盤技術開発事業(JP19ae0101028)、T-PIRC遺伝子実験センター「形質転換植物デザイン研究拠点」の一部によって実施されました。
研究の背景
生体内にある多種類のタンパク質の中から、目的タンパク質の機能・局在などを調べるためには、目的タンパク質に特異的な抗体が必要です。しかし、目的タンパク質に特異的な抗体が必ずしも入手できるとは限りません。そこで、遺伝子工学的手法によって、目的タンパク質に目印となるタグをつけて、生体内で発現させることで、他のタンパク質と区別することができます(図1)。タグは数アミノ酸からなる比較的短いポリペプチド鎖からなるものと、数100アミノ酸からなるものがあります。ポリペプチド鎖からなるタグの場合、タンパク質の構造や機能に影響を及ぼさない可能性が高いことから、様々なタグおよびそのタグを認識するタグ抗体が開発されています。しかしながら、植物細胞でタグを発現させる場合、タグ抗体が非特異的なタンパク質を検出して、特異性に問題があるなど、実際に利用されているのは数種にとどまっています。そこで、植物細胞で有効にはたらく新たなタグシステムを見出すため、近年、動物細胞において様々なタンパク質研究に活用できるタグシステムとして単離されたRAPタグ参2)に注目しました。
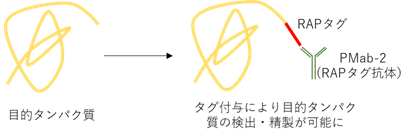
タグシステムには、タグとそのタグを特異的に認識する抗体が必要です。RAPタグを認識する抗体PMab-2はCHO細胞で生産されています参2)。植物細胞を用いたタンパク質の生産は、CHO細胞を用いる方法よりも、低コストであるという利点があります。そこで、PMab-2についても植物細胞内にて生産させることで、植物由来のタグ抗体がCHO細胞由来のタグ抗体と同様の抗体活性をもつか、また、植物細胞での抗体産出能を明らかにすることを目的としました。
研究内容と成果
まず、RAPタグが植物にて有効にはたらくことを示すため、110kDa注5)のタンパク質(シロイヌナズナBIGタンパク質のC末端領域)にRAPタグを付与したタンパク質を発現させたところ、様々なタンパク質が含まれている植物細胞からの抽出液からRAPタグを指標にして目的タンパク質が検出されました(図2A)。また、タグを指標にしたアフィニティークロマトグラフィーが利用可能であるか、その効率性に違いがあるかを明らかにするため、RAPタグとこれまでに植物細胞でタグシステムとしてよく用いられているFLAGタグを比較しました。目的タンパク質には、以前にFLAGタグを付与してもタンパク質の発現がみられたシラカバ花粉アレルゲンBet v 1参3)を用いました。その結果、FLAG-Bet v 1あるいはRAP-Bet v 1を発現させた植物から、RAPタグを用いた場合でもFLAGタグと同様に目的タンパク質を精製できることが明らかとなりました(図2B)。これらのことから、RAPタグは特異的にPMab-2により認識され、植物細胞内においても、タグとして目的タンパク質の検出・精製に有効であることが示されました。このことは、植物における有効なペプチドタグとしてバリエーションの1つに付け加えることができることを示しています。
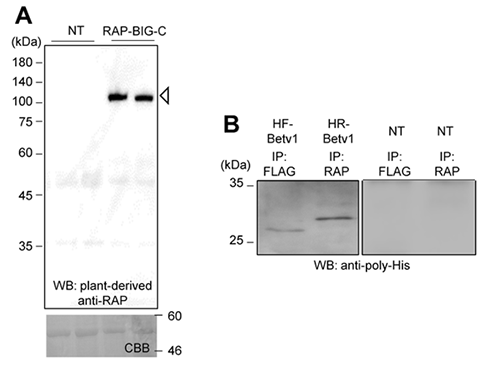
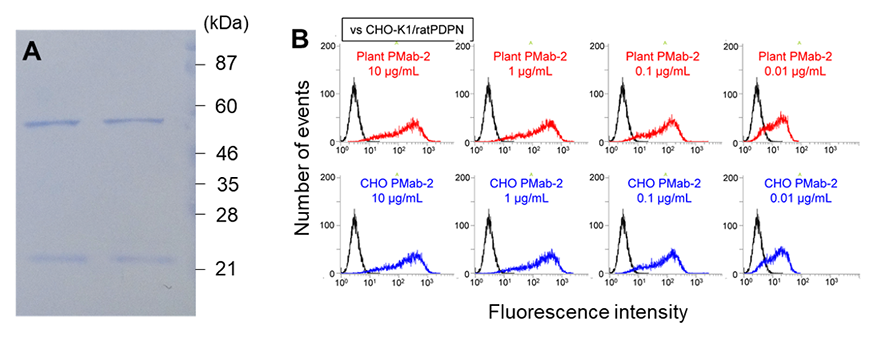
次に、抗体PMab-2を植物細胞にて大量に発現、精製可能であるかを調べました。本研究グループでは以前に、植物細胞で大量のタンパク質を生産することができる「つくばシステム」を開発しています。そこで、PMab-2抗体のH鎖(約50kDa)およびL鎖(約25kDa)を生産する遺伝子をこのシステムに導入して、ベンサミアナタバコにて発現させたところ、H鎖およびL鎖ともに発現すること、ヘテロ四量体(異なる4つのタンパク質からなる複合体、約150kDa)が植物細胞内にて構築されることが分かりました。植物細胞を用いる利点は、植物には抗体が存在していないため、ヘテロ四量体が適切に形成されれば、アフィニティークロマトグラフィーにより簡便に精製可能であることです(図3A)。この植物由来PMab-2抗体は、CHO細胞由来PMab-2抗体と同様の抗体活性を示しました(図3B)。このことから、植物由来PMab-2が抗体として機能することが明らかになりました。
今後の展開
RAPタグが植物においても特異的に認識されることから、今後、ペプチドタグの1つとして有効活用されることが期待できます。また現在、抗体作製には、CHO細胞が用いられていますが、植物細胞を用いる方が低コストであり、植物細胞には抗体が存在しないため、抗体の精製が簡便であるという利点もあります。この方法により、診断に用いるような抗体や、安価に作製する必要がある抗体などの作製も可能です。
用語解説
- 注1)RAPタグ
- DMVNPGLEDRIEの12アミノ酸からなるペプチドタグ。ラットpodoplaninタンパク質に存在するアミノ酸配列で、PMab-2抗体によって検出可能(Fujii et al., (2017) Monoclon. Antib. Immunodiagn. Immunother. 36, 68-71)。
- 注2)抗体
- 免疫グロブリンというタンパク質。一般的な抗体は、2本のH鎖(重鎖:分子量の重い分子鎖)と2本のL鎖(軽鎖:分子量の軽い分子鎖)からなるタンパク質の複合体のヘテロ四量体(異なる4つのタンパク質からなる複合体)を形成する。植物には抗体を自ら作り出す仕組みはないが、マウスやヒトなどから単離した抗体遺伝子を導入することで、H鎖あるいはL鎖といったタンパク質が生産され、植物体内でのヘテロ四量体形成が可能。
- 注3)アフィニティークロマトグラフィー
- タンパク質同士の結合や核酸とタンパク質の特異的な結合など、アフィニティー(親和性)によって物質を分離する方法。本研究では、抗体とプロテインG(免疫グロブリンに結合するタンパク質)との結合を利用した。
- 注4)CHO細胞
- チャイニーズハムスター卵巣(Chinese Hamster Ovary)細胞。タンパク質の生成に適した動物細胞であり、バイオ医薬品や抗体生産などに用いられている。
- 注5)kDa(kilodalton)
- 原子や分子の質量を表す単位で、質量12の炭素原子、12Cの1/12が1Da(dalton)として定義される。その1000倍の単位が1kDa。12Cに対する相対的な質量である。
- 注6)免疫沈降法
- 目的タンパク質に特異的な抗体を用いて、細胞抽出液など雑多なタンパク質溶液から目的のタンパク質を精製する方法。
参考文献
参1)2018年3月19日筑波大学 お知らせ・情報「植物でタンパク質を大量に作る技術を開発~一過的発現システムの改良~」
参2)「RAPタグ」に関するプレスリリースのまとめ|東北大学大学院医学系研究科・加藤研究室
参3)2020年4月3日筑波大学 お知らせ・情報「花粉症治療に利用可能なシラカバ花粉アレルゲンの大量生産に成功」
掲載論文
- 題名
- RAP tag and PMab-2 antibody: a tagging system for detecting and purifying proteins in plant cells
- (RAPタグとPMab-2抗体:植物細胞において目的タンパク質の検出・精製に利用可能なタグシステム)
- 著者名
- Kenji Miura, Hideki Yoshida, Shohei Nosaki, Mika K. Kaneko, Yukinari Kato
- 掲載誌
- Frontiers in Plant Science
- DOI
- 10.3389/fpls.2020.510444
お問い合わせ先
研究に関すること
三浦謙治(みうらけんじ)
筑波大学 生命環境系 教授/つくば機能植物イノベーション研究センター 副センター長
加藤幸成(かとうゆきなり)
東北大学未来科学技術共同研究センター/東北大学大学院医学系研究科抗体創薬研究分野 教授
取材・報道に関すること
筑波大学広報室
東北大学大学院医学系研究科・医学部広報室
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
創薬事業部 医薬品研究開発課