2020-10-16 基礎生物学研究所,筑波大学
マメ科植物は、根に根粒と呼ばれる特殊な器官を形成することで、土壌中の窒素固定細菌と共生し、多くの植物が利用できない大気中の窒素を栄養源として利用することができます。これにより、窒素栄養が乏しい土壌でも盛んに生育することができます。一方で、宿主となるマメ科植物は根粒へ多量の光合成産物を供給する必要があるため、過剰な根粒の形成は宿主の生育を著しく阻害します。このことから、宿主植物は根粒の数を最適化する仕組みを持っていることが知られています。
基礎生物学研究所の大熊直生大学院生(総合研究大学院大学)、川口正代司教授、征矢野敬准教授と筑波大学の寿崎拓哉准教授らにより構成される研究グループは、マメ科のモデル植物ミヤコグサを用いて、葉で強く発現するマイクロRNA(注遺伝子「MIR2111-5」を特定し、葉で合成されたmiR2111が根で機能する根粒形成抑制因子TOO MUCH LOVE (TML)を阻害することで、根粒の数を全身的にコントロールしていることを明らかにしました。この成果は、2020年10月15日に英国の科学雑誌『Nature Communications』に掲載されました。
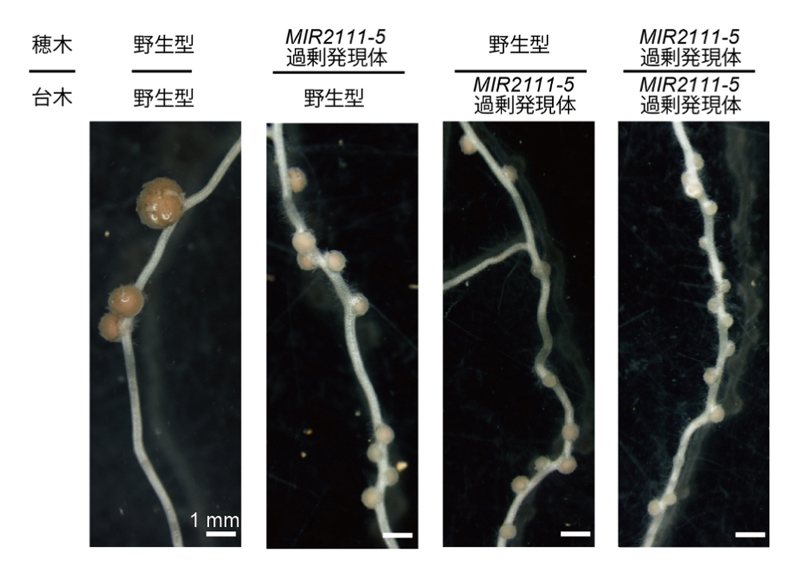
図0: 「葉」で作られたmiR2111が「根」で根粒の数を増やす
接ぎ木を用いて、地上部でのみマイクロRNA遺伝子「MIR2111-5」を過剰発現させmiR2111を過剰に蓄積させると、根の根粒の数が増加した。
【研究の背景】
窒素は植物にとって最も多量に必要とされる必須栄養素の一つです。ほとんどの植物は、土壌中に含まれる硝酸塩やアンモニウム塩などの無機栄養素を吸収することで、その窒素栄養の要求を満たしています。多くの場合、これらの窒素栄養源は土壌に十分に含まれていないため、多くの農耕地では窒素栄養を肥料として与えることで、作物に必要な栄養を補っています。一方で、マメ科植物は、土壌中に生息する窒素固定バクテリアの根粒菌と共生を行うことで、多くの植物が利用できない大気中の窒素を栄養源として利用することができます。根粒共生では、宿主植物は根に根粒という共生器官を形成し、その中で根粒菌がニトロゲナーゼを使って大気中の窒素をアンモニウムに変換することで、宿主に窒素栄養を供給しています。その見返りとして、宿主植物は光合成産物をエネルギー源として根粒菌に供給します。この共生のおかげで、マメ科植物は、窒素栄養が乏しい環境でも旺盛に生育できます。しかしながら、窒素固定や根粒の器官形成は非常に多くの光合成産物を必要とするため、必要以上の根粒の着生は宿主植物の生育を著しく阻害します。これを避けるために、マメ科植物は根粒形成を最適化するシステムをもっています。このシステムは、「葉」で働くHAR1受容体キナーゼが重要な役割を持っており、har1変異体では根粒が過剰に形成され、植物の成長が阻害されます。以前の研究で、同研究グループは、HAR1受容体の下流では「根」で働く根粒形成抑制因子、TMLが根粒形成を阻害していることを報告しています。このことから、「葉」で働くHAR1受容体と「根」で働くTMLの間を仲介する、葉で合成される遠距離シグナル因子がその制御に重要であると考えられてきました。近年、長らく謎であった葉由来の根粒数の制御因子としてTMLのmRNAを分解する機能を持つマイクロRNA、miR2111が注目されています。一方で、葉由来のmiR2111の合成に関わる遺伝子座の全容やHAR1受容体を介した発現制御、さらには葉から根への全身的な根粒数の制御については不明でした。
【研究の成果】
植物に広く保存されているマイクロRNAの多くは、複数の遺伝子座を含むファミリーを形成していることが知られており、遺伝子座ごとに発現量や発現部位が異なることによって様々な発生過程を制御していると考えられています。研究グループは、マメ科のモデル植物であるミヤコグサの葉における、転写産物の網羅的解析データを用いて、ゲノム上に合計7つのmiR2111の前駆体配列をもつ遺伝子が存在することを発見しました(図1)。更に、すべての発見した遺伝子は、マイクロRNAの前駆体に特有のヘアピン構造をとることもわかりました(図1)。
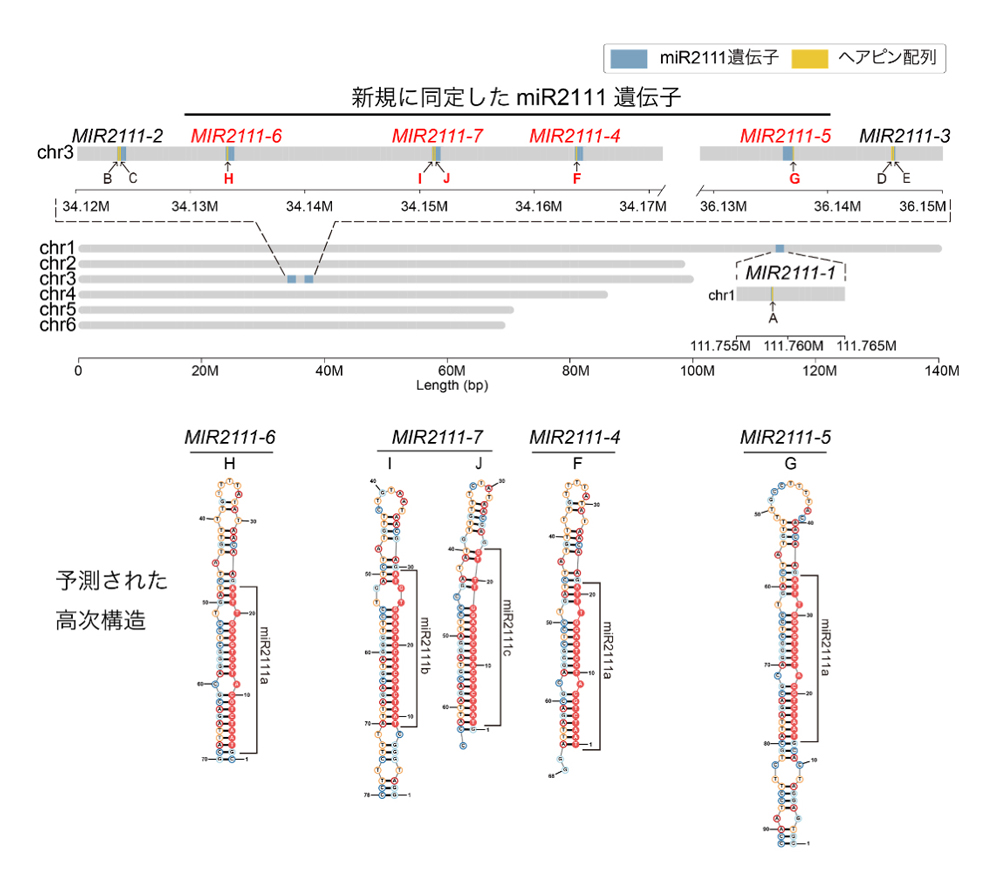 図1: ミヤコグサのmiR2111遺伝子の染色体上の位置とその高次構造
図1: ミヤコグサのmiR2111遺伝子の染色体上の位置とその高次構造
(上)ミヤコグサのmiR2111遺伝子の染色体上の位置を示した。新規に発見した4つのmiR2111遺伝子を合わせると、ミヤコグサは合計7つのmiR2111遺伝子をもつ。(下)新規に発見した4つのmiR2111遺伝子の高次構造の予測図。マイクロRNAの前駆体特有のヘアピン構造をとった。
7つのうち、どのmiR2111遺伝子が根粒数の制御に関わっているかを予想するために、根粒菌を感染させた植物の葉におけるmiR2111遺伝子の発現量を調べました。その結果、4つの遺伝子は、根粒菌の感染と、葉で機能するHAR1受容体に依存して発現のオン、オフが制御されていることがわかりました (図2)。このことから、これら4つのmiR2111遺伝子がHAR1受容体に依存的な根粒の数の制御に関わっている可能性があると考えられました。その中でも、葉で最も顕著に発現していたMIR2111-5 (図2)が重要な役割を持つ可能性が高いと考え、MIR2111-5に着目して研究を進めました。
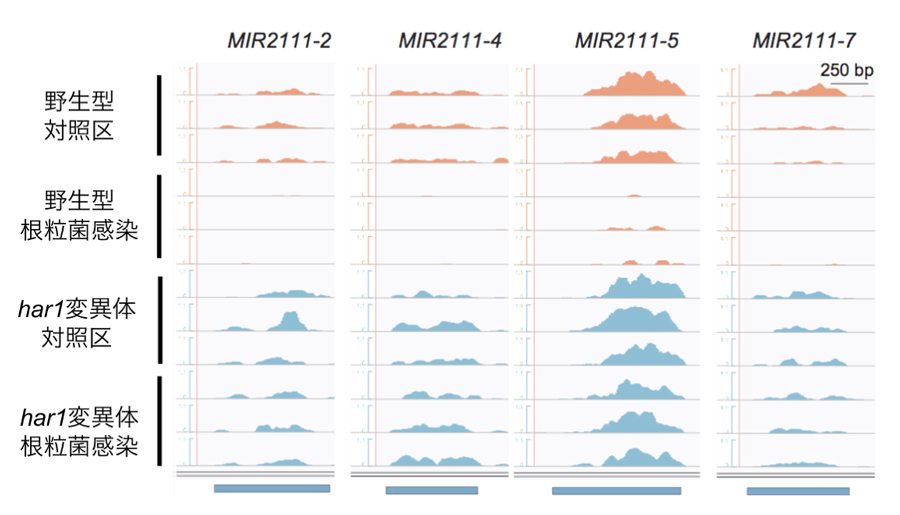 図2: ミヤコグサの葉で発現する4つのmiR2111遺伝子
図2: ミヤコグサの葉で発現する4つのmiR2111遺伝子
野生型とhar1変異体の葉でのmiR2111遺伝子の発現量。山の面積が大きいほど発現量が多い。4つのmiR2111遺伝子は野生型では根粒菌感染に伴って発現が抑制されるが、har1変異体ではそれが起こらなかった。4つのmiR2111遺伝子のうち、MIR2111-5が最も強く発現した。
先行研究では、miR2111は根で発現する根粒形成抑制因子TMLのmRNAを分解することで、根粒の数を増やす機能を持つことが示唆されています。実際に、研究グループが発見した、MIR2111-5 遺伝子を過剰発現させると、miR2111量が増加しTML mRNAが減少するともに、根粒の数が顕著に増加することがわかりました (図3)。反対に、MIR2111-5 をCRISPR/CAS9を用いてノックアウトした変異体では、根におけるmiR2111の蓄積量が半分以下に減少し、それに伴って根粒の数も顕著に減少することがわかりました。このことから、MIR2111-5は全身的な根粒数の制御に重要な役割を持つ遺伝子であることがわかりました。また、MIR2111-5の発現はほとんど葉の維管束でしか見られないことから、葉で合成されるmiR2111が根に蓄積するmiR2111の由来であり、根粒形成の全身的な制御に関わっている可能性が示唆されました。
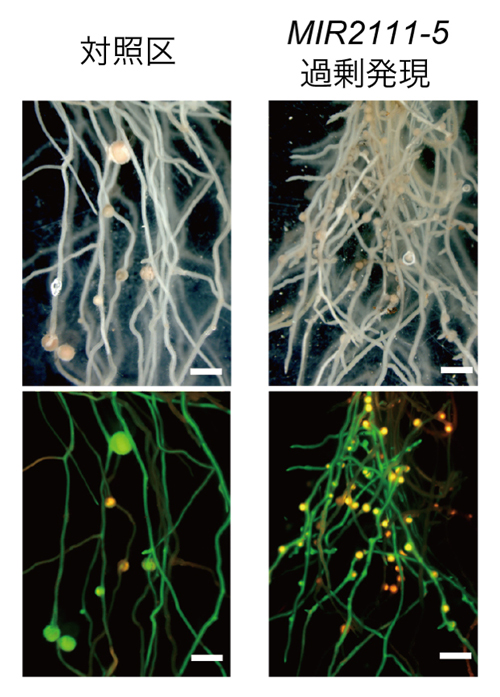
図3: MIR2111-5の過剰発現は根粒の数を著しく増加させる
MIR2111-5を過剰発現させた形質転換根 (右)。対照区 (左)と比べて過剰な数の根粒を着生した。マーカーとして、形質転換根は緑色の蛍光を、根粒は赤色の蛍光を発している。
次に、葉で作られたmiR2111が根におけるmiR2111の蓄積と根粒数の増加をもたらしていることの実験的な証拠を得るために、miR2111の蓄積量を変化させた形質転換体を用いて接ぎ木試験を行いました。miR2111を過剰に蓄積する形質転換体を穂木にした場合、野生型の台木ではmiR2111の蓄積量が増加し根粒の数も増加しました (図4)。一方、miR2111の蓄積が抑制された形質転換体の穂木は、野生型の台木における根粒の数を減少させました。これらの結果は、葉で作られたmiR2111が全身的に根粒の数を制御する機能を持っていることの明確な証拠です (図5)。
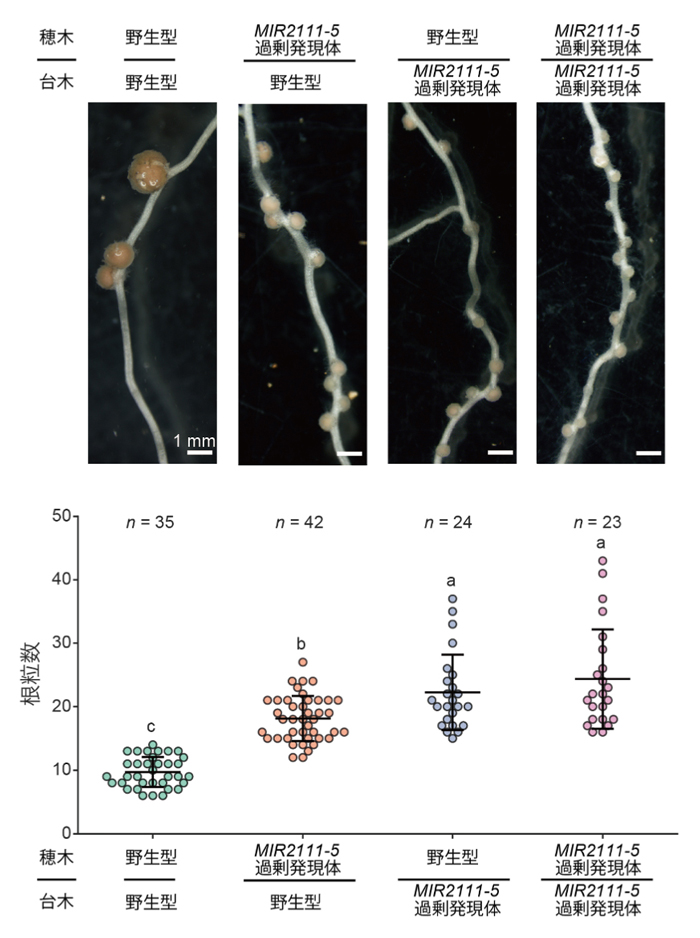
図4: 葉で合成されたmiR2111は全身的に根粒の数を制御する機能を持つ
MIR2111-5を過剰発現させることでmiR2111を生体内に大量に蓄積させた形質転換体を用いて接ぎ木を行った。穂木も台木も野生型を使って接ぎ木した場合と比較して、MIR2111-5過剰発現体を穂木に、野生型を台木にした場合、根粒が過剰に着生した。
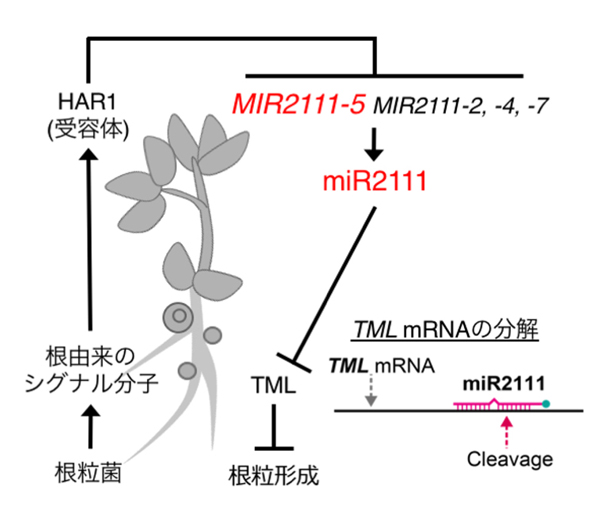
図5: 今回の成果を含めた、miR2111を介した全身的な根粒形成の抑制機構のモデル図
ミヤコグサの葉では、MIR2111-5を含む、複数のmiR2111遺伝子がHAR1受容体に依存して発現し、それに伴ったmiR2111の合成が起こることで全身的に根粒の数を制御する。
【今後の展望】
葉から根へ移動するマイクロRNAは様々な植物種で確認されており、それらは特に植物の養分獲得に関して重要な役割を持つことが示唆されていました。根粒菌との共生はマメ科を含む一部の植物でしか見られませんが、根粒共生を行わない非マメ科植物でもmiR2111やターゲットのTMLは保存されています。非マメ科植物におけるmiR2111の機能は不明ですが、栄養の利用可能度合いに応答してmiR2111の蓄積量が変化することが知られているため、変動する栄養環境に応じた植物の可塑的な発生現象の解明につながる可能性があります。今回明らかになったマメ科植物での根粒数の制御の仕組みに加えて、非マメ科植物におけるmiR2111とTMLの機能を解明することで、根粒共生を成立させる全身的な制御システムがどのように進化してきたのか、という問いへの研究に発展することが期待されます。
注)マイクロRNA
20-22塩基程度の小分子一本鎖RNAで遺伝子の発現制御に関わる。
マイクロRNAは、標的となるmRNAが持つ特異的な塩基配列と結合し、mRNAの分解や翻訳抑制によって抑制的な遺伝子発現制御を行う。マイクロRNAはゲノムにコードされており、部分的なヘアピン構造をとる前駆体RNAが転写され、それが段階的に切り出されて20-22塩基長のマイクロRNAが作られる。
【発表雑誌】
雑誌名 Nature Communications
掲載日 2020年10月15日
論文タイトル: MIR2111-5 locus and shoot-accumulated mature miR2111 systemically enhance nodulation depending on HAR1 in Lotus japonicus.
著者: Nao Okuma, Takashi Soyano, Takuya Suzaki, Masayoshi Kawaguchi
DOI: 10.1038/s41467-020-19037-9
【研究グループ】
本研究は、基礎生物学研究所 共生システム研究部門(総合研究大学院大学 生命科学研究科 基礎生物学専攻)の大熊 直生(おおくま なお)大学院生、川口 正代司(かわぐち まさよし)教授、征矢野 敬(そやの たかし)准教授、及び筑波大学 生命環境系の寿崎 拓哉(すざき たくや)准教授の共同研究として実施されました。
【研究サポート】
本研究は科学研究費助成事業 (17H03702、20H03283、18H04773、19H03239)と基礎生物学研究所の生物機能解析センターおよび生物機能情報分析室のサポートを受けて実施されました。
【本研究に関するお問い合わせ先】
基礎生物学研究所 共生システム研究部門
教授 川口 正代司
【報道担当】
基礎生物学研究所 広報室
筑波大学 広報室