2021-02-12 理化学研究所
理化学研究所(理研)脳神経科学研究センターシナプス可塑性・回路制御研究チームのルディー・トング訪問研究員(研究当時)、合田裕紀子チームリーダーらの国際共同研究チームは、神経細胞の近隣のシナプス[1]間で起こるシナプス強度[2](情報の伝わりやすさ)の変化について、新たなメカニズムを見いだしました。
本研究成果は、記憶をつかさどる脳内シナプス回路の稼働原理の解明とその制御の理解に貢献すると期待できます。
学習シグナル[3]に誘導されるシナプス可塑性[4]は記憶に重要であり、記憶の形成の理解には刺激を受けたシナプスの強度変化が鍵とされてきました。一方で、学習シグナルの刺激を受けたシナプスだけでなく、直接刺激されなかった近隣のシナプスも強度変化を起こすことが知られています。しかし、このようなシナプス間での競合の実態は不明でした。
今回、国際共同研究チームは、学習シグナルの刺激を直接受けなかったシナプスの強度は、刺激を受けたシナプスに近いほど弱くなり、逆に少し離れたシナプスでは強くなることを示し、シナプス強度を強くするシグナルと弱くするシグナルが並行して稼働していることを突き止めました。この知見は、記憶を形成するシナプス強度の変化の最小単位は何かという問いへの理解につながります。
本研究は、科学雑誌『Cell Reports』オンライン版(1月26日号)に掲載されました。
背景
脳内では、数千億個にも及ぶ神経細胞が複雑につながって、巨大な神経ネットワークを形成しています。神経細胞同士がつながっている部分は「シナプス」と呼ばれ、このシナプスを介して一つの神経細胞から次の神経細胞へと情報が伝わります。シナプスの大半は化学シナプスの類いであり、神経伝達物質[5]が神経細胞のシナプス前終末から放出され、それを別の神経細胞のシナプス後部の樹状突起にある受容体が受け取ることで情報が伝達されます。
脳内の興奮性シナプス[1]では、主にグルタミン酸が神経伝達物質として使われており、そのグルタミン酸を受け取るシナプス後部は「スパイン[6]」と呼ばれ、樹状突起から突出した小さな部位に形成されています。一つの神経細胞の樹状突起上には数千~数万個のスパインが存在し、スパインの数とほぼ同じ数の神経細胞から入力を受けています。
シナプスは使われる頻度によって、情報の伝わりやすさ(シナプス強度)が変化する性質があります。一般にシナプス強度は、神経活動によるシナプスへの情報の入力の頻度とタイミングによって増強されたり、抑圧されたりすることが知られています。このシナプス強度の変化は、シナプス前終末から神経伝達物質が放出される確率や、シナプス後部の受容体の量が増減することで引き起こされるとされ、学習や記憶を支えるメカニズムの一つであると考えられています。
学習に関わるシナプス強度の変化がどのように独立して個々のシナプス前終末とシナプス後部で起こるのか、そしてどのように樹状突起上を共有する近隣シナプスと協調して、局所のシナプス回路単位で処理されているのかは未解明です。
研究手法と成果
国際共同研究チームは、近隣シナプス間のシナプス強度の調整の原理を突き止めるために、海馬[7]培養スライスを用いて、一つの神経細胞の一つのシナプスに強度増幅を促す高頻度の学習シグナルの刺激を与え、同じ樹状突起上を共有するシナプスの前終末と後部(スパイン)の強度変化を解析しました。
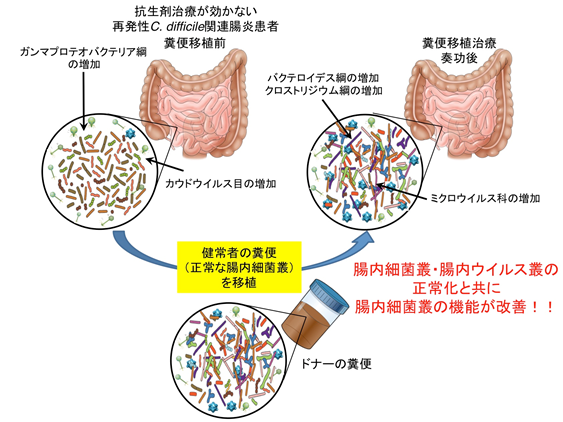
実際には、神経細胞を蛍光物質で可視化した樹状突起上のスパインクラスター(5~7個のスパイン)を標的に、光操作で局所的に神経伝達物質のグルタミン酸を放出することで個々のスパインをほぼ同時に刺激し、刺激されたシナプスのスパインと刺激されなかった近隣シナプスのスパインの形態変化(シナプス後部強度に相当する)をモニタリングしました(図1)。
また、蛍光ラベルとともに蛍光カルシウムセンサー[8]をシナプス後部の神経細胞に注入して、電極でシナプス応答を促し、シナプス後部のカルシウム反応[9]を観察することで、シナプス前終末からの神経伝達物質の放出確率(シナプス前終末強度に相当する)を推定しました(図1)。
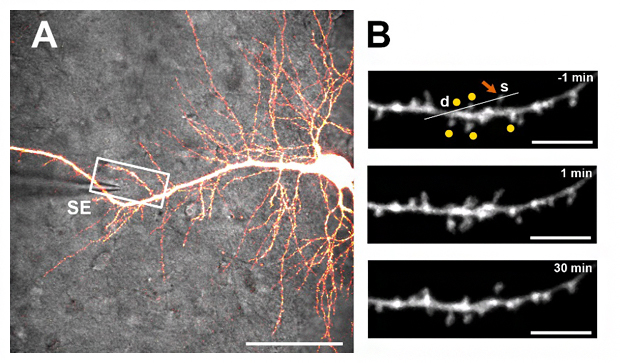
図1 スパインクラスターの学習シグナルの刺激による近隣シナプス強度変化の解析
A.蛍光ラベル(AlexaFluor594)と蛍光カルシウムセンサー(OGB-1)を注入した神経細胞の樹状突起の顕微鏡写真。シナプス前終末の強度のモニタリングには電極(SE)を使い、局所的にシナプス応答を促した。スケールバーは20マイクロメートル(μm、1μmは1,000分の1mm)。
B.5~7個のスパインクラスター(オレンジの丸印)を標的として学習刺激を与えた。S(赤矢印)は、シナプス前終末からの応答確率をモニタリングしたスパインの例。スケールバーは10μm。
実験の結果、刺激されたシナプスではスパインの形態が増大し、長期可塑性[4]が誘導されました。さらに、直接刺激されなかった近隣のスパインでも可塑性が誘導され、シナプス後部強度は刺激されたシナプスに近ければ弱くなり(長期抑圧:LTD)、少し離れたスパインでは逆に強くなりました(長期増強:LTP)(図2左)。一方で、これまで学習的シナプス可塑性で注目されていなかった近隣シナプスの前終末においても、刺激されたシナプスに近いシナプスでは、樹状突起のシグナル伝達を介して神経伝達物質の放出確率が低下し、シナプス前終末強度が減弱することが分かりました。しかし、スパインの場合とは異なり、近隣シナプスにおける前終末強度の増強は見られませんでした(図2右)。
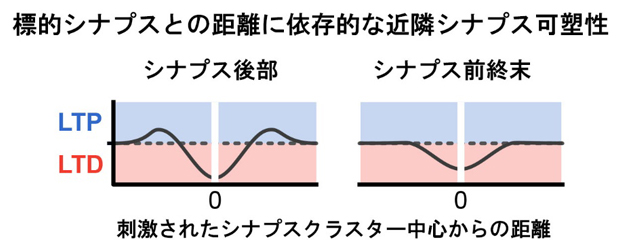
図2 標的シナプスクラスターとの距離間に依存的な近隣シナプス可塑性
左:シナプス後部(スパイン)では、刺激されたシナプスに近いと(約3μm以内)長期抑圧(LTD)が起こり、少し離れたスパイン(5~7μmほど)では長期増強(LTP)が見られた。1μmは1,000分の1mm。
右:シナプス前終末では、ごく近いシナプスにおいて神経伝達物質の放出確率が低下し、シナプス前終末強度の減弱が確認された。シナプス前終末強度の増強は見られなかった。
次に、極性が逆方向のシナプス強度変化をもたらす分子的機構を薬理学的実験で調べました。すると、シナプス後部のスパインの長期抑圧(LTD)には脱リン酸化酵素であるカルシニューリン(CaN)が、長期増強(LTP)にはリン酸化酵素であるCaMKII(カルシウムカルモジュリン依存性タンパク質キナーゼII)がそれぞれ作用することが確認できました(図3)。また、異なるシグナル伝達システムが同時に稼働して、シナプス間における複雑な可塑性のパターンを生み出すことが分かりました(図2)。
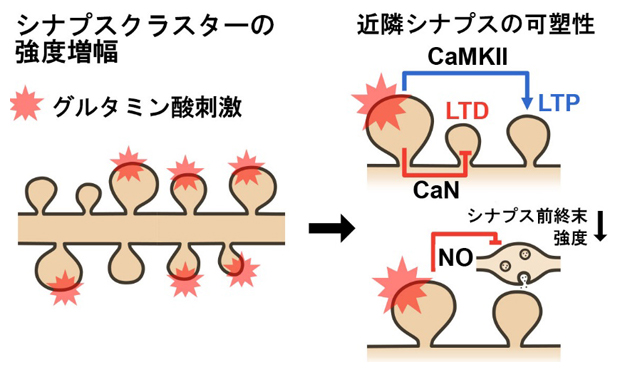
図3 標的シナプスクラスターの学習刺激が誘導する近隣シナプス可塑性の特徴
左:スパインクラスターを標的に、光操作でグルタミン酸による学習刺激を与えて、シナプス強度増大を誘発した。
右:その刺激に伴い、刺激されなかった近隣シナプスでも可塑性が誘導され、いくつかのシグナル伝達システムが並行に稼働して、シナプス可塑性の極性を制御する。シナプス後部(スパイン)の長期抑圧(LTD)は脱リン酸化酵素であるカルシニューリン(CaN)を必要とし、長期増強(LTP)はリン酸化酵素であるCaMKIIが関わる。シナプス前終末強度の低下は、一酸化窒素(NO)によるシグナル伝達が作用する。
今後の期待
本研究では、近隣シナプス間でおこる強度変化の仕組みを新たに見いだしました。学習シグナルの誘発により稼働するシグナル伝達システムの競合が、近隣シナプスの強度変化の極性を左右して、シナプス前終末とシナプス後部の強度分布のパターンを形どることが分かりました。
今後、シナプス入力によるシナプス強度分布の変動を把握して、シナプス可塑性の均衡の本質を明らかにすることで、記憶形成などに関わるシナプス強度変化の最小単位を理解できると考えられます。さらには、情報統合メカニズムの理解が深まり、脳内における情報処理をつかさどるシナプス回路のより効率的な制御方法や数理モデルへの応用が期待できます。
補足説明
1.シナプス、興奮性シナプス
シナプスは、神経細胞の軸索上にある部位(シナプス前終末)と、次の神経細胞の樹状突起上にある部位(シナプス後部)との接点であり、二つの神経細胞間の小さな間隙を跨いで形成される。その多くは化学シナプスと呼ばれ、神経細胞が活性化すると軸索上のシナプス前終末より神経伝達物質と称される化学物質が放出され、シナプス後部にある神経伝達物質の受容体に結合することで情報が伝達される。興奮性シナプスの場合は、神経伝達物質が受容体に結合するとシナプス後部が活性化する。
2.シナプス強度
シナプスにおける情報伝達の効率。化学シナプスの場合は、シナプスにおける神経伝達物質が放出される割合(神経細胞の活性化により神経伝達物質が放出される確率)や受容体の量がシナプス強度を決定づける。
3.学習シグナル
記憶形成に関わるシナプス強度変化を誘導する高頻度の入力。
4.シナプス可塑性、長期可塑性
シナプス強度変化をシナプス可塑性という。上流の神経細胞の活動により、神経伝達物質の放出確率や受容体の量が変動してシナプス可塑性を引き起こす。入力のパターンやその頻度によっては、変化したシナプス強度が長期的に維持される。これを長期可塑性という。
5.神経伝達物質
シナプス前終末から放出される化学物質(グルタミン酸やアセチルコリンなど)。シナプス後部の受容体に結合することで、シナプスを介した情報伝達を担う。
6.スパイン
樹状突起上に突き出たおよそ0.1フェムトリットルほどの小さな部位で興奮性シナプスの入力を受けるシナプス後部。
7.海馬
脳の側頭葉にある記憶や空間認知などに関わる領域。
8.蛍光カルシウムセンサー
カルシウムイオンが結合すると強い蛍光を発する化学物質。
9.シナプス後部のカルシウム反応
神経伝達物質の受容体が活性化されて、シナプス後部のカルシウムイオン濃度が一時的に上昇する現象。
国際共同研究チーム
理化学研究所 脳神経科学研究センター シナプス可塑性・回路制御研究チーム
訪問研究員(研究当時) ルディー・トング(Rudi Tong)
(オックスフォード大学 薬理学部 博士課程)
研究員 トーマス・チェーター(Thomas Chater)
チームリーダー 合田 裕紀子(ごうだ ゆきこ)
オックスフォード大学 薬理学部
教授 ナイジェル・エンプテージ(Nigel Emptage)
研究支援
本研究は、理化学研究所-ドイツ研究財団フェローシップ、オックスフォード大学および英国メディカルリサーチカウンシルなどによる支援を受けて行われました。
原論文情報
Rudi Tong, Thomas E. Chater, Nigel J. Emptage, Yukiko Goda, “Heterosynaptic cross-talk of pre- and postsynaptic strengths along segments of dendrites”, Cell Reports, 10.1016/j.celrep.2021.108693
発表者
理化学研究所
脳神経科学研究センター シナプス可塑性・回路制御研究チーム
訪問研究員(研究当時) ルディー・トング(Rudi Tong)
(オックスフォード大学 薬理学部 博士課程)
チームリーダー 合田 裕紀子(ごうだ ゆきこ)
報道担当
理化学研究所 広報室 報道担当