2021-01-26 大阪大学,日本医療研究開発機構
研究成果のポイント
- 肝がんの進展において、肝臓に存在する肝星細胞※1とがん細胞が相互作用している可能性が考えられていたが、その機序として、肝がん細胞が肝星細胞のオートファジー※2を亢進することによりGDF15(growth differentiation factor 15)※3を分泌させ、肝がん細胞の増殖を促進していることを明らかにした。
- 肝星細胞は肝臓に慢性的な炎症が起きた場合には活性化され、肝臓の線維化を進行させることが知られていたが、肝癌の進展にどのように関わっているかは不明であった。
- 肝星細胞でGDF15を欠損させた肝がんモデルマウスにおいて肝がん進展が抑制されたことから、GDF15を標的とした肝細胞がん新規治療への応用が期待される。
概要
大阪大学大学院医学系研究科の大学院生の明神悠太さん(博士課程/医学部附属病院医員)、疋田隼人助教、竹原徹郎教授(消化器内科学)、国立国際医療研究センターの杉山真也副プロジェクト長らの研究グループは、肝臓の細胞の一種である肝星細胞が肝がん細胞との相互作用によって肝細胞がんを増大させる役割を担っていることを解明しました。
肝がんを含む多くのがん組織内には、がん細胞以外に、線維芽細胞や免疫細胞、血管内皮細胞といった正常細胞や、血管、リンパ管、結合組織なども存在し、がん細胞の周囲にがんの増殖に有利ながん微小環境※4を構築することが知られています。肝星細胞は、肝臓が損傷をうけると活性化され、線維芽細胞として組織の修復に関わります。がんの微小環境において、線維芽細胞は様々な増殖因子を放出していると考えられていることから、活性化した肝星細胞が肝がん細胞と相互作用して、がんの進展に関与しているのではないかと考えられていました。
これまでに肝星細胞の活性化はオートファジーの亢進によって誘導されることが報告されていました。今回、研究グループは、肝がん細胞によって肝星細胞のオートファジーが亢進することを明らかにしました。さらに、オートファジーの亢進により肝星細胞からGDF15を分泌させることによって、肝がん細胞の増殖が促進することを発見しました(図1)。肝星細胞のGDF15を欠損させた肝がんモデルマウスでは、肝がん進展が抑制されることが分かりました。また、ヒト肝がん組織中の肝星細胞でもGDF15の発現を認め、血清GDF15濃度が高い肝細胞がん患者さんは予後が不良であることも明らかにしました。今回の成果により、GDF15を標的とした肝細胞がんの新規治療薬の開発が期待されます。
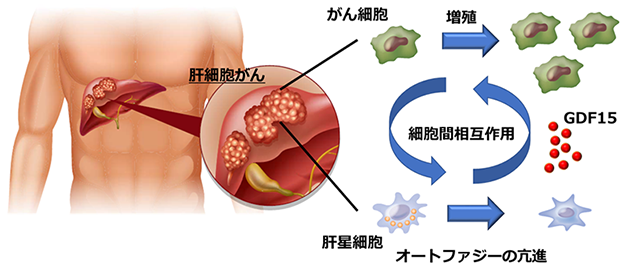
図1 肝がん微小環境における肝星細胞の肝がん細胞との相互作用
本研究成果は、米国科学誌「Gastroenterology」に、2020年12月16日(水)に公開されました。
研究の背景
C型肝炎、B型肝炎、並びに近年増加傾向にある非アルコール性脂肪肝炎(NASH)などの慢性肝疾患の患者さんは病気の進行に伴い肝細胞がんを併発することが知られており、その発症は生命予後に大きな影響を与えます。肝がんは、現在国内においてがんによる死亡原因のうち第5位となっている極めて予後不良な疾患です。
肝細胞がんを含む多くのがんでは腫瘍細胞を取り巻く免疫細胞・線維芽細胞・血管内皮細胞といった間質の細胞とがん細胞そのものが相互作用を介して発育進展に関与していると考えられています。このようながんの微小環境において、線維芽細胞は間質の線維の産生のみならず多種の増殖因子を放出していると考えられています。肝臓の類洞に存在する肝星細胞は、肝細胞が炎症を起こした際に活性化して線維芽細胞となって、細胞外マトリクスタンパク質を放出して肝臓内で線維物質を産生します。ウイルス性肝炎などによって慢性的に肝臓に炎症が生じると、肝星細胞が中心的役割を担って線維化を進展させることが分かっています。この肝星細胞の活性化にオートファジーの亢進が関与するとこれまでいくつかのグループが発表してきました。しかし、線維化の中心的役割を担う肝星細胞が肝がんの微小環境において、どのようにがん細胞と相互作用を有するのかはわかっていませんでした。
本研究の成果
研究グループは、肝星細胞と肝がん細胞を一緒に培養すると、肝星細胞のオートファジーが亢進すること、また、肝がん細胞の増殖が促進することを見出しました。さらに、オートファジーを停止させた肝星細胞を肝がん細胞とともに免疫不全マウスに移植したところ、正常な肝星細胞を移植した場合と比較して、腫瘍増殖が抑えられることが分かりました(図2(A))。肝がんモデルマウスを用いた実験では、肝星細胞のオートファジーを抑制すると、肝がん細胞増殖・肝がん進展が抑制されることを明らかにしました(図2(B))。
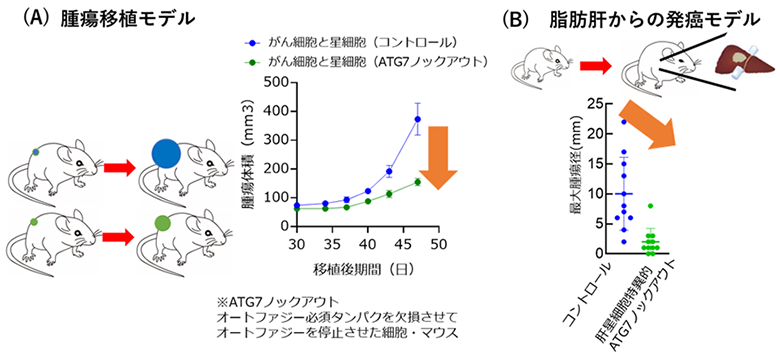
図2 星細胞のオートファジーを抑制すると腫瘍増殖が抑制される
次に、肝がん細胞と一緒に培養することで発現が増加し、肝星細胞のオートファジーを抑制することで減少するような肝星細胞分泌タンパクを網羅的に検索し、GDF15を同定しました。培養細胞を用いた実験では、肝星細胞のGDF15を抑制すると肝がん細胞の増殖は抑制されました(図3(A))。また、肝がんモデルマウスを用いた実験では、肝星細胞のGDF15を欠損させると肝がんの進展は抑制されました(図3(B))。
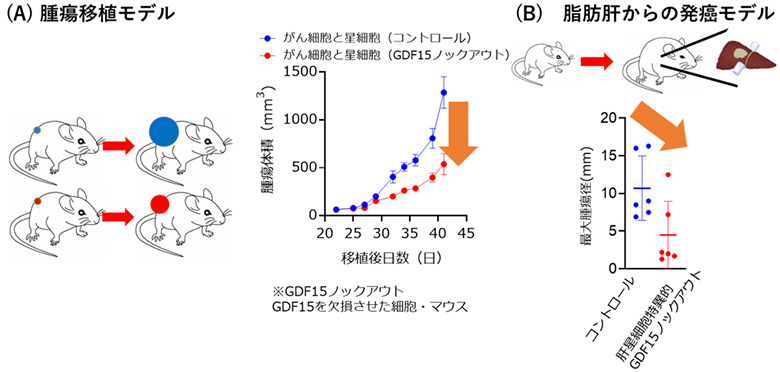
図3 星細胞のGDF15を抑制すると腫瘍増殖が抑制される
肝がん切除検体を用いたシングルセルシークエンス※5・免疫染色の結果、ヒト肝細胞癌の腫瘍組織内にもGDF15を発現した肝星細胞が存在することを明らかにしました(図4)。また肝細胞がん患者の血清GDF15の濃度は高く、血清GDF15濃度が高い肝細胞がん患者さんは予後が不良でした。
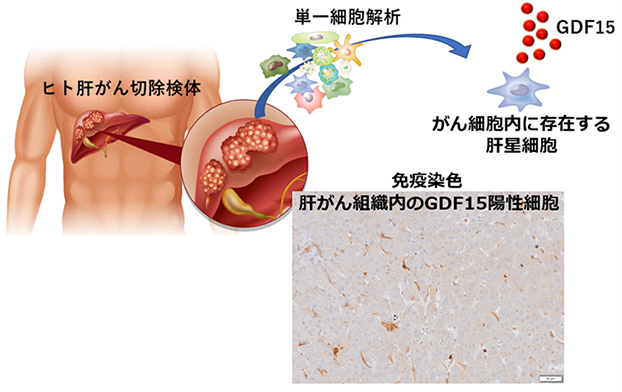
図4 ヒト肝がん内にGDF15を発現した肝星細胞が存在する
これらの結果から、肝がん微小環境における肝星細胞は、オートファジーの亢進を介してGDF15を分泌し、肝がんを増大させる役割があることを見出し、肝がん細胞と肝星細胞の相互作用機序を明らかにしました。
本研究成果が社会に与える影響(本研究成果の意義)
今後GDF15に対する中和抗体などGDF15を標的とした治療が、肝がん患者さんに対する新たな治療選択肢の1つとして臨床開発されることが期待されます。
特記事項
本研究成果は、2020年12月16日(水)に米国科学誌「Gastroenterology」(オンライン)に掲載されました。
- タイトル
- Hepatic stellate cells in hepatocellular carcinoma promote tumor growth via growth differentiation factor 15 production
- 著者名
- Yuta Myojin1, Hayato Hikita1, Masaya Sugiyama2, Yoichi Sasaki1, Kenji Fukumoto1, Sadatsugu Sakane1, Yuki Makino1, Nobuyuki Takemura3, Ryoko Yamada1, Minoru Shigekawa1, Takahiro Kodama1, Ryotaro Sakamori1, Shogo Kobayashi4, Tomohide Tatsumi1, Hiroshi Suemizu5, Hidetoshi Eguchi4, Norihiro Kokudo3, Masashi Mizokami2 and Tetsuo Takehara1*(*責任著者)
- 所属
-
- 大阪大学 大学院医学系研究科 消化器内科学
- 国立国際医療研究センター研究所 ゲノム医科学プロジェクト
- 国立国際医療研究センター病院 外科
- 大阪大学 大学院医学系研究科 消化器外科学
- 実験動物中央研究所 実験動物研究部
なお、本研究は、日本医療研究開発機構(AMED)肝炎等克服実用化研究事業(JP20fk0210064、JP20fk0310108、JP20fk0210060)、日本学術振興会(JSPS)科学研究費補助金研究、国際医療研究開発事業(29指2012)の一環として行われました。
用語説明
- ※1 肝星細胞
- 肝臓の類洞血管内皮細胞と肝細胞の間のディッセ腔に存在する細胞。ビタミンAを貯蔵する細胞で、刺激をうけて活性化すると線維芽細胞様の細胞となる。別名伊東細胞。
- ※2 オートファジー
- 細胞が自らの細胞質の一部を分解し、アミノ酸などを再生する機構。近年がんとの関連が報告されている。
- ※3 GDF15(growth differentiation factor 15)
- TGFβスーパーファミリーに属するタンパクで、食欲を抑制するサイトカインとしても知られる。近年食欲との関連での研究がおこなわれており、中和抗体はがんによる悪液質を軽減する作用があると報告されている。
- ※4 がん微小環境
- がんの組織内では線維芽細胞や血管内皮細胞、免疫細胞といったがん細胞以外の細胞ががん細胞の周りでがん細胞の増殖に有利になるような環境を構築する。この環境のことを微小環境と呼ぶ。近年新規治療標的として注目されている。
- ※5 シングルセルシークエンス
- 組織を1つの細胞ごとに分離し、各々の細胞が発現する遺伝子を網羅的に検証する技術。腫瘍の構成細胞が発現する遺伝子を別々に検討することができる。
本件に関するお問い合わせ先
研究に関すること
疋田隼人(ひきたはやと)
大阪大学 大学院医学系研究科 消化器内科学 助教
報道に関すること
大阪大学大学院医学系研究科 広報室
TEL:06-6879-3388 FAX:06-6879-3399
E-mail:medpr“AT”office.med.osaka-u.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
疾患基礎研究事業部 疾患基礎研究課