2021-06-02 国立がん研究センター,シスメックス株式会社,国立高度専門医療研究センター医療研究連携推進本部
発表のポイント
- がん患者さん並びに健常人の新型コロナウイルス抗体保有率と抗体量を、国立がん研究センターとシスメックスが共同開発した抗体検出試薬を用い評価しました。
- 測定の結果、がん患者さんと健常人では、抗体保有率に差はありませんでした。
- 抗体量は、がん患者さんは健常人と比較し有意に低いことが明らかになりました。
- 細胞障害性抗がん剤注1や免疫チェックポイント阻害薬注2といった薬物療法が、がん患者さんの抗体量に影響を与える可能性が示唆されました。
本研究結果の解釈と注意
- 感染リスクが高いと考えられているがん患者さんにおいても抗体保有率は低いことから、感染対策が十分になされていたこと、無症候性感染の頻度が高くないことが示唆されます。
- がん患者さんは健常人よりも抗体量が低いことが示されましたが、この抗体量の違いが感染リスクや重症化リスクに影響しているかについては明らかにはなっておらず、更なる検討が必要です。
- 今回の研究では、健常人として国立がん研究センター職員にご協力いただいています。同職員は、医療従事者として通常の通勤、勤務を行っていること、一部の職員においては新型コロナウイルス感染症患者さんの対応を行なっていることから、一般社会における健常人よりも抗体量が上昇している可能性もあり、解釈には一定の注意が必要です。
- がん患者さんでは細胞障害性抗がん剤や免疫チェックポイント阻害薬の治療歴によって抗体量の違いが認められており、がん薬物療法が新型コロナウイルス抗体の産生に影響を及ぼしている可能性も示唆されます。
- しかし、現時点でこの結果からがん患者さんの治療方針を変更するといった判断に結びつけることはできません。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区、以下「国立がん研究センター」)とシスメックス株式会社(本社:神戸市、代表取締役会長兼社長 CEO:家次 恒、以下「シスメックス」)は、がん患者さんにおける新型コロナウイルスの罹患状況とリスクを評価するため、2020年8月から10月にかけて500名のがん患者さんと1,190名の健常人について新型コロナウイルスの抗体保有率と抗体量を調査しました。
その結果、明らかな新型コロナウイルスの罹患歴のないがん患者さん並びに健常人における抗体保有率はいずれも低く、差がないことがわかりました。一方で、抗体の量は、がん患者さんは健常人と比較し低いことが明らかになりました。これは年齢、性別、合併症の有無、喫煙歴といった因子で調整しても有意な差を認めました。さらに、がん治療が抗体量に与える影響を検証したところ、細胞障害性抗がん剤を受けているがん患者さんでは抗体量が低く、免疫チェックポイント阻害薬を受けている患者さんでは抗体量が高いことが明らかになりました。本研究結果により、がんの合併、並びにがん薬物療法が抗体の量に影響を与える可能性が示唆されました。
本調査結果は、国際的な医学雑誌「JAMA Oncology」オンライン版(2021年5月28日付)に掲載されました。
また本研究は、国立高度専門医療研究センター医療研究連携推進本部(JH)の支援を受け実施しました。
背景
がん患者さんは、高齢で合併症を有する割合が高いことや、薬物療法や放射線治療、手術療法などのがん治療によって免疫力が一時的に低下することから、新型コロナウイルスに罹患するリスクの上昇や、罹患した場合の重篤化が懸念されています。
新型コロナウイルスの検査には、ウイルスの有無を調べ診断に用いるPCR検査や、感染により産生された抗体(タンパク質)を調べることで感染歴を把握することが出来る抗体検査などがあります。抗体検査は、PCR検査により検出されなかった無症候性感染なども把握することが出来るため、疫学的調査に有用とされています。
がん患者さんと健常人における新型コロナウイルスの抗体保有率や抗体量を比較した大規模研究は世界的にも少なく、がん患者さんは健常人と比較し抗体保有率が高いのか、がん治療と抗体量に関連があるのかは十分にわかっていません。そこで国立がん研究センターとシスメックスは、がん患者さんにおける新型コロナウイルスの罹患状況とリスクを評価するために共同で本研究を実施しました。
研究方法
国立がん研究センター中央病院に通院されているがん患者さんと、健常人として国立がん研究センター職員にご協力いただき、新型コロナウイルスの抗体保有率と抗体量を測定しました。
本研究に使用した抗体検出試薬は、国立がん研究センターとシスメックスが共同開発したもので、ヌクレオカプシドタンパク質(N抗原)注3、スパイクタンパク質(S抗原)注4に特異的に反応する2種類の抗体(IgG、IgM)注5を個別に検出することが可能です。従来の抗体測定法では抗体の有無を測定し定性的な判断となる手法が多かったものの、本測定法では抗体量を定量測定することが可能です。
測定期間
2020年8月から10月
調査対象
がん患者さん 500名(国立がん研究センター中央病院に通院中の患者さん)
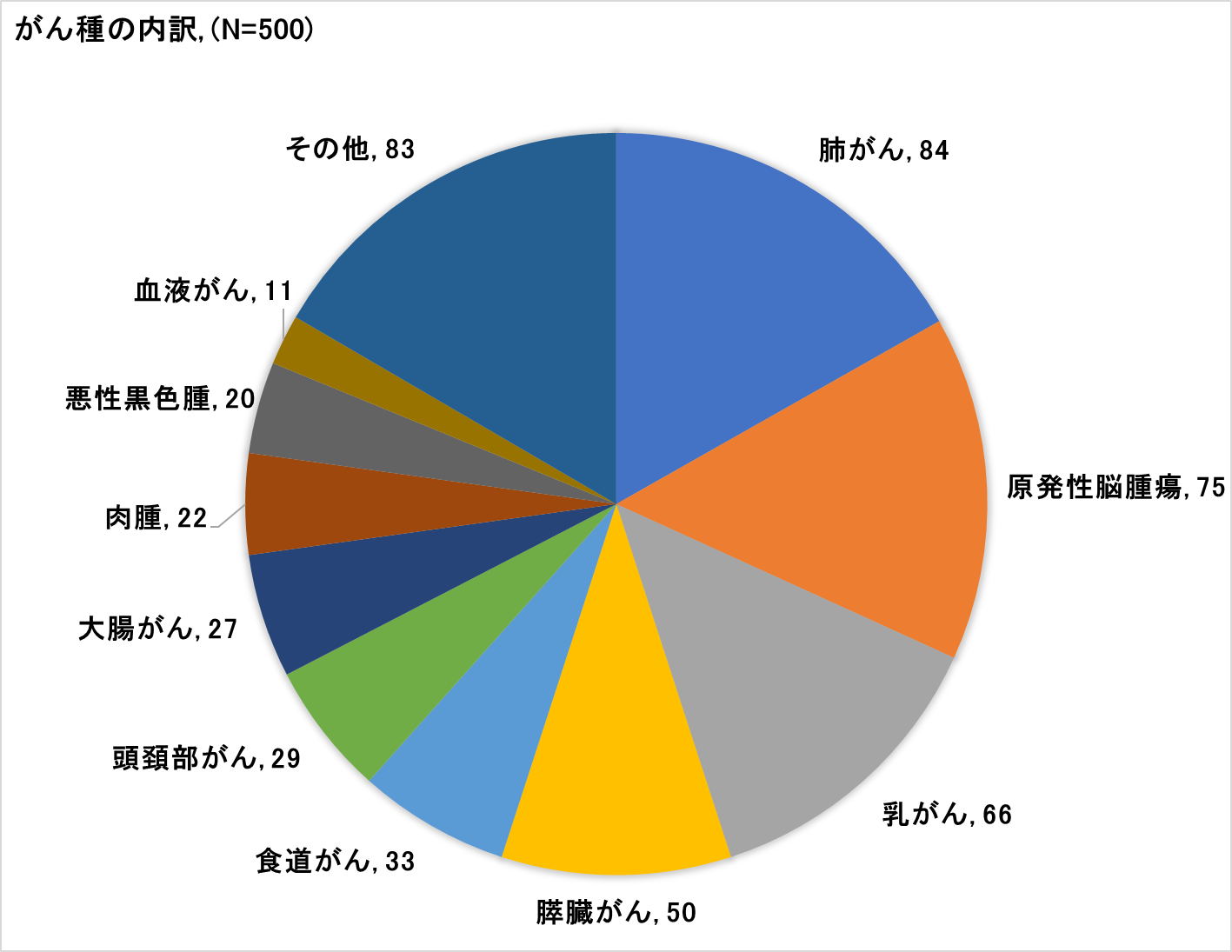
がん種の内訳 (図1)参照
固形がん489名(97.8%)、血液がん11名(2.2%)
肺がん84名、原発性脳腫瘍75名、乳がん66名、膵臓がん50名、食道がん33名、頭頚部がん29名、大腸がん27名、肉腫22名、悪性黒色腫20名、血液がん11名、その他83名
がん治療の内訳
研究参加1か月以内に何らかのがん治療を受けていた患者さん355名(71%)
放射線治療24名(4.8%)、外科手術35名(7%)、免疫チェックポイント阻害薬44名(8.8%)、分子標的治療薬92名(18.4%)、細胞障害性抗がん剤204名(40.8%)
健常人 1,190名(国立がん研究センター職員)
職種
医師179名(15.0%)、看護師385名(32.3%)、研究者197名(16.6%)、技師113名(9.5%)、薬剤師50名(4.2%)、事務職員266名(23.4%)
(図1) 研究に参加されたがん患者さんのがん種の内訳
研究結果
がん患者さんと健常人の背景を比較すると、がん患者さんでは高齢、男性、喫煙者、合併症(糖尿病や高血圧など)を有する割合が多いことがわかりました。
研究参加以前に新型コロナウイルス感染症に罹患されていた6名(がん患者さん3名、健常人3名)を除外し抗体保有率を検討したところ、がん患者さんは0.4%、健常人は0.42%で抗体保有率はいずれも低く、差がないことがわかりました。
一方、抗体量を比較したところ、がん患者さんは健常人と比較し抗体量が低いことが明らかになりました(図2)。これは年齢、性別、合併症の有無、喫煙歴といった因子で調整しても有意な差を認めました。
(図2) がん患者さんと健常人における抗体量の比較
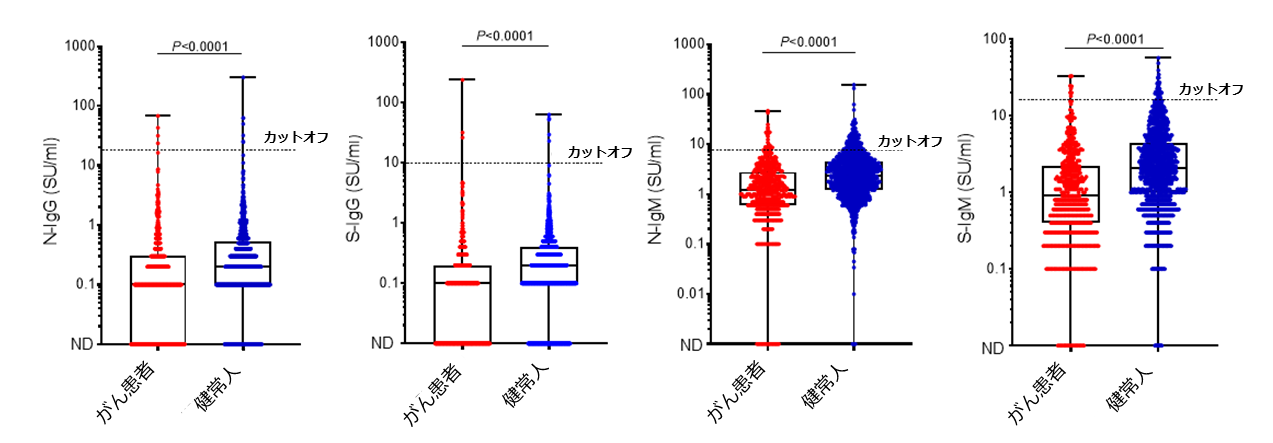
N-IgG、S-IgG、N-IgM、S-IgMそれぞれの抗体の量をがん患者さん(赤)と健常人(青)で比較。抗体の量を縦軸に表示。
次に、がん患者さんにおいて抗体量に影響を与える因子を検討した結果、研究参加1か月以内に細胞障害性抗がん剤を受けている患者さんでは抗体量(N-IgG)が低く、免疫チェックポイント阻害薬を受けている患者さんでは抗体量(N-IgG、S-IgG)が高いことが明らかになりました(図3)。さらに、免疫チェックポイント阻害薬を投与された患者さんにおいては年齢、性別、合併症の有無、喫煙歴で調整しても、投与された患者さんでは投与されていない患者さんに比べ有意に抗体量(N-IgG、S-IgG)が高いことが明らかになりました。一方、放射線治療や外科治療の有無による抗体量に差は認められませんでした。
(図3) がん薬物療法と抗体量の関連
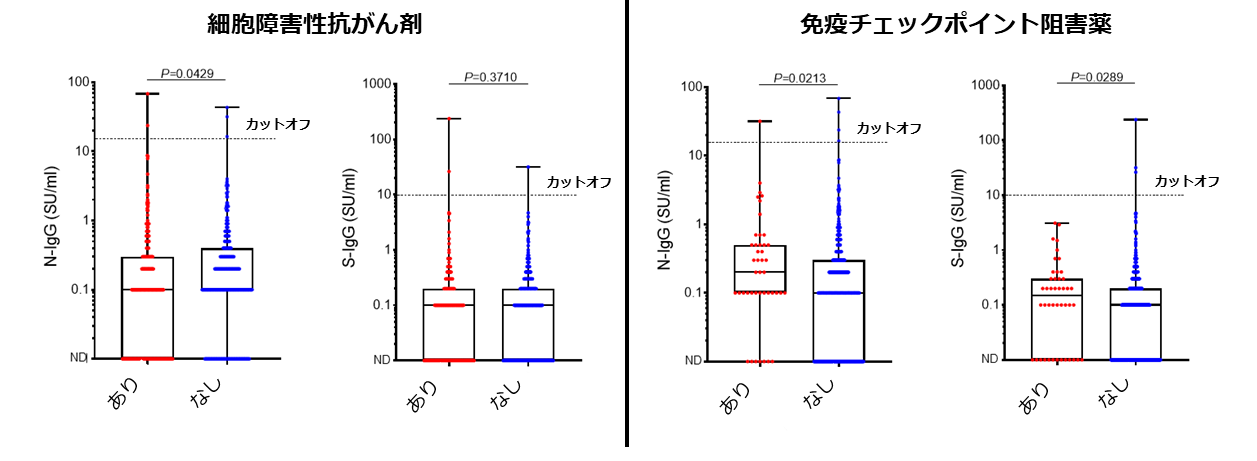
細胞障害性抗がん剤を使用中の患者さんと、使用していない患者さんでN-IgG、S-IgG抗体の量を比較(図3左)。
免疫チェックポイント阻害薬を使用中の患者さんと、使用していない患者さんでN-IgG、S-IgG抗体の量を比較(図3右)。
展望
今後、がん患者さんに対するワクチン接種の有効性を評価するため、ワクチン接種後の抗体量の推移を検討するとともに、がん治療が新型コロナウイルス抗体の産生に与える影響を明らかにしたいと考えています。
参考
厚生労働省による抗体保有調査(一般住民調査)について
厚生労働省では、2020年6月と12月に一般市民を対象に新型コロナウイルスの抗体保有調査を実施しています。調査結果は、以下のページよりご参照ください。
厚生労働省 新型コロナウイルス感染症に関する検査について https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000121431_00132.html
発表論文
雑誌名
JAMA Oncology
タイトル
Difference in SARS-CoV-2 antibody status between patients with cancer and health care workers during the COVID-19 pandemic in Japan
著者
Shu Yazaki, Tatsuya Yoshida, Yuki Kojima, Shigehiro Yagishita, Hiroko Nakahama, Keiji Okinaka, Hiromichi Matsushita, Mika Shiotsuka, Osamu Kobayashi, Satoshi Iwata, Yoshitaka Narita, Akihiro Ohba, Masamichi Takahashi, Satoru Iwasa, Kenya Kobayashi, Yuichiro Ohe, Tomokazu Yoshida, Akinobu Hamada, Toshihiko Doi, and Noboru Yamamoto
掲載日
2021年5月28日
研究費
- 国立高度専門医療研究センター医療研究連携推進本部 横断的研究推進課題(2020-A-1)
- シスメックス株式会社共同研究費
国立高度専門医療研究センター医療研究連携推進本部(JH)について
国立高度専門医療研究センター医療研究連携推進本部(Japan Health Research Promotion Bureau:JH)は、我が国の6つの国立高度専門医療研究センターの資源・情報を集約し、それぞれの専門性を生かしつつ有機的・機能的連携を行うことによって、世界最高水準の研究開発・医療を目指した新たなイノベーションを創出することを目的とし、2020年4月に発足した横断的組織です。
- 国立高度専門医療研究センター医療研究連携推進本部(JH) https://www.japanhealth.jp
シスメックスの新型コロナウイルス感染症への取り組み
シスメックスは、臨床検査機器・試薬メーカーとして、世界中の医療現場で行われている臨床検査の継続実施を支援し、新型コロナウイルス感染症拡大防止に尽力される医療従事者の皆様と共にこの困難を乗り越えることが使命と考えており、そのための「製品・サービスの安定供給」に全力を挙げて取り組んでいます。また、新型コロナウイルス感染症の拡大防止および一日も早い沈静化に貢献するため、国内初となる新型コロナウイルスPCR検査キット(RT-PCR 法)の薬事承認取得や、全国に先駆けて神戸市との産官連携によるPCR 検査体制強化に加え、新たな診断技術の開発に積極的に取り組んでいます。
本研究で用いた抗体検出試薬は、新型コロナウイルス感染症に対するN抗原およびS抗原に対する2種類の抗体(IgG、IgM)の定量測定が可能かつ高い弁別性能を有し、幅広い疫学的研究やワクチンの効果モニタリングなどの臨床応用へ活用できることを、国立がん研究センターなどとの共同研究において報告しています。
- シスメックス株式会社 https://www.sysmex.co.jp/COVID19.html
- 2020年6月11日 プレスリリース https://www.ncc.go.jp/jp/information/pr_release/2020/0611/index.html
- 論文 Noda K. et al. Sci Rep. 2021 Mar 4;11(1):5198. doi: 10.1038/s41598-021-84387-3.
用語解説
注1 細胞障害性抗がん剤
細胞障害性抗がん薬は、細胞の増殖の仕組みに着目して、その仕組みの一部を邪魔することでがん細胞を攻撃する薬です。がん以外の正常に増殖している細胞も影響を受けます。古くより用いられている治療方法であり、白金製剤やアルキル化剤、微小管阻害薬などが含まれます。(国立がん研究センター がん情報ホームページより引用 https://ganjoho.jp/public/dia_tre/treatment/drug_therapy/dt02.html https://ganjoho.jp/public/dia_tre/treatment/drug_therapy/dt02.html)
注2 免疫チェックポイント阻害薬
体の中には、異物の侵入を防いだり、侵入してきた異物を排除したりして、体を守る抵抗力を備えた「免疫細胞」があります。がん細胞の中には、免疫細胞と結合することによって、免疫細胞にブレーキをかけ、その攻撃から逃れる仕組みをもっているものがあります。このような、がん細胞と免疫細胞の結合を“免疫チェックポイント”といいます。免疫チェックポイント阻害薬は、免疫チェックポイント分子を標的とした抗体薬です。がん細胞と免疫細胞が結合できないように邪魔をすることで、免疫細胞にかけられたブレーキを外して、自分の免疫細胞ががん細胞を攻撃できるようにする薬です。(国立がん研究センター がん情報ホームページより引用 https://ganjoho.jp/public/dia_tre/treatment/drug_therapy/dt02.html https://ganjoho.jp/public/dia_tre/treatment/drug_therapy/dt02.html)
注3 ヌクレオカプシドタンパク質(N抗原)
ウイルスの基本構造であり、ウイルスの性質に大きく影響するタンパク質です。
注4 スパイクタンパク質(S抗原)
ウイルスの周りに無数に突き出したタンパク質であり、細胞の受容体と結合することで感染が生じます。
注5 抗体(IgG、IgM)
新型コロナウイルスに感染した場合、他のウイルス感染症と同じく抗体(タンパク質)が産生されます。抗体には感染後比較的早く出現するIgM抗体(1から2週間)と遅れて(2から3週間)出現するIgG抗体があります。PCR検査と抗体検査を両方用いることで、診断精度を高めることや感染者数を正確に把握することが出来る可能性があります。
報道関係からのお問い合わせ先
国立研究開発法人国立がん研究センター 企画戦略局 広報企画室
シスメックス株式会社 IR・広報部 担当:林