心疾患、喘息、骨疾患など11の病気の発症リスクと相関
2019-03-26 理化学研究所,日本医療研究開発機構
理化学研究所(理研)生命医科学研究センター統計解析研究チームの鎌谷洋一郎チームリーダー、的場奈々特別研究員(研究当時)、秋山雅人リサーチアソシエイト(研究当時)らの共同研究グループ※は、バイオバンク・ジャパン[1]に参加した日本人約16万人の遺伝情報を用いた大規模なゲノムワイド関連解析(GWAS)[2]により、喫煙習慣に関連する新たな7カ所の感受性領域(遺伝子座)を発見し、さらに喫煙習慣と11種類の病気(心疾患や喘息、慢性閉塞性肺疾患[3]、後縦靱帯骨化症[4]など)の発症リスクが遺伝的に相関していることを見いだしました。
喫煙習慣の健康への影響については広く知られていますが、喫煙習慣が個人の遺伝子配列と具体的にどのように関係しているのかについて、これまで欧米を中心に遺伝学的研究が進められてきました。
われわれは2012年に約1万7千人の日本人集団を対象とした結果を報告していました注1)が、本研究では、約10倍の参加者の情報を用いることで、新たに日本人特異的な喫煙感受性領域を同定することに成功しました。また、喫煙感受性と心疾患や喘息、肺疾患等の発症リスクが遺伝学的背景を共有していることが明らかとなりました。今後、喫煙習慣やそれに起因する病気の予防など遺伝子情報に基づいた精密医療への応用が期待できます。
本研究成果は、オンライン科学雑誌『Nature Human Behaviour』(3月25日付け:日本時間3月26日)に掲載されます。
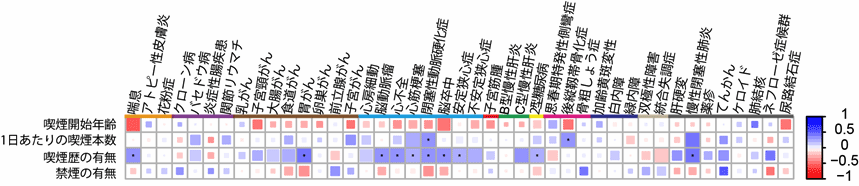
図 喫煙習慣と病気の遺伝学的相関
- 注1)
- Kumasaka et al, Haplotypes with Copy Number and Single Nucleotide Polymorphisms in CYP2A6 Locus Are Associated with Smoking Quantity in a Japanese Population. PLoS One. 2012; 7 (9) e44507
- ※共同研究グループ
- 理化学研究所
- 生命医科学研究センター
- 統計解析研究チーム
- チームリーダー 鎌谷 洋一郎(かまたに よういちろう)
(京都大学大学院 医学研究科 京都大学マギル大学ゲノム医学国際連携専攻 准教授) - 特別研究員(研究当時) 的場 奈々(まとば なな)
(米国ノースカロライナ大学 チャペルヒル校 神経科学センター 博士研究員) - リサーチアソシエイト(研究当時) 秋山 雅人(あきやま まさと)
(現客員研究員、九州大学 医学部 眼科 特任講師) - 特別研究員(研究当時) 石垣 和慶(いしがき かずよし)
(現客員研究員、米国ハーバード大学 ポスドクフェロー) - 研修生 金井 仁弘(かない まさひろ)
(米国ハーバード大学 医学部 博士課程) - 客員主管研究員 高橋 篤(たかはし あつし)
(国立循環器病研究センター研究所 病態ゲノム医学部 部長) - 客員主管研究員 岡田 随象(おかだ ゆきのり)
(大阪大学大学院医学系研究科 遺伝統計学 教授)
- チームリーダー 鎌谷 洋一郎(かまたに よういちろう)
- 基盤技術開発研究チーム
- チームリーダー 桃沢 幸秀(ももざわ ゆきひで)
- 骨関節疾患研究チーム
- チームリーダー 池川 志郎(いけがわ しろう)
- 統合生命医科学研究センター(研究当時)
- 副センター長 久保 充明(くぼ みちあき)
- 東京大学大学院 新領域創成科学研究科 クリニカルシークエンス分野
-
- 教授 松田 浩一(まつだ こういち)
- 東京大学医科学研究所 シークエンス技術開発分野
-
- 特任助教 平田 真(ひらた まこと)
- 藤田保健衛生大学 医学部 精神科
-
- 教授 岩田 仲生(いわた なかお)
- 准教授 池田 匡志(いけだ まさし)
- ※研究支援
- 本研究は、日本医療研究開発機構の「オーダーメイド医療の実現プログラム」、「脳科学研究戦略推進プログラム」、「ゲノム医療実現プラットホーム事業」「再生医療実現拠点ネットワークプログラム:疾患特異的iPS細胞の利活用促進・難病研究加速プログラム」、「難治性疾患実用化研究事業」の支援のもと行われました。本研究で使用したサンプルは、「オーダーメイド医療の実現プログラム」において収集されたものです。
1.背景
喫煙習慣は、呼吸器疾患や心血管疾患、がんなど、さまざまな病気のリスク因子として知られています。さらに、喫煙本数と死亡率との関連を調査した研究では、1日の喫煙本数が多いほど死亡率が高いこと、また禁煙により死亡率は下がることが報告されています注2)。喫煙をやめることで、健康な人生につながり、また社会的な医療費の抑制にもつながると考えられています注3)。それにもかかわらず、世界規模で11億人の人が喫煙者として報告されており注4)、日本における喫煙率は18.2%注5)と、欧米諸国(例えばアメリカでは15.1%注6))に比べて依然高い状態です。
一方、双子を対象とした研究から、喫煙習慣には遺伝子配列の個人差が影響することが明らかになっています。禁煙成功率を上げる一つの可能性として、CHRNA5、CYP2A6などと言った既知の喫煙関連遺伝子情報を用いて禁煙に導く精密医療(プレシジョン・メディシン)が近年提唱されています注7)。実際には喫煙の遺伝因子はこれらの遺伝子だけでは説明しきれない多遺伝子構造(polygenic architecture)を取ること、また少なくとも1万人前後の人数の大サンプルを用いたゲノムワイド関連解析(GWAS)を行うことでリスクを算出できることが近年分かってきました注8)。そこで、欧米系集団を中心に大規模な喫煙関連遺伝子を探索するゲノムワイド関連解析(GWAS)が行われています注9)。しかし多遺伝子を用いた遺伝的リスク推定値は、遺伝的背景の異なる集団では異なった計算方法を用いる必要性があることが分かっている注10)ため、同様の精密医療の日本での実装を目指すためには、日本人集団を対象とした研究を行うことが求められていました。
- 注2)
- Inoue-Choi, M. et al., Association Between Reductions of Number of Cigarettes Smoked per Day and Mortality Among Older Adults in the United States. Am. J. Epidemiol. 188, 363–371 (2019).
- 注3)
- Cronwell J et al, Cost-effectiveness of the clinical practice recommendations in th AHCPR guideline for smoking cessation. Agency for Health Care Policy and Research. JAMA. 278(21) 1759-1766 (1997)
- 注4)
- World Health Organization. WHO report on the global tobacco epidemic, 2017: monitoring tobacco use and prevention policies. (2017)
- 注5)
- Jamal, A. et al.Summary Results of the National Health and Nutrition Survey Japan. (2016)
- 注6)
- Current Cigarette Smoking Among Adults — United States, 2005–2015. MMWR Morb Mortal Wkly Rep 65, 1205–1211 (2016).
- 注7)
- Bierut LJ and Tyndale RF. Preparing the Way: Exploiting Genomic Medicine to Stop Smoking. Trends Mol Med 2018; 24: 187-96.
- 注8)
- Khera AV et al. Genome-wide polygenic scores for common diseases identify individuals with risk equivalent to monogenic mutations. Nat Genet 2018; 50: 1219-24.
- 注9)
- Liu M et al. Association studies of up to 1.2 million individuals yield new insights into the genetic etiology of tobacco and alcohol use. Nat Genet 2019; 51: 237-44.
- 注10)
- Martin AR et al. Human Demographic History Impacts Genetic Risk Prediction across Diverse Populations. Am J Hum Genet 2017; 100: 635-49.
2.研究手法と成果
共同研究グループは、バイオバンク・ジャパンに参加した日本人約16万人の遺伝情報と、喫煙に関わる4項目の情報(喫煙歴の有無、喫煙開始年齢、1日あたりの喫煙本数、現在の喫煙状況[禁煙中か喫煙中か])を用いて、GWASを実施しました。その結果、1日あたりの喫煙本数(の多い少ない)に関連する感受性領域(遺伝子座)を5ヵ所、喫煙歴の有無に関連する遺伝子座を1ヵ所同定しました。これら6遺伝子座のうち四つは、初めて(ゲノムワイド水準で)喫煙との関連が示された領域です(図1)。
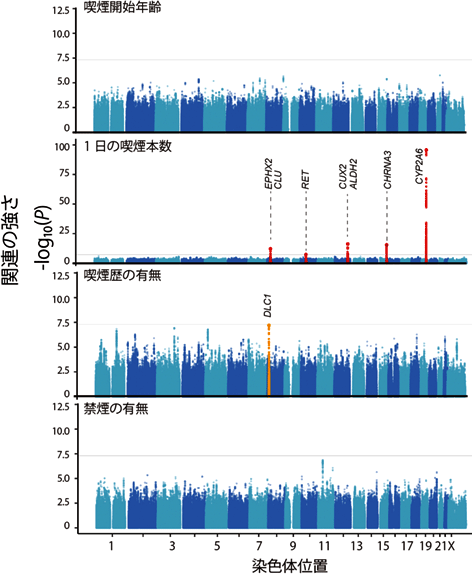
図1 喫煙習慣4項目のゲノムワイド関連解析(GWAS)の結果
横軸が染色体上の位置を示しており、縦軸は関連の強さを示している。喫煙に関わる4項目での解析において、GWASの有意水準を超えた領域は赤色、関連が示唆される水準を超えた領域をオレンジ色で示している。1日あたりの喫煙本数(の多い少ない)に関連する遺伝子座を5ヵ所、喫煙歴の有無に関連する遺伝子座を1ヵ所同定した。
また、男女別で同様にGWASを行ったところ、さらに3遺伝子座を新たに同定しました。そのうち2遺伝子座は男性における喫煙歴の有無への影響があると考えられ、1遺伝子座は女性の喫煙開始年齢への影響が考えられます。LDスコア[5]を用いて全ゲノムの遺伝的構造を検討すると、男女間で喫煙歴の有無に関連する領域は、さらに非常に多数の領域にわたる可能性があることが明らかになりました。喫煙歴の有無は、双子を対象とした研究でも男女間での遺伝的な影響の差が指摘されており、今回の研究結果はそれを支持する結果となりました。
今回新たに発見した7遺伝子座をイギリスのUK Biobank[6]のデータで確認したところ、日本人特有の領域であることが示されました。民族横断的な遺伝的相関[7]を、LDスコアを利用して推定する手法注11)を用いたところ、喫煙歴の有無に影響する遺伝的背景は欧米人と同一ではないことが明らかになり、さまざまな集団で研究を行うことの重要性が改めて示されました。
次に、今回の喫煙習慣のGWAS結果と、これまでに理研で実施した43の病気(生活習慣病、自己免疫疾患、悪性腫瘍、精神神経疾患、骨関節疾患など)におけるGWAS結果を合わせた上で、喫煙習慣と病気の各組み合わせにおける遺伝的背景の共有関係(遺伝学的相関)を調べました。その結果、疫学調査でも指摘されていた喫煙歴と10種類の病気(心血管疾患や喘息、慢性閉塞性肺疾患など)の発症リスクが遺伝的に相関していることが明らかになりました。さらに、1日あたりの喫煙本数は、閉塞性動脈硬化症や後縦靱帯骨化症と遺伝的背景を共有していることが分かりました。これらをまとめると、喫煙習慣と11種類の病気が遺伝学的に相関しているといえます(図2)。
特に、喫煙本数と後縦靱帯骨化症の遺伝学的相関は本研究で初めて明らかになったものです。これまで、喫煙本数と後縦靱帯骨化症の疫学調査では、その関連性は指摘されていませんでした。しかし今後、この関係を調べることで、病気の理解や発症予防の対策に役立つ可能性があると考えられます。

図2 喫煙習慣と病気の遺伝学的相関
喫煙習慣のGWAS結果を用いて43の病気との遺伝学的相関を評価したところ、11の病気と統計学的に有意な相関があった(図中の青い点)。青色は正の相関、例えば生まれつきタバコを吸いやすい傾向にある人がかかりやすい病気、赤色はその逆の相関を示している。なお、数値は相関係数(濃いほど強い相関)を示している。
さらに、喫煙習慣に関わる遺伝的変異が身体のどのような細胞組織の遺伝子調節領域に集中しているかを評価するため、細胞組織ごとのエピゲノム情報[8]と喫煙習慣のGWAS結果を照らし合わせたエンリッチメント解析[9]を行いました。その結果、喫煙歴の有無に関わる遺伝的変異は、中枢神経での遺伝子発現を調節する領域に多く存在することが明らかになりました(図3)。この結果は、これまでの欧米人を対象とした研究結果からも示されており、欧米人と日本人での喫煙歴の有無に関連する遺伝的背景に差はあるものの、生物学的に共通したメカニズムがあることを示しています。
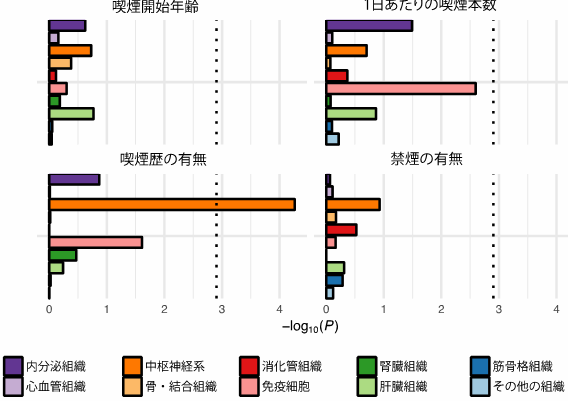
図3 喫煙習慣GWAS結果における組織特異性
喫煙習慣4項目について、横軸に各組織との関連の強さ、縦軸(色別)に組織を示した。点線は多重検定を考慮の上有意とみなすことのできる閾値を示している。喫煙歴の有無に関わる遺伝的変異は、中枢神経での遺伝子発現を調節する領域に多く存在することが分かった。
3.今後の期待
本研究成果は、喫煙習慣に影響する遺伝要因や、喫煙習慣と病気との関わり、生物学的に関連する組織など広範な視点から新しい知見を提供するものです。今後、喫煙習慣やそれに起因する病気の予防など幅広い科学分野での研究の発展に寄与するものと期待できます。
現在、理研研究チームは国際共同研究(the GWAS & Sequencing Consortium of Alcohol and Nicotine use [GSCAN] )を通して、喫煙習慣についてより理解を深めるための研究を進めています。
なお、本研究で利用したバイオバンク・ジャパンのサンプルの遺伝情報は、科学技術振興機構(JST)バイオサイエンスデータベースセンター(NBDC)、理研生命医科学研究センター統計解析研究チームが構築した日本人集団ゲノム関連解析情報データベース「Jenger注12)」を通じて一般公開されます。これらのデータを世界中の研究者が利用可能になることで、さらなる研究成果につながると考えられます。
- 注12)
- Japanese ENcyclopedia of GEnetic associations by Riken (Jenger).
4.論文情報
- タイトル
- GWAS of smoking behaviour in 165,436 Japanese people reveals seven new loci and shared genetic architecture
- 著者名
- Nana Matoba, Masato Akiyama, Kazuyoshi Ishigaki, Masahiro Kanai, Atsushi Takahashi, Yukihide Momozawa, Shiro Ikegawa, Masashi Ikeda, Nakao Iwata, Makoto Hirata, Koichi Matsuda, Michiaki Kubo, Yukinori Okada and Yoichiro Kamatani.
- 雑誌
- Nature Human Behaviour
- DOI
- 10.1038/s41562-019-0557-y
5.補足説明
- [1]バイオバンク・ジャパン
- 日本人集団27万人を対象とした生体試料バイオバンク。約20万人のゲノムデータを保有する。オーダーメイド医療の実現プログラムを通じて実施され、ゲノムDNAや血清サンプルを臨床情報とともに収集し、研究者へのデータ提供や分譲を行っている。
- [2]ゲノムワイド関連解析(GWAS)
- 病気や身長・体重など形質に影響がある遺伝的変異を、ゲノム全域に渡って網羅的に検索する遺伝統計的手法。GWASはGenome-Wide Association Studyの略。
- [3]慢性閉塞性肺疾患
- 肺気腫や慢性気管支炎の総称で、気道の閉塞による呼吸困難を引き起こす。世界保健機関(WHO)によれば、2030年までに世界の死亡原因の3位を占めるようになると推定されている。
- [4]後縦靱帯骨化症
- 背骨の後ろ側にあって背骨を縦につないでいる後縦靭帯が骨化することで起きる疾患。脊髄や神経を圧迫して、手や足のしびれや痛み、運動障害などさまざまな症状を引き起こす。日本での患者数は、潜在的な患者も含めると100万人以上と考えられている。
- [5]LDスコア
- 有限の大きさの生物集団では、ゲノム上の個人間の違いがある場所(遺伝的バリアント)は、近傍にあると互いに相関する(連鎖不平衡、Linkage disequilibrium;LD)。あるバリアントがより多くのバリアントとLDにあるなら、たまたま形質に関連するバリアントとLDにあって関連を示す確率が上がると考えられる。そのバリアントが周囲のバリアントとどれだけ多くLDにあるかの指標をLDスコアと呼ぶ。もしゲノム上には形質の原因バリアントが数十個弱しかないなら、LDスコアが示すのは単なる偶然の可能性に過ぎない。しかし、もし数千以上の原因バリアントがあるなら、無作為に取り出したあるバリアントは、それが原因かどうかにかかわらず、LDをもとに量的に遺伝的関連を示すと考えられる。実際に観察されているのは後者であり、このときさまざまな形質の遺伝的構造を、LDスコアを介して理解することが可能である。
- [6]UK Biobank
- 50万人という大人数を追跡するイギリスの前向きコホート研究であり、参加者の様々な臨床情報、ゲノムデータ、血液・尿バイオマーカー、画像データを収集している。とりわけ、申請次第で研究者に検体・データを供与すると言うシステムに特色があり、世界中の研究者が一斉にデータを取得・解析し、その結果がまた世界中で共有されると言うサイクルによりゲノム研究の世界が一変した。本研究でもこのようにして共有された解析データを使用している。
- [7]民族横断的な遺伝的相関
- 遺伝的相関は、ニつの形質の遺伝的構造がどの程度類似しているかを示す指標で、一般的にはGWASにより計算される遺伝的バリアントの効果量の相関として定義される。遺伝的相関が見られる理由としては、別々の形質であるが因果関係がある場合、生物学的経路を共有する同じサブグループの疾患である場合、多面的関連による場合などいくつかの可能性がある。GWAS結果により遺伝的相関を検出し、その後それが因果関係によるものと確認できたなら、創薬や疫学的介入などの実効性のある医学的成果へと結びつく可能性がある。ところで、集団における遺伝的バリアントの影響の大きさは、効果量とアレル頻度の関数として表される。単一集団の中ではアレル頻度は同じなので、定義通りに効果量だけを見て遺伝的相関を評価できる。ところが、欧米人と日本人というように異なった遺伝的集団の間で比較しようとした場合は、アレル頻度が異なる。そこで、従来法のように効果量を見るだけではなく、アレル頻度も同時に評価するようにしたのが「民族横断的な遺伝的相関(Transethnic genetic correlation)」である。
- [8]エピゲノム情報
- DNAの塩基配列情報に施される化学修飾のことで、環境などの影響で後天的に変化する。また、修飾の仕方は細胞や組織によってさまざまである。
- [9]エンリッチメント解析
- GWASが特定の仮説をおかず、客観的な統計学的評価を行うことを志向する解析であるのに対し、強い生物学的仮説を設定してオミックス・ビッグデータで検証する代表的手法。例えば本研究では、喫煙歴の有無に関わる遺伝的バリアントは中枢神経系細胞における遺伝子発現に影響を与えているだろう、そうならばこれらのバリアントは他の組織・細胞型と比較して、中枢神経での遺伝子発現を調節する領域に多く存在するはずだ、とまず仮説を立て、それを統計学的に検定した。
6.発表者・機関窓口
発表者
理化学研究所 生命医科学研究センター
統計解析研究チーム
チームリーダー 鎌谷 洋一郎(かまたに よういちろう)
機関窓口
理化学研究所 広報室 報道担当
AMED事業に関するお問い合わせ先
日本医療研究開発機構(AMED)
基盤研究事業部 バイオバンク課