2020-09-04 慶應義塾大学医学部,日本医療研究開発機構
慶應義塾大学医学部医化学教室の加部泰明准教授、末松誠教授および同整形外科学教室の古旗了伍助教らのグループは、マウス脂肪前駆細胞の分化誘導実験と肥満モデルマウスを用いた検討により、ヘム結合性膜タンパク質PGRMC1が脂肪細胞の脂質蓄積を亢進することを発見し、高脂肪食摂取による体重増加や白色脂肪組織の増大に大きく寄与することを発見しました。
同グループは2016年に、PGRMC1はさまざまな固形がんに高発現してがん増殖や薬剤耐性に関与することを発見しましたが、正常での生理機能については不明でした。本研究では、脂肪細胞の分化誘導の過程でPGRMC1の発現が誘導され、本分子が脂肪細胞における脂質や糖質の取り込みを増強することにより脂質蓄積を亢進することを明らかにしました。またマウス個体レベルにおいても、高脂肪食によって肥大化した脂肪組織においてPGRMC1が発現上昇し、体重増加と白色脂肪組織の肥大化を促進することが示されました。
これらの成果は、脂肪細胞における脂質と炭水化物の代謝調節を介した肥満の増進においてPGRMC1が極めて重要な役割を果たしていることを示しており、PGRMC1の機能制御を指標とした新規の抗肥満薬の開発や、メタボリックシンドロームへの治療戦略の構築につながる可能性があります。
本研究成果は、2020年9月4日(英国時間)にNature Publishing Group科学誌『Communications Biology』のオンライン速報版で公開されます。
研究の背景
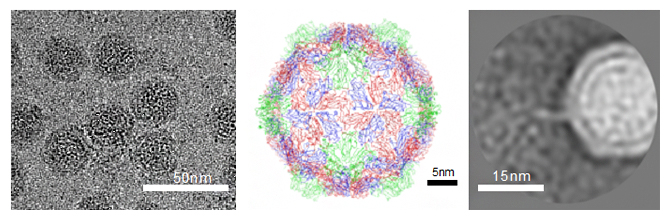
PGRMC1(progesterone receptor membrane associated component 1)は、当初ステロイドホルモンの一種であるプロゲステロン(注1)が結合する膜成分の一つとして同定されました。その後、乳がん、前立腺がん、卵巣がん、肝がん、肺がん、膵臓がんなどの多くの固形がんにおいて高発現していることが報告され、がん増殖に関わると考えられていましたが、このタンパク質の構造機能相関は長く不明なままでした。2016年に本研究グループは、PGRMC1タンパク質の構造解析(注2)に成功しました。さらに、PGRMC1が補欠分子(注3)であるヘム(注4)と結合して特異な2量体構造(ヘムスタッキング構造)を形成し、がん増殖に関わるEGF受容体(注5)や、抗がん剤分解に関わるシトクロームP450酵素(注6)に結合し活性化すること、またこの活性化が難治性がんの増悪や抗がん剤耐性に関わることを解明しました(参考文献1)。しかし、正常組織におけるPGRMC1の役割はその後も不明でした。本研究では、未知であったPGRMC1の生理機能について検討を行い、脂肪細胞におけるPGRMC1の新たな機能を見出し、肥満の亢進に関わることを発見しました。
研究の内容
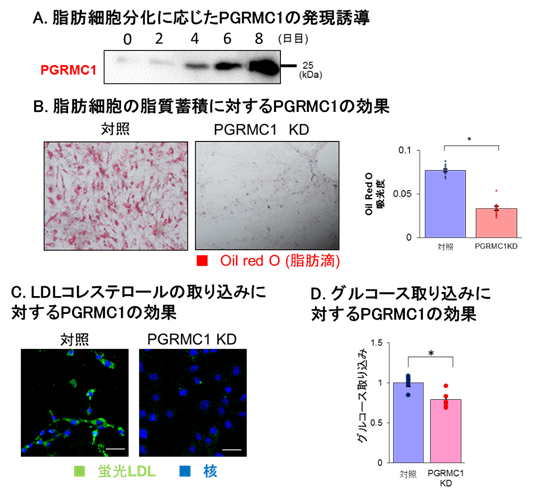
本研究グループは、まず、マウス由来の脂肪前駆細胞株である3T3L1細胞の分化誘導の過程において、PGRMC1が顕著に発現誘導されることを見出しました(図1A)。この発現誘導は、脂質蓄積を誘導するインスリンおよびPPARγ(注7)活性化剤の刺激によっても同様に生じました。さらに、PGRMC1発現を人為的に低下させた前駆細胞を分化誘導して得られた白色脂肪細胞では、正常な細胞と比較して脂肪滴(注8)の蓄積が著しく減少したことから、この分子が白色脂肪細胞の脂質の蓄積に必須であることが明らかになりました(図1B)。また、ヘムにより二量体化したPGRMC1が、脂質取り込みに関わるリポタンパク質受容体(VLDL-RおよびLDL-R)や細胞内に糖を取り込むグルコーストランスポーター(GLUT4)と相互作用することによって、細胞内に存在するLDL-RやGLUT4の細胞膜上への移行が促進され、またこれらが活性化されることにより、脂肪細胞の脂質や糖質の取り込みが促進されることが解明されました(図1C、D)。
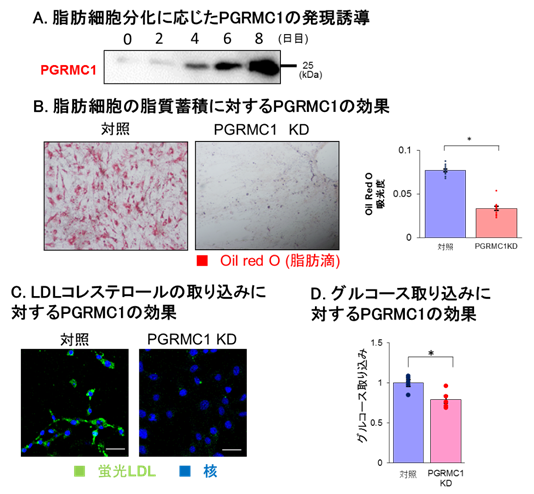
図1 脂肪細胞におけるPGRMC1の作用A.脂肪細胞分化に応じたPGRMC1の発現誘導。
B.脂肪細胞の脂質蓄積に対するPGRMC1の効果。PGRMC1の発現抑制(ノックダウン:KD)により脂肪滴(oil red O染色)が顕著に抑制される。
C.LDLコレステロール取り込みに対するPGRMC1の効果。PGRMC1抑制(KD)で蛍光標識LDLの脂肪細胞への取り込みが抑制される。
D.グルコース取り込みに対するPGRMC1の効果。PGRMC1抑制(KD)でグルコースの脂肪細胞への取り込みが抑制される。
さらに、高脂肪食により起こるマウス肥満モデルでは、肥満の増大に応じて脂肪組織におけるPGRMC1の発現が誘導されることが明らかになりました。さらに、脂肪組織特異的にPGRMC1の発現をノックアウトしたマウスを作出したところ、高脂肪食による体重増加および白色脂肪細胞の肥大が顕著に抑制されることが明らかになりました(図2)。この脂肪組織特異的PGRMC1ノックアウトマウスでは、血糖値やエネルギー代謝能などには影響を示さないことから、脂肪組織における脂質の蓄積に特異的に作用していることが示唆されました。
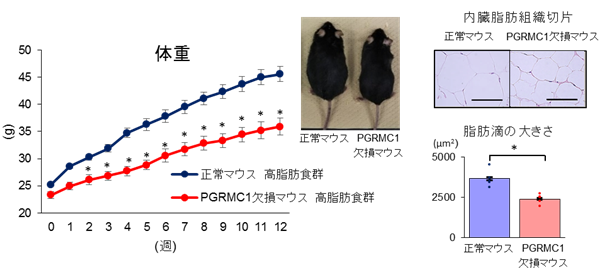
図2 高脂肪食下におけるPGRMC1欠損マウスの体重減少および白色脂肪縮小効果
以上の結果から、脂肪細胞の分化誘導によりPGRMC1の発現が亢進し、さらにヘムの重合によりPGRMC1は2量体化することで、脂質と炭水化物(グルコース)の摂取が亢進することによって、脂肪細胞内の脂質蓄積を亢進させ、白色脂肪細胞の肥大などによる肥満の増進に大きく寄与することが初めて明らかになりました(図3)。
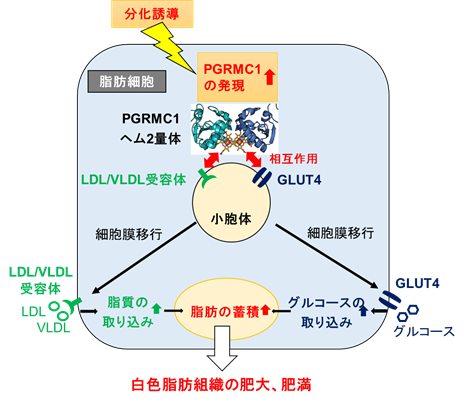
図3 脂肪細胞におけるPGRMC1の脂質蓄積作用のモデル図
研究の意義・今後の展開
栄養過多により内臓脂肪などが増大する肥満は、心疾患や脳卒中などの血管疾患や糖尿病などのメタボリックシンドロームの要因となり大きな問題となっています。本研究成果は、脂肪細胞における脂質と炭水化物の代謝調節を介した肥満の増進におけるPGRMC1の極めて重要な役割を示しています。この知見に基づいてPGRMC1の機能を抑制する薬剤などを開発することにより、メタボリックシンドロームに対する新たな治療戦略の構築に発展することが期待されます。
特記事項
本研究は、国立研究開発法人日本医療研究開発機構革新的先端研究開発支援事業ユニットタイプ「疾患における代謝産物の解析および代謝制御に基づく革新的医療基盤技術の創出」研究開発領域「代謝システム制御分子の系統的探索による治療戦略創出と創薬展開」、JSPS科研費JP18K06921および国立研究開発法人科学技術振興機構戦略的創造研究推進事業(JST-ERATO、末松ガスバイオロジープロジェクト)の支援により行われました。末松教授は、本研究に関する研究開発費をAMEDから受給していません。
論文
- 英文タイトル
- Progesterone receptor membrane associated component 1 enhances obesity progression in mice by facilitating lipid accumulation in adipocytes
- タイトル和訳
PGRMC1は脂肪細胞の脂質蓄積を増強することにより肥満の増大を促進する - 著者名
- 古旗了伍、加部泰明、金井彩香、杉浦悠毅、津川仁、杉山栄次、平井美和、山本雄広、小池一康、吉川賢忠、田中廣壽、小関正博、中江淳、松本守雄、中村雅也、末松誠
- 掲載誌:Communications Biology(オンライン速報版)
- DOI:10.1038/s42003-020-01202-x
用語解説
- (注1)プロゲステロン
- 黄体ホルモンとも呼ばれ月経周期の制御などに関わることが知られている。
- (注2)構造解析
- 目的タンパク質の結晶を用いたX線解析によりタンパク質の高次構造を解析した。
- (注3)補欠分子
- タンパク質の活性に不可欠な非タンパク質性の物質。ヘムや金属イオンなど知られる。
- (注4)ヘム
- 2価の鉄原子とポルフィリンから成る錯体であり、ヘモグロビンなどの酸素運搬や酸化還元酵素の補因子として働く。
- (注5)EGF受容体
- 細胞の増殖を促進する上皮成長因子(EGF)の受容体であり、いくつかのがん細胞ではこの機能が亢進して悪性度が増強することが知られる。
- (注6)シトクロームP450酵素
- 薬物代謝、解毒に関与する酸化酵素ファミリーで抗がん剤の不活性化にも関わることが知られる。
- (注7)PPARγ
- リガンド応答性転写因子である核内受容体の一つであり、脂肪細胞分化などに関与し、インスリン抵抗性改善薬の標的分子でもある。
- (注8)脂肪滴
- 中性脂肪やコレステロールなどの脂質を貯蔵する液滴状の細胞小器官。
参考文献
- タイトル:Haem-dependent dimerization of PGRMC1/Sigma-2 receptor facilitates cancer proliferation and chemoresistance
- 掲載誌:Nature Communications誌
- DOI:10.1038/ncomms11030
お問い合わせ先
本発表資料のお問い合わせ先
慶應義塾大学医学部 医化学教室 准教授 加部泰明(かべやすあき)
本リリースの配信元
慶應義塾大学 信濃町キャンパス総務課:山崎・飯塚
AMEDに関すること
国立研究開発法人日本医療研究開発機構 シーズ開発・基盤研究基盤事業部 革新的先端研究開発課