2020-09-29 金沢大学,日本医療研究開発機構
金沢大学がん進展制御研究所/ナノ生命科学研究所の矢野聖二教授、がん進展制御研究所/新学術創成研究機構の鈴木健之教授、京都府立医科大学の山田忠明病院准教授らの共同研究グループは、分子標的薬(※1)にさらされた肺がん細胞が、インスリン様増殖因子1受容体(IGF-1R)(※2)のタンパク質量を増やすことにより、抵抗し生き延びることを初めて明らかにしました。
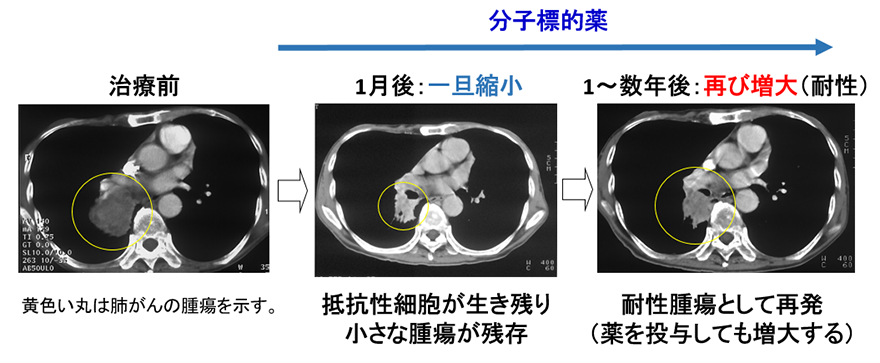
がんの分子標的薬は、効果があった場合でも腫瘍の一部が抵抗性細胞(※3)として生き残り、耐性のがんとして再発することが問題でした。
本研究グループは、日本人の肺がんの約20%を占めるEGFR変異肺がん(※4)において、分子標的薬にさらされた腫瘍細胞の一部が抵抗して生き残るメカニズムを解明しました。さらに、動物実験において分子標的薬にIGF-1R阻害薬を短期間併用することにより、肺がん細胞をほぼ死滅させ、再発をほとんど防ぐことにも成功しました。
本研究成果は、将来、肺がんを根治させる治療につながるものと期待されます。
本研究成果は、2020年9月14日(英国時間)に英国科学誌『Nature Communications』のオンライン版に掲載されました。
研究の背景
肺がんは、年間約8万人が死亡するわが国のがん死亡原因第一位のがんです。日本人の肺がんの約20%は、上皮成長因子受容体(epidermal growth factor receptor:EGFR)という遺伝子の変異が原因の肺がん(EGFR変異肺がん)で、その頻度は欧米人(10%以下)よりも高いのが特徴です。EGFR変異肺がんは変異したEGFRからの生存シグナルで増殖しており、変異EGFRの機能を抑えるオシメルチニブ(※5)という分子標的薬が有効です。オシメルチニブは、約8割のEGFR変異肺がんに劇的に効いて腫瘍を一旦小さくしますが、一部のがん細胞が抵抗性細胞として生き残り、1年から数年後に耐性のがんとして再発することが問題になっています(図1)。
本研究グループは、これまでに、EGFR変異肺がんのうちAXL(アクセル、※6)というタンパク質を多く発現したがん細胞はオシメルチニブが効きにくく、その原因はAXLが生存シグナルを補うことで抵抗性細胞を生み出し、耐性の温床になることを報告していました(Nature Communications, 2019)(図2)。

研究成果の概要
本研究では、AXL低発現のEGFR変異肺がんについて解析し、分子標的薬オシメルチニブにさらされた腫瘍細胞の一部が抵抗し生き残るメカニズムを解明しました(図3)。
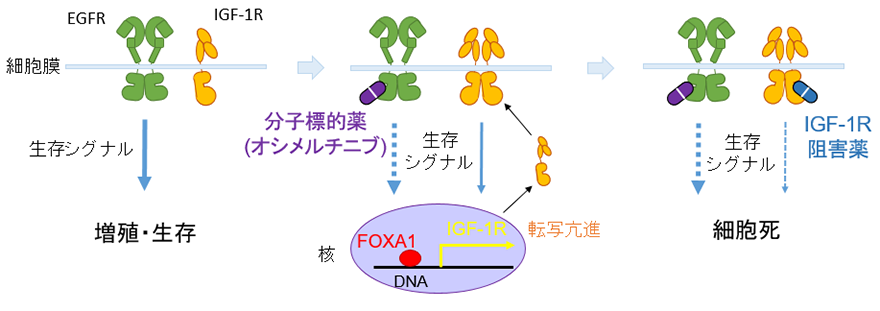
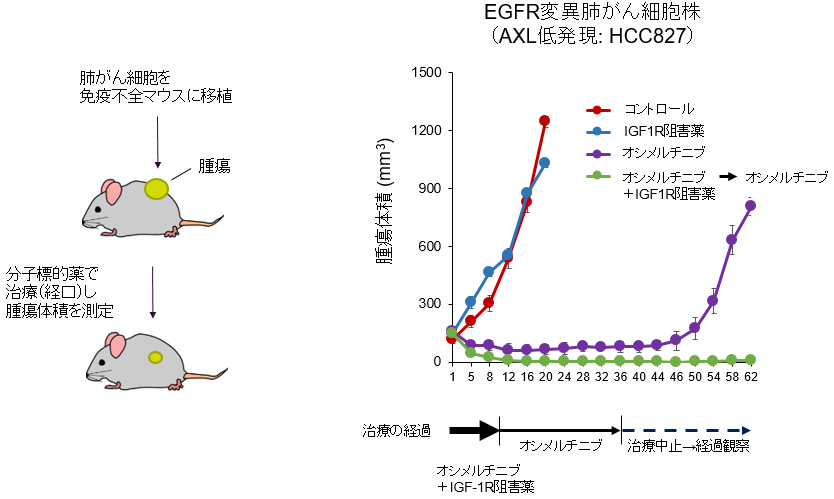
AXL低発現のEGFR変異肺がん細胞は、1)オシメルチニブが効きやすいものの、やはり一部のがん細胞が抵抗性細胞として生き残り、最終的には耐性がんとして再発してしまいました。そのメカニズムとしては、2)インスリン様増殖因子1受容体(insulin-like growth factor-1 receptor:IGF-1R)のタンパク質量を増やし、増えたIGF-1Rが生存シグナルを補うことで、がん細胞の一部が抵抗性細胞として生き延びていました。さらに、3)抵抗性細胞ではオシメルチニブ処理に応答して、転写因子(※7)であるFOXA1(※8)がIGF-1Rの転写を亢進してIGF-1Rのタンパク質量を増やすことを発見しました。4)動物モデルでは、オシメルチニブに短期間(動物モデルでは40日間治療のうちの10日間)IGF-1R阻害薬を併用することで腫瘍を消失させ、治療を止めても再発をほぼ完全に防げることを明らかにしました(図4)。
IGF-1Rはこれまでにもがん治療の標的と考えられてきましたが、インスリン受容体と非常に形が似ているため、薬で長期間IGF-1Rを阻害しようとするとインスリン受容体まで阻害してしまい、生体の糖代謝に重要なインスリンの働きを狂わせるため、大きな副作用が出ることが問題でした。本研究では、分子標的薬にIGF-1R阻害薬を短期間併用することで、大きな副作用なく腫瘍をほぼ根治できることを見いだしました。
また、抵抗性細胞が生き残るにはFOXA1という転写因子が働いてIGF-1Rのタンパク質量が増える必要があることを明らかにしました。従って、FOXA1の働きを阻害する薬を開発できればインスリン受容体には作用せず、IGF-1Rのみを阻害し分子標的薬の効果を増強できる可能性があります。
今後の展開
本研究成果により、AXL低発現のEGFR変異肺がん患者に、治療当初から短期間IGF-1R阻害薬を分子標的薬に併用することで、腫瘍を消しきり、根治あるいは再発までの期間を劇的に伸ばすことが期待されます。また、FOXA1の機能を抑制する薬剤はインスリン受容体には影響せずIGF-1Rのみを抑制できる可能性があり、今後FOXA1阻害薬の開発を目指します。
本研究への支援
本研究は、国立研究開発法人日本医療研究開発機構(AMED)次世代がん医療創生研究事業「MAPKシグナル抑制が誘導するフィードバック機構の不均一性解明と制御に基づくKRAS/BRAF変異腫瘍に対する新規治療開発」(研究代表者矢野聖二)、日本学術振興会科学研究費助成事業、金沢大学がん進展制御研究所共同研究費などの支援を受けて実施されました。
掲載論文
- 雑誌名
- Nature Communications
- 論文名
- Transient IGF-1R inhibition combined with osimertinib eradicates AXL-low expressing EGFR mutated lung cancer
- (オシメルチニブと一過性のIGF-1R阻害の併用はAXL低発現のEGFR変異肺がんを根絶する)
- 著者名
- Rong Wang, Tadaaki Yamada, Kenji Kita, Hirokazu Taniguchi, Sachiko Arai, Koji Fukuda, Minoru Terashima, Akihiko Ishimura, Akihiro Nishiyama, Azusa Tanimoto, Shinji Takeuchi, Koshiro Ohtsubo, Kaname Yamashita, Tomoyoshi Yamano, Akihiro Yoshimura, Koichi Takayama, Kyoichi Kaira, Yoshihiko Taniguchi, Shinji Atagi, Hisanori Uehara, Rikinari Hanayama, Isao Matsumoto, Xujun Han, Kunio Matsumoto, Wei Wang, Takeshi Suzuki, Seiji Yano
- (Wang Rong、山田忠明、北賢二、谷口寛和、新井祥子、福田康二、寺島農、石村昭彦、西山明宏、谷本 梓、竹内伸司、大坪公士郎、山下要、山野友義、吉村彰紘、高山浩一、解良恭一、谷口善彦、安宅信二、上原久典、華山力成、松本勲、Han Xujun、松本邦夫、Wang Wei、鈴木健之、矢野聖二)
- 掲載日時
- 2020年9月14日(英国時間)にオンライン版に掲載
- DOI
- 10.1038/s41467-020-18442-4
用語解説
- ※1 分子標的薬
- がんの増殖や生存に重要な役割を果している分子にピンポイントで作用する薬。2001年に白血病に対するイマチニブ(商品名グリベック)と乳がんに対するトラスツズマブ(商品名ハーセプチン)が認可されたのを皮切りに、日本では現在40種類以上の分子標的薬ががんに対して認可されている。
- ※2 インスリン様増殖因子1受容体(insulin-like growth factor-1 receptor:IGF-1R)
- インスリンと類似した増殖因子であるIGF-1の受容体。さまざまながんで発現されており、増殖や薬剤耐性に関与する。
- ※3 抵抗性細胞
- 分子標的薬にさらされた時に増殖を停止して生き残る細胞。抵抗性細胞にさらなる何らかの変化が起こると増殖できるようになり、耐性腫瘍を形成する温床になる。
- ※4 EGFR変異肺がん
- 上皮成長因子受容体(EGFR)の遺伝子に変異が生じて発生する肺がんで、日本人の肺がんの約20%を占める。変異EGFRタンパク質からのシグナルにより生存・増殖しており、これを抑制する分子標的薬であるEGFRチロシンキナーゼ阻害薬がよく効く。
- ※5 オシメルチニブ
- 商品名はタグリッソ。第一世代EGFRチロシンキナーゼ阻害薬であるゲフィチニブやエルロチニブに耐性となるEGFR-T790M変異に対しても効果を発揮する第三世代EGFRチロシンキナーゼ阻害薬として開発された。進行期EGFR変異肺がんの初回治療として用いても、ゲフィチニブやエルロチニブよりも有効であることが臨床試験で示されており、現在EGFR変異肺がんに最も有効な新世代分子標的薬である。
- ※6 AXL(アクセル)
- Gas6というタンパク質が結合する受容体タンパク質で、細胞膜に存在する。がん細胞に過剰に発現されていることが知られており、増殖や転移、薬剤耐性などに関与する。
- ※7 転写因子
- DNAに特異的に結合するタンパク質。DNAの遺伝情報をRNAに転写する過程を促進する。転写因子は複数の他のタンパク質と複合体を形成することにより転写を促進する。
- ※8 FOXA1(Forkhead box protein A1:フォックスA1)
- フォークヘッド転写因子ファミリーの一つ。転写されるDNA上に最初に結合し、転写に必要な他の因子を呼び寄せることで転写を促すため、パイオニア転写因子ともよばれる。
本件に関するお問い合わせ先
研究内容に関すること
金沢大学がん進展制御研究所/ナノ生命科学研究所 教授
矢野聖二(やのせいじ)
広報担当
金沢大学総務部広報室広報係
上沼孝平(かみぬまたかひら)
金沢大学医薬保健系事務部薬学・がん研支援課企画総務係
岡田あゆみ(おかだあゆみ)
金沢大学ナノ生命科学研究所事務室
米田洋恵(よねだひろえ)
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
創薬事業部医薬品研究開発課