2026-04-15 ノースウェスタン大学
<関連情報>
- https://news.northwestern.edu/stories/2026/4/printed-neurons-communicate-with-living-brain-cells
- https://www.nature.com/articles/s41565-026-02149-6
多次複雑性を持つスパイクニューロンのための印刷されたMoS₂メモリスティブナノシートネットワーク Printed MoS2 memristive nanosheet networks for spiking neurons with multi-order complexity
Shreyash S. Hadke,Carol N. Klingler,Spencer T. Brown,Meghana Holla,Xudong Zhuang,Linda Li,M. Iqbal Bakti Utama,Santiago Diaz-Arauzo,Anurag Chapagain,Siyang Li,Jung Hun Lee,Indira M. Raman,Vinod K. Sangwan & Mark C. Hersam
Nature Nanotechnology Published:15 April 2026
DOI:https://doi.org/10.1038/s41565-026-02149-6
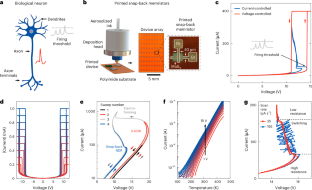
Abstract
Artificial neurons that reproduce the rich dynamical behaviour of biological spiking are essential for neuromorphic hardware and biohybrid interfaces, yet scalable solution-processed devices with physiologically relevant spiking characteristics remain elusive. Here we demonstrate aerosol-jet-printed memristive networks of MoS2 nanosheets that exhibit thermally activated filamentary switching and snap-back negative differential resistance, enabling volatile threshold switching in fully printed graphene/MoS2/graphene devices on flexible substrates. In situ thermal imaging and circuit modelling reveal that current-constricted filaments formed through Joule heating govern the nonlinear switching dynamics. These printed memristors enable oscillatory and spiking neuron circuits with tunable frequencies up to 20 kHz and stable operation over more than 106 cycles. Simple neuristor circuits realize first-, second- and third-order spiking complexity, including integrate-and-fire behaviour, spike latency, tonic firing, class 1 excitability, tonic bursting and phasic dynamics. The generated spike waveforms match physiological timescales and stimulate Purkinje neurons in mouse cerebellar slices. Our results establish printed nanosheet memristive networks as a scalable platform for bio-realistic neuromorphic hardware and flexible brain–machine interfaces.

